Adenozin -deamináz - Adenosine deaminase
| Adenozin/AMP deamináz | |||||||||
|---|---|---|---|---|---|---|---|---|---|
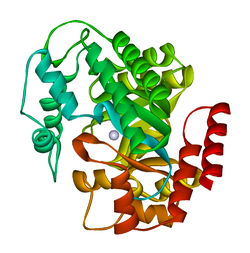
 A plazmodium yoelii adenozin -deamináz kristályszerkezete (py02076)
| |||||||||
| Azonosítók | |||||||||
| Szimbólum | A_deaminase | ||||||||
| Pfam | PF00962 | ||||||||
| Pfam klán | CL0034 | ||||||||
| InterPro | IPR001365 | ||||||||
| PROSITE | PDOC00419 | ||||||||
| SCOP2 | 1add / SCOPe / SUPFAM | ||||||||
| CDD | cd01320 | ||||||||
| |||||||||
| Adenozin -deamináz (szerkesztő) domain | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Azonosítók | |||||||||
| Szimbólum | A_deamin | ||||||||
| Pfam | PF02137 | ||||||||
| InterPro | IPR002466 | ||||||||
| PROSITE | PDOC00419 | ||||||||
| SCOP2 | 1add / SCOPe / SUPFAM | ||||||||
| |||||||||
| Adenozin/AMP deamináz N-terminális | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Azonosítók | |||||||||
| Szimbólum | A_deaminase_N | ||||||||
| Pfam | PF08451 | ||||||||
| InterPro | IPR013659 | ||||||||
| |||||||||
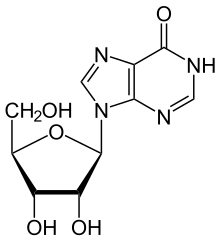
Az adenozin -deamináz (más néven adenozin -aminohidroláz vagy ADA ) egy enzim ( EC 3.5.4.4 ), amely részt vesz a purin -anyagcserében . Szükség van az adenozin lebontására az élelmiszerekből és a szövetekben a nukleinsavak cseréjéhez.
Elsődleges funkciója az emberben az immunrendszer fejlesztése és fenntartása. Az ADA teljes fiziológiai szerepe azonban még nem teljesen ismert.
Szerkezet
Az ADA kis formában (monomer formájában) és nagy formában (dimer-komplex formájában) létezik. Monomer formában az enzim egy polipeptid lánc, amely párhuzamos α/β hordók nyolc szálába hajtogatott, és amelyek egy központi mély zsebet vesznek körül, amely az aktív hely. A nyolc központi β-hordón és nyolc perifériás α- hélixen kívül az ADA öt további hélixet is tartalmaz: a 19-76. és két anti-párhuzamos karboxi-terminális hélix található a β-hordó amino-terminálisán.
Az ADA aktív hely egy cink -iont tartalmaz, amely az aktív hely legmélyebb mélyedésében található, és amelyet a His15, His17, His214, Asp295 és a szubsztrát öt atomja koordinál. A cink az egyetlen kofaktor, amely szükséges a tevékenységhez.
A szubsztrát, az adenozin stabilizálódik, és kilenc hidrogénkötéssel kötődik az aktív helyhez. A Glu217 karboxilcsoportja, nagyjából egy síkban a szubsztrát puringyűrűjével, abban a helyzetben van, hogy hidrogénkötést hoz létre a szubsztrát N1 -jével. Az Asp296 karboxilcsoportja, amely szintén egy síkban van a szubsztrát puringyűrűjével, hidrogénkötést képez a szubsztrát N7 -gyel. A Gly184 NH csoportja abban a helyzetben van, hogy hidrogénkötést hoz létre a szubsztrát N3 -jával. Az Asp296 kötéseket képez mind a Zn 2+ ionnal, mind a szubsztrát 6-OH- jával . His238 szintén hidrogénkötést köt a 6-OH szubsztráthoz. A szubsztrát ribóz 3'-OH hidrogénkötést képez Asp19-gyel, míg az 5'-OH hidrogénkötést képez His17-gyel. Két további hidrogénkötés jön létre a vízmolekulákhoz az aktív hely nyitásakor a szubsztrát 2'-OH és 3'-OH által.
Az enzim belsejében lévő aktív hely bemélyedése miatt a megkötött szubsztrát szinte teljesen elválik az oldószertől. A szubsztrátum felületi expozíciója az oldószerhez kötéskor 0,5% a hordozó felületi expozíciója szabad állapotban.
Reakciók
Az ADA visszafordíthatatlanul dezaminálja az adenozint, átalakítja azt rokon nukleozid inozinná azáltal, hogy az aminocsoportot ketocsoporttal helyettesíti .
Inozin ezután deribosylated (távolítani ribóz ) egy másik enzim, az úgynevezett purin-nukleozid-foszforiláz (PNP), átalakítva azt hipoxantin .
A katalízis mechanizmusa
Az ADA által katalizált dezaminálás javasolt mechanizmusa a sztereospecifikus addíció-elimináció a tetraéderes intermedier segítségével. Bármelyik mechanizmus szerint a Zn 2+ erős elektrofilként aktiválja a vízmolekulát, amelyet az Asp295 bázikus deprotonál, hogy támadó hidroxidot képezzen. His238 orientálja a vízmolekulát és stabilizálja a támadó hidroxid töltését. A Glu217 protonálásával protont adományoz a szubsztrát N1 -jének.
A reakció sztereospecifikus a cink-, Asp295- és His238-maradékok elhelyezkedése miatt, amelyek mindegyike a szubsztrát puringyűrűjének B-oldala felé néz.
Versenyképes gátlást figyeltek meg az ADA esetében, ahol az inozin termék az enzimaktivitás kompetitív gátlójára hat.
Funkció
Az ADA -t a purin -anyagcsere egyik legfontosabb enzimének tekintik. Az enzimet baktériumokban, növényekben, gerinctelenekben, gerincesekben és emlősökben találták , aminosavszekvenciája nagymértékben megőrződött . Az aminosavszekvencia nagyfokú megőrzése azt sugallja, hogy az ADA döntő jelentőségű a purinmentő útban.
Elsősorban az ADA emberekben vesz részt az immunrendszer fejlesztésében és fenntartásában. Azonban az ADA asszociációt megfigyelték a hámsejtek differenciálódásával , a neurotranszmisszióval és a terhesség fenntartásával is. Azt is javasolták, hogy az ADA az adenozin lebontása mellett serkenti az izgató aminosavak felszabadulását, és szükséges az A1 adenozin receptorok és a heterotrimer G fehérjék kapcsolásához . Az adenozin -deamináz -hiány tüdőfibrózishoz vezet, ami arra utal, hogy a magas adenozin -szint krónikus expozíciója súlyosbíthatja a gyulladásos reakciókat, nem pedig elnyomhatja azokat. Azt is felismerték, hogy az adenozin-deamináz fehérje és aktivitása felül van szabályozva a HIF1α túlexpresszáló egér szívekben , ami részben megmagyarázza az adenozin gyengített szintjét a HIF-1α kifejező szívekben ischaemiás stressz alatt .
Patológia
Az adenozin -deamináz gén egyes mutációi miatt nem expresszálódik. Az ebből eredő hiány a súlyos kombinált immunhiány (SCID), különösen az autoszomális recesszív öröklődés egyik oka . Az ADA hiányos szintje tüdőgyulladással, thymussejt-elhalással és hibás T-sejt-receptor jelzéssel is összefüggésbe hozható.
Ezzel szemben az enzim túlexpresszálódását okozó mutációk a hemolitikus anaemia egyik oka .
Van néhány bizonyíték arra, hogy egy másik allél (ADA2) autizmushoz vezethet .
Az ADA emelkedett szintjét AIDS -szel is összefüggésbe hozták .
Izoformák
Az ADA -nak 2 izoformája van: ADA1 és ADA2.
- Az ADA1 megtalálható a legtöbb sejtben, különösen a limfocitákban és a makrofágokban , ahol nemcsak a citoszolban és a sejtmagban van jelen, hanem a dipeptidil-peptidáz-4-hez (más néven CD26) kapcsolódó sejtmembránon lévő ekto-forma formájában is . Az ADA1 főként az intracelluláris aktivitásban vesz részt, és kis formában (monomer) és nagy formában (dimer) is létezik. A kis és nagy formák közötti átalakulást a tüdőben lévő „konverziós tényező” szabályozza.
- Az ADA2 -t először emberi lépben azonosították. Ezt követően más szövetekben is megtalálták, beleértve a makrofágot is, ahol az ADA1-gyel együtt létezik. A két izoforma szabályozza az adenozin és a dezoxi -adenozin arányát, fokozva a paraziták elpusztítását. Az ADA2 túlnyomórészt a humán plazmában és szérumban található, és kizárólag homodimer formájában létezik.
Klinikai jelentőség
Az ADA2 az emberi vérplazmában uralkodó forma, és számos betegségben, különösen az immunrendszerrel összefüggésben fokozódik: például a reumás ízületi gyulladásban , a pikkelysömörben és a szarkoidózisban . A plazma ADA2 izoforma a legtöbb rák esetében is megemelkedik. Az ADA2 nem mindenütt jelen van, de az ADA1-gyel együtt csak monociták-makrofágokban létezik.
A teljes plazma ADA nagy teljesítményű folyadékkromatográfiával vagy enzimatikus vagy kolorimetriás technikákkal mérhető . Talán a legegyszerűbb rendszer az inozinra bontva adenozinból felszabaduló ammónia mérése . A plazma pufferolt adenozin -oldattal történő inkubálása után az ammóniát Berthelot -reagenssel reagáltatva kék színűvé válik, amely arányos az enzimaktivitás mennyiségével. Az ADA2 méréséhez eritro-9- (2-hidroxi-3-nonil) -adenint ( EHNS ) adunk az inkubálás előtt, hogy gátoljuk az ADA1 enzimatikus aktivitását. Az ADA1 hiánya okozza az SCID -t .
Az ADA a limfocitikus pleurális effúziók vagy a peritoneális ascites feldolgozásában is alkalmazható, mivel az alacsony ADA -szinttel rendelkező minták lényegében kizárják a tuberkulózist.
A tuberkulózis pleurális effúzióit ma már pontosan lehet diagnosztizálni a pleurális folyadék adenozin -deamináz szintjének megnövekedett szintjével, 40 E / liter felett.
A kladribin és a pentosztatin daganatellenes szerek, amelyeket szőrös sejtes leukémia kezelésére használnak ; hatásmechanizmusuk az adenozin -deamináz gátlása.
Lásd még
Hivatkozások
További irodalom
- da Cunha JG (1992). "[Adenozin -deamináz. Egy pluridiszciplináris enzim]". Acta Médica Portuguesa . 4 (6): 315–23. PMID 1807098 .
- Franco R, Casadó V, Ciruela F, Saura C, Mallol J, Canela EI, Lluis C (1997. július). "Sejtfelszíni adenozin -deamináz: sokkal több, mint egy ektoenzim". A neurobiológia fejlődése . 52. (4): 283–94. doi : 10.1016/S0301-0082 (97) 00013-0 . PMID 9247966 . S2CID 40318396 .
- Valenzuela A, Blanco J, Callebaut C, Jacotot E, Lluis C, Hovanessian AG, Franco R (1997). "A gp120 HIV-1 boríték és a vírusrészecskék blokkolják az adenozin-deamináz kötődését a humán CD26-hoz". A kísérleti orvostudomány és a biológia fejlődése . 421 : 185–92. doi : 10.1007/978-1-4757-9613-1_24 . ISBN 978-1-4757-9615-5. PMID 9330696 .
- Moriwaki Y, Yamamoto T, Higashino K (1999. október). "A purin anyagcserében részt vevő enzimek-a hisztokémiai lokalizáció és a funkcionális következmények áttekintése". Szövettan és szövettan . 14 (4): 1321–40. PMID 10506947 .
- Hirschhorn R (1993). "Két új missense mutáció (R156C és S291L) azonosítása két ADA-SCID betegben, amelyek szokatlanok a részleges csere-transzfúzióval történő kezelésre adott válaszra". Emberi mutáció . 1 (2): 166–8. doi : 10.1002/humu.1380010214 . PMID 1284479 . S2CID 44617309 .
- Berkvens TM, van Ormondt H, Gerritsen EJ, Khan PM, van der Eb AJ (1990. augusztus). "Azonos 3250 bp-s deléció két AluI ismétlés között a független ADA-SCID betegek ADA génjeiben". Genomika . 7 (4): 486–90. doi : 10.1016/0888-7543 (90) 90190-6 . PMID 1696926 .
- Aran JM, Colomer D, Matutes E, Vives-Corrons JL, Franco R (1991. augusztus). "Adenozin -deamináz jelenléte a mononukleáris vérsejtek felületén: immunokémiai lokalizáció fény- és elektronmikroszkóppal" . The Journal of Histochemistry and Cytochemistry . 39 (8): 1001–8. doi : 10.1177/39.8.1856451 . PMID 1856451 .
- Bielat K, Tritsch GL (1989. ápr.). "A humán eritrocita adenozin-deamináz ekto-enzimaktivitása". Molekuláris és celluláris biokémia . 86. (2): 135–42. doi : 10.1007/BF00222613 . PMID 2770711 . S2CID 20850552 .
- Hirschhorn R, Tzall S, Ellenbogen A, Orkin SH (1989. február). "Hőlabiális adenozin-deaminázt (ADA) eredményező pontmutáció azonosítása két, egymással nem rokon, részleges ADA-hiányos gyermekben" . A Journal of Clinical Investigation . 83 (2): 497–501. doi : 10.1172/JCI113909 . PMC 303706 . PMID 2783588 .
- Murray JL, Perez-Soler R, Bywaters D, Hersh EM (1986. január). "Csökkent adenozin -deamináz (ADA) és 5' -nukleotidáz (5NT) aktivitás a perifériás vér T -sejtjeiben Hodgkin -betegségben". American Journal of Hematology . 21. (1): 57–66. doi : 10.1002/ajh.2830210108 . PMID 3010705 . S2CID 25540139 .
- Wiginton DA, Kaplan DJ, States JC, Akeson AL, Perme CM, Bilyk IJ, Vaughn AJ, Lattier DL, Hutton JJ (1986. december). "A humán adenozin -deamináz génjének teljes szekvenciája és szerkezete". Biokémia . 25 (25): 8234–44. doi : 10.1021/bi00373a017 . PMID 3028473 .
- Akeson AL, Wiginton DA, Dusing MR, States JC, Hutton JJ (1988. november). "Mutáns humán adenozin -deamináz allélok és azok kifejeződése fibroblasztokká történő transzfekcióval" . The Journal of Biological Chemistry . 263 (31): 16291–6. doi : 10.1016/S0021-9258 (18) 37591-4 . PMID 3182793 .
- Glader BE, Backer K (1988. február). „Fokozott vörösvértest-adenozin-deamináz aktivitás: a rendezetlen eritropoézis jelzője Diamond-Blackfan vérszegénységben és más hematológiai betegségekben”. British Journal of Hematology . 68. (2): 165–8. doi : 10.1111/j.1365-2141.1988.tb06184.x . PMID 3348976 . S2CID 44789636 .
- Petersen MB, Tranebjaerg L, Tommerup N, Nygaard P, Edwards H (1987. február). "Az adenozin -deamináz génlókusz új hozzárendelése a 20q13 X 11 kromoszómához 20q intersticiális delécióval rendelkező beteg vizsgálatával" . Journal of Medical Genetics . 24 (2): 93–6. doi : 10.1136/jmg.24.2.93 . PMC 1049896 . PMID 3560174 .
- Orkin SH, Goff SC, Kelley WN, Daddona PE (1985. ápr.). "A humán adenozin -deamináz cDNS -ek átmeneti expressziója: egyetlen aminosav -szubsztitúcióból származó nem működő klón azonosítása" . Molekuláris és sejtbiológia . 5 (4): 762-7. doi : 10.1128/mcb.5.4.762 . PMC 366780 . PMID 3838797 .
- Valerio D, Duyvesteyn MG, Dekker BM, Weeda G, Berkvens TM, van der Voorn L, van Ormondt H, van der Eb AJ (1985. február). "Adenozin -deamináz: egy gén jellemzése és expressziója figyelemre méltó promóterrel" . Az EMBO folyóirat . 4 (2): 437–43. doi : 10.1002/j.1460-2075.1985.tb03648.x . PMC 554205 . PMID 3839456 .
- Bonthron DT, Markham AF, Ginsburg D, Orkin SH (1985. augusztus). "Pontmutáció azonosítása az immunhiányért felelős adenozin -deamináz génben" . A Journal of Clinical Investigation . 76. (2): 894-7. doi : 10.1172/JCI112050 . PMC 423929 . PMID 3839802 .
- Daddona PE, Shewach DS, Kelley WN, Argos P, Markham AF, Orkin SH (1984. október). "Humán adenozin -deamináz. CDNS és teljes elsődleges aminosavszekvencia" . The Journal of Biological Chemistry . 259 (19): 12101–6. doi : 10.1016/S0021-9258 (20) 71325-6 . PMID 6090454 .
- Valerio D, Duyvesteyn MG, Meera Khan P, Geurts van Kessel A, de Waard A, van der Eb AJ (1983. november). "CDNS -klónok izolálása humán adenozin -deaminázhoz". Gene . 25. (2–3): 231–40. doi : 10.1016/0378-1119 (83) 90227-5 . PMID 6198240 .
Külső linkek
- ADA humán gén elhelyezkedése az UCSC genomböngészőben .
- ADA humán gén részletei az UCSC genomböngészőben .
- A PDBe-KB áttekintést nyújt a humán adenozin-deaminázra vonatkozó EKT-ban rendelkezésre álló összes strukturális információról
- A PDBe-KB áttekintést nyújt az egér adenozin-deaminázra vonatkozó PDB-ben rendelkezésre álló összes strukturális információról