Bikarbonát - Bicarbonate
|
|

|
|
| Nevek | |
|---|---|
|
Szisztematikus IUPAC név
Hidroxidodioxidokarbonát (1−) |
|
| Más nevek
Hidrogén -karbonát
|
|
| Azonosítók | |
|
3D modell ( JSmol )
|
|
| 3DMet | |
| 3903504 | |
| ChEBI | |
| CHEMBL | |
| ChemSpider | |
| 49249 | |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
CompTox műszerfal ( EPA )
|
|
|
|
|
|
| Tulajdonságok | |
|
HCO- 3 |
|
| Moláris tömeg | 61,0168 g mol −1 |
| log P | −0,82 |
| Savasság (p K a ) | 10.3 |
| Alaposság (p K b ) | 7.7 |
| Konjugált sav | Szénsav |
| Konjugált bázis | Karbonát |
|
Eltérő rendelkezés hiányában az adatok a szabványos állapotú anyagokra vonatkoznak (25 ° C [77 ° F], 100 kPa). |
|
| Infobox hivatkozások | |
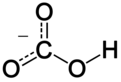
A szervetlen kémia , hidrogén-karbonát ( IUPAC -recommended nómenklatúra: -hidrogén-karbonát ) egy köztes formája a deprotonálódása a szénsav . Ez egy poliatomikus anion , amelynek kémiai képlete H C O-
3.
A bikarbonát kulcsfontosságú biokémiai szerepet tölt be a fiziológiás pH pufferelő rendszerben.
A "bikarbonát" kifejezést 1814 -ben William Hyde Wollaston angol vegyész alkotta meg . A "bi" előtag a "bikarbonát" -ban egy elavult elnevezési rendszerből származik, és azon a megfigyelésen alapul, hogy kétszer annyi karbonát van ( CO2−
3) nátrium -iononként nátrium -hidrogén -karbonátban ( NaHCO 3 ) és más bikarbonátokban, mint nátrium -karbonátban (Na 2 CO 3 ) és más karbonátokban. A név triviális névként él tovább .
Kémiai tulajdonságok
A hidrogén-karbonát-ion (hidrogén-karbonát-ion) egy anion a tapasztalati képletű HCO-
3és 61,01 dalton molekulatömegű ; ez áll egy központi szénatom atom körül három oxigénatom egy trigonális síkbeli elrendezése, egy hidrogénatom kapcsolódik az egyik oxigénatomot tartalmaz. Ez izoelektronos a salétromsav HNO
3. A hidrogén -karbonát ion negatív formai töltést hordoz, és amfiprotikus faj, amely savas és bázikus tulajdonságokkal is rendelkezik. Hogy mind a konjugált bázisa a szénsav H
2CO
3; és a konjugált sav a CO2−
3, a karbonát -ion, amint ezeket az egyensúlyi reakciók mutatják :
-
CO2−
3+ 2 H 2 O ⇌ HCO-
3+ H 2 O + OH - ⇌ H 2 CO 3 + 2 OH -
- H 2 CO 3 + 2 H 2 O ⇌ HCO-
3+ H 3 O + + H 2 O ⇌ CO2−
3+ 2 H 3 O + .
A hidrogén -karbonát -só akkor képződik, amikor pozitív töltésű ion kapcsolódik az ion negatív töltésű oxigénatomjaihoz, ionos vegyületet képezve . Sok hidrogén-karbonátok oldódik a vízben a standard hőmérsékleten és nyomáson ; különösen a nátrium -hidrogén -karbonát hozzájárul az összes oldott szilárd anyaghoz , ami a vízminőség értékelésének közös paramétere .
Fiziológiai szerep
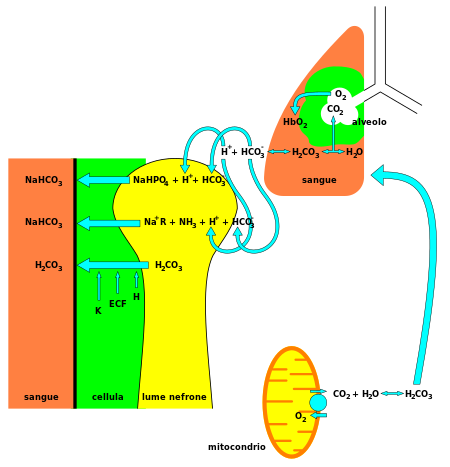
Bikarbonát ( HCO-
3) az emberi test pH -pufferelő rendszerének létfontosságú eleme (a sav -bázis homeosztázis fenntartása ). A szervezetben lévő CO 2 70–75% -a szénsavvá (H 2 CO 3 ) alakul át , amely a HCO konjugált savja-
3 és gyorsan be tud fordulni.
Szénsavval, mint a központi közbenső fajok , hidrogén-karbonát - együtt vízzel, hidrogén ionok , és a szén-dioxid - képezi ezt a puffer-rendszerek, amelyek tartjuk az illékony egyensúlyi szükséges, hogy gyors rezisztencia pH változásokat mind a savas és bázikus irányok . Ez különösen fontos a központi idegrendszer szöveteinek védelmében , ahol a pH túlságosan megváltozik a normál tartományon kívül, bármely irányba, katasztrofálisnak bizonyulhat (lásd acidózis vagy alkalózis ).
Ezenkívül a bikarbonát kulcsfontosságú szerepet játszik az emésztőrendszerben. Emeli a gyomor belső pH -ját, miután az erősen savas emésztőnedvek befejezték az élelmiszer emésztését. A bikarbonát szabályozza a vékonybél pH -ját is. A hasnyálmirigyből választódik ki a szekréciós hormon hatására, hogy semlegesítse a gyomorból a nyombélbe jutó savas chimet .
Bikarbonát a környezetben
A bikarbonát az oldott szervetlen szén domináns formája a tengervízben és a legtöbb édesvízben. Mint ilyen, ez a szén -dioxid -körforgás fontos elnyelője .
Az édesvízi ökológiában az édesvízi növények napközbeni erős fotoszintetikus aktivitása gáznemű oxigént bocsát ki a vízbe, és ugyanakkor bikarbonát -ionokat termel. Ezek a pH -t felfelé tolják, amíg bizonyos körülmények között a lúgosság mértéke egyes szervezetekre mérgezővé válhat, vagy más kémiai összetevőket, például az ammóniát mérgezővé teheti . Sötétben, amikor nem történik fotoszintézis, a légzési folyamatok szén -dioxidot szabadítanak fel, és nem keletkeznek új bikarbonát -ionok, ami a pH gyors csökkenését eredményezi.
Egyéb felhasználások
A bikarbonát -ion leggyakoribb sója a nátrium -hidrogén -karbonát , a NaHCO 3 , amelyet általában szódabikarbónának neveznek . Hevítés vagy sav , például ecetsav ( ecet ) hatásának kitéve a nátrium -hidrogén -karbonát szén -dioxidot szabadít fel . Ezt használják a térfogatnövelő szer a sütés .
A szénsav által mállott kőzetekből származó bikarbonát -ionok áramlása az esővízben a szénciklus fontos része .
Az ammónium -hidrogén -karbonátot az emésztéses kekszek gyártásához használják.
Diagnosztika
A diagnosztikai orvostudomány , a vér értéke bikarbonát egyike a számos mutatók állapotának sav-bázis fiziológia a szervezetben. A szén -dioxiddal , a kloriddal , a káliummal és a nátriummal együtt mérik az elektrolit szintjének meghatározását egy elektrolit panel tesztben (amelynek jelenlegi eljárási terminológiája CPT, 80051 kód).
A standard bikarbonát -koncentráció (SBC e ) paraméter a bikarbonát -koncentráció a vérben 40 Hgmm (5,33 kPa) P a CO 2 , teljes oxigéntelítettség és 36 ° C mellett.
Bikarbonát vegyületek
- Szódabikarbóna
- Kálium -hidrogén -karbonát
- Cézium -bikarbonát
- Magnézium -bikarbonát
- Kalcium -hidrogén -karbonát
- Ammónium -hidrogén -karbonát
- Szénsav
Lásd még
Hivatkozások
Külső linkek
- Hidrogén-karbonátok az amerikai National Library of Medicine orvosi tárgyszórendszere (mm)
