Lawesson reagens - Lawesson's reagent

|
|

|
|
| Nevek | |
|---|---|
|
IUPAC név
2,4-bisz (4-metoxi-fenil) -1,3,2,4-ditiadifoszfetán-2,4-diszulfid
|
|
|
Előnyben részesített IUPAC név
2,4-Bisz (4-metoxi-fenil) -1,3,2,4-ditiadifoszfetán-2,4-dition |
|
| Más nevek
Lawesson reagens; LR
|
|
| Azonosítók | |
|
3D modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100,038,944 |
|
PubChem CID
|
|
| UNII | |
|
CompTox műszerfal ( EPA )
|
|
|
|
|
|
| Tulajdonságok | |
| C 14 H 14 O 2 P 2 S 4 | |
| Moláris tömeg | 404,45 g · mol −1 |
| Megjelenés | Enyhén sárga por |
| Olvadáspont | 228–231 ° C (442–448 ° F; 501–504 K) |
| Oldhatatlan | |
| Veszélyek | |
|
EU besorolás (DSD) (elavult)
|
Irritatív, ártalmas (XN) |
| R-mondatok (elavult) | R15/29 - R20/21/22 |
| S-mondatok (elavult) | S7/8 - S22 - S45 |
| Rokon vegyületek | |
|
Kapcsolódó thiation szerek
|
Hidrogén -szulfid , foszfor -pentaszulfid |
|
Eltérő rendelkezés hiányában az adatok a szabványos állapotú anyagokra vonatkoznak (25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Infobox hivatkozások | |
Lawesson-reagens , vagy LR , egy kémiai vegyület használt szerves szintézis , mint egy tionálási szer. Lawesson reagensét először Sven-Olov Lawesson tette népszerűvé , aki azonban nem találta fel. Lawesson reagensét először 1956 -ban készítették, amikor szisztematikusan tanulmányozták az arénák P 4 S 10 reakcióit .
Készítmény
Lawesson reagens kereskedelmi forgalomban kapható. Azt is meg lehet kényelmesen előállíthatjuk a laboratóriumban keverékét hevítjük anizol a foszfor-pentaszulfiddal , amíg a keverék tiszta és nem több, hidrogén-szulfid keletkezik, majd átkristályosítjuk a toluol vagy a xilol .
A minták részleges hidrolízis miatt erős hidrogén -szulfid szagot adnak. A kellemetlen szagú maradványok elpusztításának egyik gyakori és hatékony módja a felesleges nátrium -hipoklorit ( klórfehérítő ) használata.
A cselekvés mechanizmusa
Lawesson reagensének négytagú gyűrűje kén- és foszforatomok váltakozása . A központi foszfor/kén négytagú gyűrű disszociál, és két reaktív ditiofoszfin- ilidet (R-PS 2 ) képez . Lawessons reagensének kémiájának nagy része valójában ennek a reaktív köztiterméknek a kémiája.
Általában minél több elektronban gazdag egy karbonil, annál gyorsabban alakul át a karbonilcsoport a megfelelő tiokarbonil -csoportba Lawesson reagensével.
Alkalmazások
Lawesson reagensének és rokon anyagainak kémiáját többször áttekintették. Lawesson reagensének fő felhasználási területe a karbonilvegyületek tionálása. Például Lawesson reagensével a karbonil -csoport tiokarbonil -csoporttá alakul . Továbbá, Lawesson-reagenst használunk, a thionate enonok , észterek , laktonok , amidok , laktámok , és kinonok .
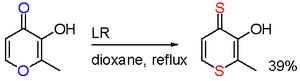
Egy vizsgálatban a maltol és az LR reakciója két pozícióban szelektív oxigénpótlást eredményez.
Kombinációja ezüst-perklorát , és Lawesson-reagens képes működni, mint egy oxofil Lewis-sav , amely képes katalizálni a Diels-Alder reakció az diének a α, β-telítetlen aldehidek .
bizonyos esetekben az alkoholok Lawesson -reagenssel végzett kezeléssel tiolokká alakulhatnak át.
Lawesson reagense szulfoxidokkal reagálva tioétereket képez.
Lásd még
Hivatkozások
Külső linkek
- "Lawesson reagens" . Szerves kémia portál . Letöltve: 2007-10-16 .