Luciferáz - Luciferase
| Bakteriális Luciferáz monooxigenáz család | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Azonosítók | |||||||||||
| Szimbólum | Bac_luciferáz | ||||||||||
| Pfam | PF00296 | ||||||||||
| InterPro | IPR016048 | ||||||||||
| PROSITE | PDOC00397 | ||||||||||
| SCOP2 | 1nfp / SCOPe / SUPFAM | ||||||||||
| |||||||||||
| Dinoflagellate Luciferáz katalitikus domén | |||||||||
|---|---|---|---|---|---|---|---|---|---|
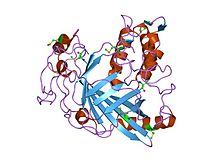 a Lingulodinium polyedrum dinoflagellate luciferáz domén kristályszerkezete
| |||||||||
| Azonosítók | |||||||||
| Szimbólum | Luciferase_cat | ||||||||
| Pfam | PF10285 | ||||||||
| InterPro | IPR018804 | ||||||||
| |||||||||
| Dinoflagellate Luciferáz/LBP N-terminális domén | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Azonosítók | |||||||||
| Szimbólum | Luciferáz_N | ||||||||
| Pfam | PF05295 | ||||||||
| InterPro | IPR007959 | ||||||||
| |||||||||
| Dinoflagellate Luciferáz spirális köteg tartomány | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Azonosítók | |||||||||
| Szimbólum | Luciferáz_3H | ||||||||
| Pfam | PF10284 | ||||||||
| InterPro | IPR018475 | ||||||||
| |||||||||
A luciferáz egy általános kifejezés a biolumineszcenciát előállító oxidatív enzimek osztályára , és általában megkülönböztetik a fotoproteintől . A nevet először Raphaël Dubois használta, aki feltalálta a luciferin és a luciferáz szavakat az és az enzimre . Mindkét szó a latin lucifer szóból származik , jelentése "fényhordozó", ami viszont a "fény" ( lux) és a "hozni vagy hordozni" ( ferre) latin szavakból származik .
| Firefly luciferáz | |||||||
|---|---|---|---|---|---|---|---|
 A Photinus pyralis szentjánosbogár luciferáz szerkezete.
| |||||||
| Azonosítók | |||||||
| Szervezet | |||||||
| Szimbólum | Firefly luciferáz | ||||||
| EKT | 1LCI További struktúrák | ||||||
| UniProt | P08659 | ||||||
| Egyéb adatok | |||||||
| EK -szám | 1.13.12.7 | ||||||
| |||||||
A luciferázokat széles körben használják a biotechnológiában , mikroszkópiában és riportergénekként , sok olyan alkalmazásban, mint a fluoreszkáló fehérjék . A fluoreszcens fehérjékkel ellentétben azonban a luciferázok nem igényelnek külső fényforrást , de szükségük van luciferin , a fogyasztható szubsztrát hozzáadására .
Példák
Különféle élőlények szabályozzák fénytermelésüket különböző luciferázok felhasználásával, különböző fénykibocsátó reakciók során. A vizsgált luciferázok többségét állatokban találták, beleértve a szentjánosbogarakat , és sok tengeri állatot, például a lábaslábúakat , a medúzákat és a tengeri árvácskákat . A luciferázokat azonban fényes gombákban, például a Jack-O-Lantern gombában , valamint más királyságokban, például fénylő baktériumokban és dinoflagellátumokban is tanulmányozták .
Firefly és kattintson bogár
A szentjánosbogarak luciferázai - amelyeknek több mint 2000 faja van - és a többi Elateroidea (kattintóbogár és általában rokonai) luciferázai elég sokfélék ahhoz, hogy hasznosak legyenek a molekuláris filogenézisben . A szentjánosbogaraknál a szükséges oxigént a hasban lévő csövön keresztül, a hasi légcsőbe juttatják . Az egyik jól tanulmányozott luciferáz a Photinini szentjánosbogár Photinus pyralis , amelynek optimális pH-ja 7,8.
Tengeri árvácska
Szintén jól tanulmányozott a tengeri árvácska , a Renilla reniformis . Ebben a szervezetben a luciferáz ( Renilla-luciferin 2-monooxigenáz ) szoros kapcsolatban áll egy luciferin-kötő fehérjével, valamint egy zöld fluoreszkáló fehérjével ( GFP ). A kalcium kiváltja a luciferin ( koelenterazin ) felszabadulását a luciferin -kötő fehérjéből. A szubsztrát ezután rendelkezésre áll a luciferáz általi oxidációhoz , ahol kolenteramiddá bomlik le, és ennek következtében energia szabadul fel. GFP hiányában ez az energia kék fény fotonjaként szabadul fel (csúcs emissziós hullámhossz 482 nm). Azonban, mivel a szorosan kapcsolódó GFP, a felszabaduló energia a luciferázt az helyett keresztül csatlakozik rezonancia energia transzfer a fluorofor a GFP, és ezt követően megjelent egy foton a zöld fény (csúcs-emissziós hullámhossz 510 nm). A katalizált reakció a következő:
- koelenterazin + O 2 → koelenteramid + CO 2 + fényfoton
Copepod
Újabb luciferázokat azonosítottak a közelmúltban, amelyek más luciferázokkal ellentétben természetesen kiválasztott molekulák. Ilyen például a Metridia coelenterazine -függő luciferáz (MetLuc, A0A1L6CBM1 ), amely a tengeri coppodból, a Metridia longa -ból származik . A Metridia longa szekretált luciferáz gén 24 kDa fehérjét kódol, amely 17 aminosavból álló N-terminális szekréciós szignálpeptidet tartalmaz. Ennek a luciferáz molekulának az érzékenysége és a magas jelintenzitása számos újságírói vizsgálatban előnyösnek bizonyul. A MetLuc-hoz hasonló szekretált riportermolekula használatának néhány előnye a lízismentes protokoll, amely lehetővé teszi, hogy élő sejtvizsgálatokat és több vizsgálatot végezzen ugyanazon a sejten.
Bakteriális
A bakteriális biolumineszcencia látható a Photobacterium fajokban, a Vibrio fischeri , a Vibrio haweyi és a Vibrio harveyi fajokban . Fényemisszió néhány biolumineszcens baktériumokban hasznosítja „antennát”, mint például a lumazin fehérjét, hogy elfogadja az energiát a primer gerjesztett állapot a luciferáz, így egy gerjesztett lulnazine kromofort , amely fényt bocsát ki, amely a rövidebb hullámhosszúságú (több kék), míg mások használjon sárga fluoreszkáló fehérjét (YFP), kromofórként FMN-t, és vörös fényt bocsát ki a luciferázhoz képest.
Dinoflagellate
Páncélos ostorosok luciferáz egy multi- domént eukarióta fehérje, amely egy N-terminális domént, és a három katalitikus domének , amelyek mindegyike megelőz egy helikális köteg domént. A szerkezet a páncélos ostorosok luciferáz katalitikus domént lett megoldva. A domén központi része egy 10 szálú béta hordó , amely szerkezetileg hasonló a lipokalinokhoz és az FABP -hez . Az N-terminális domén konzerválódott a dinoflagellate luciferáz és a luciferin- kötő fehérjék (LBP-k) között. Felmerült, hogy ez a régió közvetítheti az LBP és a luciferáz közötti kölcsönhatást, vagy azoknak a vakuoláris membránhoz való kapcsolódását . A spirális köteg domén három hélix kötegszerkezettel rendelkezik , amely négy fontos hisztidint tartalmaz , amelyekről úgy gondolják, hogy szerepet játszanak az enzim pH -szabályozásában . A dinoflagellate luciferáz β-hordójában egy nagy zseb található 8 pH-n, hogy elférjen a tetrapirrol szubsztrát, de nincs olyan nyílás, amely lehetővé teszi a szubsztrát bejutását. Ezért jelentős konformációs változásnak kell bekövetkeznie, hogy hozzáférést és teret biztosítson a ligandumnak az aktív helyen, és ennek a változásnak a forrása a négy N-terminális hisztidin-maradék. 8 pH -n látható, hogy a nem protonált hisztidin -maradékok hidrogénkötések hálózatában vesznek részt a kötegben lévő hélixek határfelületén, amelyek blokkolják a szubsztrát hozzáférését az aktív helyhez, és ezt a kölcsönhatást protonálással megzavarják (pH 6,3). vagy a hisztidin -maradékok alaninnal történő helyettesítése a köteg nagy molekuláris mozgását okozza, amely 11Å -el választja el a hélixeket és megnyitja a katalitikus helyet. Logikailag a hisztidin -maradékokat nem lehet alaninnal helyettesíteni a természetben, de ez a kísérleti helyettesítés tovább erősíti, hogy a nagyobb hisztidin -maradékok blokkolják az aktív helyet. Ezenkívül három Gly-Gly szekvencia, az egyik az N-terminális hélixben és kettő a hélix-hurok-hélix motívumban, csuklópántként szolgálhat, amely körül a láncok forognak, hogy tovább nyissák a katalitikus helyhez vezető utat és növeljék az aktív webhely.
A dinoflagellate luciferáz képes fényt kibocsátani, mivel kölcsönhatásba lép a szubsztrátumával ( luciferin ) és a luciferin-kötő fehérjével (LBP) a dinoflagellates-ben található scintillon organellában . A luciferáz a luciferin és az LBP szerint működik, hogy fényt bocsásson ki, de mindegyik komponens más pH -n működik. A luciferáz és doménjei nem aktívak 8 -as pH -n, de rendkívül aktívak az optimális 6,3 -as pH -n, míg az LBP 8 -as pH -n megköti a luciferint, és 6,3 -on szabadítja fel. Következésképpen a luciferin csak akkor szabadul fel, hogy reagáljon egy aktív luciferázzal, ha a szcintillont 6,3 pH -ra savanyítják. Ezért, annak érdekében, hogy csökkentse a pH, feszültségfüggő csatornákon a scintillon membrán nyílnak, hogy lehetővé tegye a belépését protonok egy vakuólumba rendelkező egy akciós potenciál előállított mechanikai stimuláció. Ezért látható, hogy a vakuoláris membránban fellépő akciópotenciál savasodáshoz vezet, és ez lehetővé teszi a luciferin felszabadulását, hogy reagáljon a luciferázzal a szcintillonban, és kék fényt villan fel.
A reakció mechanizmusa
Valamennyi luciferáz oxidoreduktáz ( EC 1.13.12.- ), azaz egyetlen donorra hat , molekuláris oxigénnel. Mivel a luciferázok sokféle , egymástól független fehérjecsaládból származnak, nincs egységesítő mechanizmus, mivel bármely mechanizmus a luciferáz és a luciferin kombinációjától függ. Mindazonáltal az összes jellemzett luciferáz-luciferin reakcióról kimutatták, hogy bizonyos szakaszokban molekuláris oxigénre van szükség .
Bakteriális luciferáz
A bakteriális luciferáz által katalizált reakció szintén oxidatív folyamat:
- FMNH 2 + O 2 + RCHO → FMN + RCOOH + H 2 O + fény
A reakció során a molekuláris oxigén oxidálja a flavin-mononukleotidot és egy hosszú láncú alifás aldehidet alifás karbonsavvá . A reakció gerjesztett hidroxiflavin köztiterméket képez, amelyet az FMN termékké dehidratálva kék-zöld fényt bocsát ki.
A reakcióba bevitt energia majdnem minden energiája fénysé alakul. A reakció hatékonysága 80-90%. Összehasonlításképpen, az izzólámpa csak energiájának körülbelül 10% -át alakítja át fényké, a 150 lumen/Watt (lm/W) LED pedig a bemenő energia 20% -át látható fénysé.
Alkalmazások
A luciferázok számos célból előállíthatók a laboratóriumban géntechnológiával . A luciferáz gének szintetizálhatók és beilleszthetők a szervezetekbe, vagy transzfektálhatók a sejtekbe. 2002 -től az egerek , a selyemhernyók és a burgonya csak néhány azon organizmusok közül, amelyeket már kifejlesztettek a fehérje előállítására.
A luciferáz reakció során fény sugárzik, amikor a luciferáz a megfelelő luciferin szubsztrátra hat . A fotonkibocsátást fényérzékeny készülékekkel, például luminométerrel vagy módosított optikai mikroszkópokkal lehet kimutatni . Ez lehetővé teszi a biológiai folyamatok megfigyelését. Mivel a luciferáz biolumineszcenciához nincs szükség fénygerjesztésre, minimális az autofluoreszcencia, és ezáltal gyakorlatilag háttérmentes fluoreszcencia. Ezért akár 0,02 pg is pontosan mérhető egy szokásos szcintillációs számlálóval .
A biológiai kutatások során a luciferázt általában riporterként használják fel azoknak a sejteknek a transzkripciós aktivitásának felmérésére , amelyeket luciferáz gént tartalmazó genetikai konstrukcióval transzfektálnak, egy érdeklődő promoter irányítása alatt . Ezenkívül prolumineszcens molekulák, amelyek egy adott enzim aktivitása után luciferinné alakulnak, felhasználhatók az enzimaktivitás kimutatására kapcsolt vagy kétlépéses luciferáz vizsgálatokban. Ilyen szubsztrátokat használtak többek között a kaszpázaktivitás és a citokróm P450 aktivitás kimutatására .
A luciferáz a sejt ATP szintjének kimutatására is használható a sejtek életképességének vizsgálatában vagy a kináz aktivitás vizsgálatában. A luciferáz biotinilezés révén ATP -érzékelő fehérjeként működhet . Biotinilezése fog immobilizáljuk luciferáz a sejt-felületen történő kötődés révén egy sztreptavidin - biotin komplex. Ez lehetővé teszi a luciferáz számára, hogy érzékelje az ATP kiáramlását a sejtből, és hatékonyan megjeleníti az ATP valós idejű felszabadulását biolumineszcencián keresztül. A luciferáz ezenkívül tenni érzékenyebb az ATP kimutatási növelésével lumineszcenciaintenzitás megváltoztatásával bizonyos aminosav- maradékok a fehérje szekvenciáját.
Egész állat képalkotó (a továbbiakban in vivo , amikor élő vagy, más néven ex vivo képalkotás) egy erős technika tanulmányozására sejtpopulációk az élő állatok, mint például egerek. Különböző típusú sejtek (pl. Csontvelő őssejtek, T-sejtek) tervezhetők luciferáz expressziójához, amely lehetővé teszi azok nem invazív megjelenítését élő állatokon belül egy érzékeny töltéspárosító kamerával ( CCD kamera ). Ezt a technikát alkalmazták állatmodellekben követni a tumor kialakulását és a daganatok kezelésre adott válaszát. A környezeti tényezők és a terápiás interferenciák azonban bizonyos eltéréseket okozhatnak a daganatterhelés és a biolumineszcencia intenzitása között a proliferációs aktivitás változásaihoz képest. Az in vivo képalkotással mért jel intenzitása számos tényezőtől függhet, mint például a D-luciferin felszívódása a hashártyán, a véráramlás, a sejtmembrán permeabilitása, a társfaktorok elérhetősége, az intracelluláris pH és a fedő szövet átlátszósága. a luciferáz mennyisége.
A luciferáz egy hőérzékeny fehérje, amelyet a fehérjék denaturálásával kapcsolatos vizsgálatokban használnak, a hősokk fehérjék védő képességének tesztelésére . A luciferáz alkalmazásának lehetőségei tovább bővülnek.
Lásd még
Hivatkozások
Külső linkek
-
 Luciferase -hoz kapcsolódó média a Wikimedia Commons -ban
Luciferase -hoz kapcsolódó média a Wikimedia Commons -ban - Az előzetes tervezetben rendelkezésre álló strukturális információk áttekintése az UniProt : P08659 (Luciferin 4- monooxygenase ) PDBe-KB-ban .
- Trimmer B, Zayas R, Qazi S, Lewis S, Michel T, Dudzinski D, Aprille J, Lagace C (2001-06-28). "Firefly villan és nitrogén -oxid" . Tufts Egyetem . Letöltve: 2008-10-02 .
- "A riportergének fejlődésének tendenciái" . reportergene.com . Letöltve: 2009-03-07 .
- "BL Web: Luciferin típusok" . A Biolumineszcens weboldal . Kaliforniai Egyetem, Santa Barbara . Letöltve: 2009-03-07 .
- "Biolumineszcens riporter protokollok és alkalmazások útmutatója" . Protokollok és alkalmazások . Promega Corporation. Archiválva az eredetiből 2010-08-08 . Letöltve: 2009-03-07 .
- "BL Web: Luciferin típusok" . ISCID Tudomány és Filozófia Enciklopédia . ISCID. Archiválva az eredetiből 2012-09-21 . Letöltve: 2010-04-20 .
- Goodsell D. "Luciferáz" . A hónap molekulája . Fehérje Adatbank . Letöltve: 2013-01-15 .
