Rimonabant - Rimonabant
 | |
 | |
| Klinikai adatok | |
|---|---|
| AHFS / Drugs.com | Fogyasztói gyógyszerekkel kapcsolatos információk |
| Licenc adatok | |
| Terhességi kategória |
|
| Utak ügyintézés |
Orális |
| ATC kód | |
| Jogi státusz | |
| Jogi státusz | |
| Farmakokinetikai adatok | |
| Biológiai hozzáférhetőség | Meghatározatlan |
| Fehérjekötés | Közel 100% |
| Anyagcsere | Máj , CYP3A4 érintett |
| Felszámolási felezési idő | Változó: 6–9 nap normál BMI-vel 16 nap, ha a BMI> 30 |
| Kiválasztás | Széklet (86%) és vese (3%) |
| Azonosítók | |
| |
| CAS szám | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| CompTox műszerfal ( EPA ) | |
| ECHA információs kártya |
100.210.978 |
| Kémiai és fizikai adatok | |
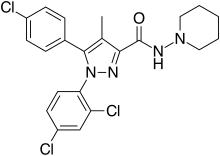
| Képlet | C 22 H 21 Cl 3 N 4 O |
| Moláris tömeg | 463,79 g · mol −1 |
| 3D modell ( JSmol ) | |
| |
| |
| (ellenőrizni) | |
A Rimonabant (más néven SR141716 ; kereskedelmi nevek Acomplia , Zimulti ) anorektikus elhízás elleni gyógyszer , amelyet először 2006-ban hagytak jóvá Európában, de 2008-ban világszerte visszavonták súlyos pszichiátriai mellékhatások miatt; soha nem hagyták jóvá az Egyesült Államokban. A rimonabant a CB 1 kannabinoid receptor inverz agonistája , és ez volt az első jóváhagyott gyógyszer ebben az osztályban.
Történelem
A rimonabant egy szelektív CB 1 receptor blokkoló , amelyet a Sanofi-Aventis fedezett fel és fejlesztett ki ;
2006. június 21-én az Európai Bizottság jóváhagyta a rimonabant eladását az akkor 25 tagú Európai Unióban vényköteles gyógyszerként, diétával és testmozgással együtt alkalmazva 30 kg / m testtömeg-indexnél (BMI) nagyobb betegek esetén. 2 vagy 27 kg / m 2- nél nagyobb BMI-vel rendelkező betegek kapcsolódó kockázati tényezőkkel, például 2- es típusú cukorbetegséggel vagy diszlipidémiával . Osztályában elsőként hagyták jóvá bárhol a világon.
A rimonabantot 2005-ben benyújtották jóváhagyásra az Élelmiszer- és Gyógyszerügyi Hivatalhoz (FDA) az Egyesült Államokban; 2007-ben az FDA endokrin és anyagcsere-gyógyszerekkel foglalkozó tanácsadó bizottsága (EMDAC) arra a következtetésre jutott, hogy a Sanofi-Aventis nem tudta bizonyítani a rimonabant biztonságosságát, és az ellen szavazott, hogy jóváhagyásra javasolja az elhízás elleni kezelést, és két héttel később a vállalat visszavonta a kérelmet.
A gyógyszert 2007 áprilisában hagyták jóvá Brazíliában.
2008 októberében az Európai Gyógyszerügynökség javasolta az Acomplia felfüggesztését, miután az emberi felhasználásra szánt gyógyszerek bizottsága (CHMP) megállapította, hogy az Acomplia kockázatai meghaladják annak előnyeit a súlyos pszichiátriai problémák, köztük az öngyilkosság kockázata miatt. 2008 novemberében egy brazíliai tanácsadó bizottság szintén felfüggesztést javasolt, és abban a hónapban a Sanofi-Aventis felfüggesztette a gyógyszer értékesítését világszerte. Az EMA jóváhagyását 2009 januárjában visszavonták. 2009-ben India megtiltotta a gyógyszer gyártását és értékesítését.
Káros hatások
A szabályozó hatóságoknak benyújtott klinikai vizsgálatok adatai azt mutatták, hogy a rimonabant depressziós rendellenességeket vagy hangulatváltozásokat okozott az alanyok legfeljebb 10% -ában és öngyilkossági gondolatokat körülbelül 1% -ban, Európában pedig ellenjavallt bármilyen pszichiátriai rendellenességben szenvedő emberek számára, beleértve a depressziós vagy öngyilkosokat is. .
Ezenkívül az émelygés és a felső légúti fertőzések nagyon gyakori káros hatások voltak (az emberek több mint 10% -ánál fordultak elő); gyakori mellékhatások (az emberek 1-10% -a között fordulnak elő): gastroenteritis , szorongás, ingerlékenység, álmatlanság és egyéb alvászavarok, hőhullámok, hasmenés, hányás, száraz vagy viszkető bőr, íngyulladás, izomgörcsök és görcsök, fáradtság, influenza -szerű tünetek és fokozott esésveszély.
Az FDA tanácsadó bizottsága aggályokat vetett fel azzal kapcsolatban, hogy az állatokra vonatkozó adatok alapján úgy tűnt, hogy a központi idegrendszeri toxicitás és konkrétan a rohamok tekintetében a terápiás ablak szinte nem létezik; a terápiás dózis és az állatoknál rohamokat okozó dózis azonosnak tűnt.
Amikor az EMA áttekintette a forgalomba hozatalt követő megfigyelési adatokat, azt találta, hogy a rimonabantot szedő betegeknél megduplázódott a pszichiátriai rendellenességek kockázata.
Kémia
A rimonabant kémiai szintézisét a következőképpen írják le:
Kutatás
Az elhízással kapcsolatos klinikai vizsgálatok mellett, amelyek a szabályozó hatóságokhoz benyújtott adatokat állították elő, a rimonabantot klinikai vizsgálatokban is tanulmányozták más betegségek lehetséges kezelésére, beleértve a cukorbetegséget, az érelmeszesedést és a dohányzásról való leszokást.

