Cink-cianid - Zinc cyanide
|
|
| Azonosítók | |
|---|---|
|
3D modell ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.008.331 |
|
PubChem CID
|
|
| RTECS szám | |
| UNII | |
|
CompTox műszerfal ( EPA )
|
|
|
|
|
|
| Tulajdonságok | |
| Zn (CN) 2 | |
| Moláris tömeg | 117,444 g / mol |
| Megjelenés | fehér szilárd anyag |
| Sűrűség | 1.852 g / cm 3 , szilárd |
| Olvadáspont | 800 ° C (1470 ° F; 1070 K) (bomlik) |
| 0,00005 g / 100 ml (20 ° C) | |
| Oldékonyság | lúgok , KCN , ammónia támadja meg |
| −46,0 · 10 −6 cm 3 / mol | |
| Veszélyek | |
|
EU besorolás (DSD) (elavult)
|
nem felsorolt |
| NFPA 704 (tűz gyémánt) | |
| Halálos dózis vagy koncentráció (LD, LC): | |
|
LD 50 ( medián dózis )
|
100 mg / kg, patkány (intraperitoneális) |
|
Hacsak másképp nem jelezzük, az adatokat a normál állapotú anyagokra vonatkozóan adjuk meg (25 ° C-on (100 kPa). |
|
|
|
|
| Infobox hivatkozások | |
A cink-cianid a Zn ( CN ) 2 képletű szervetlen vegyület . Ez egy fehér szilárd anyag, amelyet főleg cink galvanizálására használnak, de emellett a szerves vegyületek szintézisének speciálisabb alkalmazásai is vannak .
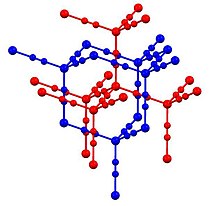
Szerkezet
A Zn (CN) 2- ben a cink átveszi a tetraéderes koordinációs környezetet, mindezt összekapcsolják áthidaló cianid ligandumok . A szerkezet két "áthatoló" struktúrából áll (kék és piros a fenti képen). Az ilyen motívumokat néha "kiterjesztett diamondoid " szerkezeteknek nevezik . A SiO 2 egyes formái hasonló szerkezetet képviselnek, ahol a tetraéderes Si központokat oxidok kötik össze. A cianidcsoport fej-farok rendellenességet mutat minden olyan cinkatomnál, amelynek egy-négy szénszomszédja van, a fennmaradó pedig nitrogénatom. Az egyik legnagyobb negatív hőtágulási együtthatót mutatja (meghaladja az előző rekordot, a cirkónium-volframátot ).
Kémiai tulajdonságok
Szervetlen polimer esetében a Zn (CN) 2 oldhatatlan a legtöbb oldószerben. A szilárd anyag feloldódik vagy pontosabban lebontja bázikus ligandumok, például hidroxid , ammónia és további cianid vizes oldatában, anionos komplexeket kapva.
Szintézis
A Zn (CN) 2 könnyen elkészíthető a cianid és a cinkionok vizes oldatainak kombinálásával, például a KCN és a ZnSO 4 közötti kettős helyettesítési reakció útján :
- ZnSO 4 + 2 KCN → Zn (CN) 2 + K 2 SO 4
Kereskedelmi alkalmazásokban bizonyos erőfeszítéseket tesznek a halogenid- szennyeződések elkerülésére a cink- acetát- sók alkalmazásával:
- Zn (CH 3 COO) 2 + HCN → Zn (CN) 2 + 2 CH 3 COOH
A cink-cianidot bizonyos aranykivonási módszerek melléktermékeként is előállítják . Az arany és a vizes arany-cianid elkülönítésére szolgáló eljárások néha cink hozzáadását teszik szükségessé:
- 2 [Au (CN) 2 ] - + Zn → 2 Au + Zn (CN) 2 + 2 CN -
Alkalmazások
Galvanizálás
A Zn (CN) 2 fő alkalmazása a cink galvanizálása további cianidot tartalmazó vizes oldatokból.
Szerves szintézis
Zn (CN) 2 bevitelére alkalmazunk, a formilcsoport csoport, hogy az aromás vegyületek a Gatterman reakciót , ahol szolgál kényelmes, biztonságosabb, és nem gáznemű alternatívája HCN . Mivel a reakció használ HCI , Zn (CN) 2 is ellátja a reakciót in situ a ZnCl 2 , egy Lewis-sav katalizátor . Az ilyen módon alkalmazott Zn (CN) 2 példák közé tartozik a 2-hidroxi-1-naftaldehid és a mezitaldehid szintézise.
Zn (CN) 2 katalizátorként is alkalmazható az aldehidek és ketonok ciano-szililezéséhez.
Hivatkozások

