Magnézit - Magnesite
| Magnezit | |
|---|---|
 Brazíliai magnezit kristályok (11,4 x 9,2 x 3,6 cm)
| |
| Tábornok | |
| Kategória | Karbonát ásvány |
|
Képlet (ismétlődő egység) |
MgCO 3 |
| Strunz osztályozás | 5.AB.05 |
| Kristály rendszer | Trigonális |
| Kristály osztály | Hatszögletű scalenohedral ( 3 m) HM szimbólum : ( 3 2/m) |
| Űrcsoport | R 3 c |
| Azonosítás | |
| Szín | Színtelen, fehér, halványsárga, halványbarna, halvány rózsaszín, lila-rózsa |
| Kristály szokás | Általában masszív, ritkán romboéder vagy hatszögletű prizma |
| Hasítás | [10 1 1] tökéletes |
| Törés | Conchoidal |
| Kitartás | Törékeny |
| Mohs -skála keménysége | 3,5 - 4,5 |
| Ragyogás | Üvegszerű |
| Csík | fehér |
| Diaphaneity | Átlátszó -áttetsző |
| Fajsúly | 3.0 - 3.2 |
| Optikai tulajdonságok | Egytengelyű (-) |
| Törésmutató | n ω = 1,508 - 1,510 n ε = 1,700 |
| Kettős törés | 0,191 |
| Olvadékonyság | beönthetetlen |
| Oldhatóság | Forró HCl -ben pezsgő |
| Egyéb jellemzők | Halványzöldtől halványkék fluoreszcenciáig és foszforeszcenciához vezethet UV fényben; tribolumineszcens |
| Hivatkozások | |
Magnesite egy ásványi a kémiai képlete Mg C O
3( magnézium -karbonát ). Vas , mangán , kobalt és nikkel adalékanyagként fordulhat elő, de csak kis mennyiségben.
Esemény
A magnézit vénaként és ultramafikus kőzetek , szerpentinit és más magnéziumban gazdag kőzettípusok változásának termékeiként fordul elő mind érintkező, mind regionális metamorf terepen. Ezek a magnézitek gyakran kripto -kristályosak, és szilícium -dioxidot tartalmaznak opál vagy chert formájában .
Magnesite is jelen van a regolith fenti ultrabázisos kőzetek, mint másodlagos karbonát belül a talaj és az altalaj , ahol lerakódik következtében oldódási magnézium-csapágy ásványok szén-dioxid felszín alatti vizekben.
Izotópszerkezet: csomós izotóp
A közelmúltban elért fejlődés a stabil izotóp -geokémia területén az ásványok és molekulák izotópszerkezetének tanulmányozása. Ez megköveteli a nagy felbontású molekulák tanulmányozását a kötési forgatókönyv alapján (hogyan kötődnek egymáshoz a nehéz izotópok)- ami a molekula izotópszerkezetétől függően stabilitásának ismeretéhez vezet.
Az oxigénnek három stabil izotópja van ( 16 O, 17 O és 18 O), a szénnek kettő ( 13 C, 12 C). Egy 12 C 16 O 2 molekulát (amely csak az alkotóelemek leggyakoribb izotópjaiból áll) monoizotóp fajnak nevezik . Ha csak egy atomot helyettesítenek bármely alkotóelem nehéz izotópjával (pl. 13 C 16 O 2 ), akkor azt „egyszer szubsztituált” fajnak nevezik. Hasonlóképpen, ha két atomot egyszerre helyettesítenek nehezebb izotópokkal (pl. 13 C 16 O 18 O), akkor ezt „kétszer helyettesített” fajnak nevezzük. A „halmozott” faj ( 13 C 16 O 18 O) a CO 2 számára kétszeresen helyettesített CO 2 molekula. Az izotóppal helyettesített molekulák tömege nagyobb. Ennek következtében a molekuláris rezgés csökken, és a molekula alacsonyabb nullapont energiát fejleszt ki (lásd Kinetikus izotóp hatás ).
A bizonyos kötések sokasága bizonyos molekulákban érzékeny a hőmérsékletre, amelyen létrejött (pl. 13 C 16 O 18 O karbonátokban , 13 C- 18 O kötésként való jelenléte ). Ezt az információt felhasználták a csomós izotóp -geokémia megalapozásához . Összecsomósodott izotóp hőmérőket hoztak létre olyan karbonát ásványokra, mint a dolomit , kalcit , sziderit stb., És a nem karbonátos vegyületekre, mint a metán és az oxigén . A kation-karbonát-oxigén (azaz Mg-O, Ca-O) kötések erősségétől függően a különböző karbonát ásványok különbözőképpen alkothatnak vagy őrizhetnek meg halmozott izotóp aláírásokat.
Mérések és jelentések
A csomós izotóp analízisnek bizonyos aspektusai vannak. Ezek:
Emésztés, elemzés és savfrakció korrekció
Összetapadt Izotópelemzésre általában történik gázforrás tömegspektrometriával , ahol a CO 2 felszabadítjuk magnezit foszforsavval emésztéssel táplálják be a izotóparány tömegspektrométer . Ebben az esetben gondoskodni kell arról, hogy a CO 2 magnezitből való felszabadulása teljes legyen. A magnezit emésztése nehéz, mivel hosszú ideig tart, és a különböző laboratóriumok különböző emésztési időket és hőmérsékletet jelentenek (12 órától 100 ° C -on 1 óráig 90 ° C -on foszforsavban ). Ezen a magas hőmérsékleten történő emésztés miatt a felszabadult CO 2 -ban lévő 13 C- 18 O kötés egy része megszakad (ami a „csomósodott” CO 2 mennyiségének csökkenéséhez vezet ) a karbonátok foszforsav-emésztése során. Ennek a kiegészítő (analitikai műterméknek) a figyelembevételéhez a sav -frakcionálási korrekciónak nevezett korrekciót hozzáadjuk az emésztési hőmérsékleten kapott magnezit -csomós izotópértékhez.
Mivel a CO 2 -gáz a savas emésztés során felszabadul a karbonát ásványból, egy O-t hagyva hátra- frakcionálódás következik be, és az elemzett CO 2 -gáz izotóp összetételét korrigálni kell. A magnezit esetében a legmegbízhatóbb frakcionálási tényező ( α) egyenlet a következő:
10 3 ln (α) = [(6,845 ± 0,475) * 10 5 / T 2 ] + (4,22 ± 0,08); T K -ban
Különböző kutatók más frakcionálási tényezőket is alkalmaztak, például a dolomit frakcionálási tényezőt.
Szabványok
Ismeretlen összetételű minták mérésekor bizonyos szabványos anyagokat kell mérni (lásd: Referenciaanyagok a stabil izotóp elemzéshez ). A belső szabványok és referenciaanyagok segítségével az elemzési munkamenetet rendszeresen felügyelik. A standard anyagok főleg kalcit és márvány.
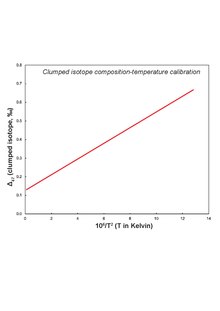
Δ 47 - Hőmérséklet kalibrálása
A halmozott izotópadatok hőmérsékletre konvertálásához kalibrációs görbére van szükség, amely az összetapadt izotópösszetétel hőmérsékletfüggésének funkcionális formáját fejezi ki. A magnézitre nincs ásványspecifikus kalibrálás. Néhány kísérleti adat alapján, ahol az ásványi csapadék hőmérséklete és az összetapadt izotópból származó hőmérséklet nem egyezik, felmerül az ásványspecifikus kalibrálás szükségessége. Az eltérés abból adódik, hogy a magnezitben a kötés eltér a kalcit/dolomittól, és/vagy a savas emésztés magasabb hőmérsékleten történik.
Magnezit -víz és CO 2 -Magnesit -izotóp -frakcionálási tényezők
A csomósított izotópból származó hőmérséklet alkalmazásával a szülőfolyadék C- és O-izotóp-összetétele ismert magnezit-folyadék izotóp-frakcionálási tényezők segítségével számítható ki, mivel a frakcionálás hőmérsékletfüggő. Az irodalomban közölt magnezit-folyadék O és C izotóp frakcionálási tényezők nincsenek összhangban egymással. A frakcionálási viselkedést kísérleti megfigyelések nem támasztották alá.
A magnezit izotópszerkezetét szabályozó tényezők
Átalakítás hidrogén-magnézium-karbonátokból magnézitre
Alacsony hőmérsékleten tehát vizes Mg-karbonátok ( hidromágnesit , nesquehonit stb.) Képződnek . Ezeket a fázisokat magnezitté lehet alakítani a hőmérséklet ásványi oldódással, kicsapással vagy dehidratálással történő megváltoztatásával. Bár ez megtörténik, egy kapcsolódó izotóphatás szabályozhatja a kicsapódott magnezit izotóp -összetételét.
Egyensúlyhiány
Az egyensúlyhiányos folyamatok, mint a gáztalanítás, a gyors CO 2 -felvétel stb., Kifejezetten alacsony hőmérsékleten módosítják a karbonátos ásványok összetapadt izotóp -összetételét. Ezek változóan gazdagítják vagy kimerítik a rendszert a C és O nehéz izotópjaiban. Mivel a csomósodott izotópok száma a C és O izotópok mennyiségétől függ, ezeket is módosítják. Egy másik kiemelkedő hatás itt a kicsapó folyadék pH -ja. Ahogy a kicsapódó folyadék pH -ja változik, a DIC -medence befolyásolódik, és a kicsapódó karbonát izotóp összetétele megváltozik.
Ásványi szerkezet és későbbi hőhatások
A kristályos és kriptokristályos magnezitek ásványi szerkezete nagyon eltérő. Míg a kristályos magnezit jól fejlett kristályszerkezettel rendelkezik, a kriptokristályos magnezit amorf, többnyire finom szemcsék halmaza. Mivel a csomósodott izotóp összetétel a specifikus kötődéstől függ, a kristályszerkezet különbsége nagy valószínűséggel befolyásolja a csomósodott izotóp aláírások rögzítésének módját ezekben a különböző struktúrákban. Ez ahhoz a tényhez vezet, hogy érintetlen aláírásukat másképp módosíthatják a későbbi termikus események, például a diagenezis /temetési fűtés stb.
Képződés
Magnesite lehet kialakítani, a talkum-karbonát metasomatism a peridotit és más ultrabázisos kőzetek. A magnezit az olivin szén és szén -dioxid jelenlétében, szénhidrogén jelenlétében, szénhidrogénnel képződése során keletkezik, a zöldbarát fáciesre jellemző magas hőmérsékleten és magas nyomáson .
Magnesite is képezhetők keresztül szénsavas magnézium szerpentin (lizardit) keresztül a következő reakció :
- 2 Mg 3 Si 2 O 5 (OH) 4 + 3 CO 2 → Mg 3 Si 4 O 10 (OH) 2 + 3 MgCO 3 + 3 H 2 O
Ha azonban ezt a reakciót laboratóriumban végzik, szobahőmérsékleten a magnézium -karbonát (nesquehonite) trihidratált formája képződik. Ez a megfigyelés ahhoz vezetett, hogy egy "dehidratációs gát" feltételezte, hogy részt vesz a vízmentes magnézium-karbonát alacsony hőmérsékletű képződésében. A laboratóriumi kísérletek formamiddal , vízzel hasonlító folyadékkal mutatták ki, hogy ilyen dehidratációs gátat nem lehet bevonni. A vízmentes magnézium-karbonát nukleációjának alapvető nehézsége továbbra is fennáll e nemvizes oldat használatakor. Nem a kationos dehidratáció, hanem inkább a karbonát-anionok térbeli konfigurációja képezi a gátat a magnezit alacsony hőmérsékletű nukleációjában. A magnezit megtalálható a modern üledékekben, barlangokban és talajokban. Alacsony hőmérsékletű (körülbelül 40 ° C [104 ° F]) képződése ismert, hogy váltakozást igényel a csapadék és az oldódási időközök között. A magnezit alacsony hőmérsékletű képződése jelentős lehet a nagyméretű szén - dioxid megkötés szempontjából . Vandeginste nagy lépést tett a magnézit ipari előállítása felé légköri nyomáson és 316 K hőmérsékleten. Ezekben a kísérletekben a sósav kis adagjai rendszeresen váltakoztak nátrium -karbonát -oldat hozzáadásával. Új volt a nagyon rövid, mindössze néhány órás időtartam a váltakozó oldódási és kicsapási ciklusokhoz.
A magnézitet az ALH84001 meteoritban és a Mars bolygón észlelték . A magnézitet a Marson azonosították a műhold pályájáról származó infravörös spektroszkópia segítségével . A Jezero-kráter közelében Mg-karbonátokat észleltek és jelentették, hogy az ott uralkodó tavaszi környezetben képződtek. Továbbra is vita folyik ezen karbonátok keletkezési hőmérsékletéről . Alacsony hőmérsékletű képződést javasoltak a magnezithez a Marsból származó ALH84001 meteoritból.
A magnéziumban gazdag olivin ( forsterit ) elősegíti a magnezit peridotitból történő előállítását. A vasban gazdag olivin ( fayalit ) elősegíti a magnetit- magnézit -szilícium-dioxid kompozíciók előállítását.
Magnesite is képezhetők útján metasomatism a Skarn betétek, a dolomit mészkövek , társított wollastonit , periklász , és a talkum .
A magas hőmérsékletnek ellenálló és a magas nyomást ellenálló magnezit a Föld köpenyének egyik fő karbonáttartó fázisa, és a mély széntartályok lehetséges hordozója. Hasonló okok miatt megtalálható a metamorfizált peridotit kőzetekben a Közép -Alpokban, Svájcban és a nagynyomású eclogitikus kőzetekben a kínai Tianshanból.
A magnezit a tavakban is kicsapódhat baktériumok jelenlétében, akár víztartalmú Mg-karbonátok, akár magnezit formájában.
Az izotópszerkezetből származó információk
A csomósodott izotópokat a magnezitképződés körülményeinek és a kicsapó folyadék izotóp összetételének értelmezésére használták. Belül ultrabázisos komplexek, magnesites találhatók belül vénák és stockworks a kriptokristályos formában, valamint belül szénsavas peridotit egységek kristályos formában. Ezek a kripto -kristályos formák többnyire változóan mállottak, és alacsony képződési hőmérsékletet eredményeznek. Másrészt a durva magneziták nagyon magas hőmérsékletet adnak, ami a hidrotermális eredetre utal . Feltételezések szerint durva, magas hőmérsékletű magnezitek képződnek köpenyből származó folyadékokból, míg a kripto-kristályosak kicsapódnak a keringő meteorikus víz által, amely felveszi a szenet az oldott szervetlen széngyűjtőből, a talajszénből, és befolyásolja az egyensúlytalan izotóphatások.
A tavakban és a playa környezetben képződő mágnesesek általában a C és O nehéz izotópjaiban dúsulnak a párolgás és a CO 2 gáztalanítás miatt. Ez tükrözi, hogy az izotópokból származó halmozott hőmérséklet nagyon alacsony. Ezeket befolyásolja a pH -hatás, a biológiai aktivitás, valamint a gáztalanításhoz kapcsolódó kinetikus izotóphatás. A magnézit felületi öntőformaként alakul ki ilyen körülmények között, de általában víztartalmú Mg-karbonátok formájában fordul elő, mivel kicsapódásuk kinetikailag előnyös. A legtöbb esetben a C -t a DIC -ből vagy a közeli ultramafikus komplexekből származtatják (pl. Altin Playa, Brit Columbia, Kanada).
A metamorf kőzetekben lévő magnézitek viszont nagyon magas képződési hőmérsékletet jeleznek. A szülői folyadék izotóp összetétele szintén nehéz- általában metamorf folyadékok. Ezt a folyadékbevonatból származtatott hőmérséklettel, valamint a hagyományos O-izotóp-hőméréssel, kvarc-magnezit együttes kicsapásával igazolták.
A magnezit gyakran alacsonyabb halmozott izotóphőmérsékletet rögzít, mint a kapcsolódó dolomit, kalcit. Ennek oka az lehet, hogy a kalcit, a dolomit hamarabb keletkezik magasabb hőmérsékleten (köpenyszerű folyadékokból), ami a magnéziit kicsapódásához szükséges mértékben növeli a folyadék Mg/Ca arányát. Ahogy ez az idő előrehaladtával történik, a folyadék lehűl, más folyadékokkal keverve fejlődik, és amikor magnezit képződik, csökkenti a hőmérsékletét. Tehát a kapcsolódó karbonátok jelenléte szabályozza a magnezit izotóp összetételét.
A marsi karbonátok eredete összeomlott izotóp alkalmazásával felbontható. Ezekből a kőzetekből lehetett felmérni a CO 2 forrását, a Mars éghajlati-hidrológiai viszonyait. A legutóbbi tanulmány kimutatta (a csomósodott izotóp -hőmérés végrehajtása ), hogy az ALH84001 -ben található karbonátok jelzik a felszín alatti vízből történő alacsony hőmérsékletű párolgási körülmények között történő képződést és a CO 2 származtatását a marsi légkörből.
Felhasználások
Tűzálló anyag
A mész előállításához hasonlóan a magnézitet szén jelenlétében is el lehet égetni, hogy MgO keletkezzen , amely ásványi anyag formájában perikláz néven ismert . Nagy mennyiségű magnézitet égetnek el, hogy magnézium-oxidot állítsanak elő : ez egy fontos tűzálló (hőálló) anyag, amelyet kohókban , kemencékben és égetőkben bélésként használnak .
A kalcinálási hőmérsékletek határozzák meg a keletkező oxidtermékek reaktivitását, a könnyű égetett és elégett égési osztályok pedig a termék felületére és a kapott reakcióképességre vonatkoznak (ezt jellemzően a jódszám iparági mutatója határozza meg).
A „könnyen égett ” termék általában a 450 ° C -on kezdődő kalcinálást jelenti, amely 900 ° C felső határig halad - ami jó felületet és reakcióképességet eredményez.
900 ° C felett az anyag elveszíti reaktív kristályszerkezetét, és visszatér a kémiailag inert „ holtan égett ” termékhez, amelyet tűzálló anyagokban, például kemencebélésekben használnak.
Szintetikus gumi
A mágnesit padlóburkolatban ( magnézit esztrich ) kötőanyagként is használható . Ezenkívül katalizátorként és töltőanyagként használják szintetikus gumi előállításában, valamint magnézium vegyi anyagok és műtrágyák előállításában.
A tűzvizsgálat során a magnezit kupolák használhatók a kuplézióhoz, mivel a magnezit kupak ellenáll a magas hőmérsékleteknek.
A magnézit vágható, fúrható és polírozható, hogy gyöngyöket képezzen, amelyeket ékszerkészítésben használnak. A magnézitgyöngyök merész színek széles spektrumára festhetők, beleértve a világoskék színt is, amely utánozza a türkiz megjelenését .
Kutatások folynak annak érdekében, hogy értékeljék az üvegházhatású gázok szén -dioxidjának magnézitben történő nagy mennyiségű megkötésének célszerűségét . Ez összpontosított peridotitok származó ofiolit összlet (obducted köpeny kőzetek kéreg), ahol magnezit hozható létre azáltal, hogy a szén-dioxid reagál ezeket a köveket. Némi előrelépés történt az Ománi opiolitok terén. A fő probléma azonban az, hogy ezek a mesterséges eljárások elegendő porozitás-áteresztőképességet igényelnek ahhoz, hogy a folyadékok áramolhassanak, de ez peridotiták esetében aligha fordul elő .
Munkahelyi biztonság és egészségvédelem
Az embereket belélegezve, bőrrel és szemmel érintkezve ki lehet téve a munkahelyi magnezitnek.
Egyesült Államok
A Munkahelyi Biztonsági és Egészségügyi Hatóság (OSHA) a munkahelyi magnezit-expozíció törvényi határértékét ( megengedett expozíciós határértékét ) 15 mg/m 3 teljes expozíciónak és 5 mg/m 3 légúti expozíciónak határozta meg egy 8 órás munkanapon. Az Országos Munkavédelmi és Egészségügyi Intézet (NIOSH) egy 8 órás munkanapon 10 mg/m 3 és 5 mg/m 3 légúti expozíció javasolt expozíciós határértékét (REL) határozta meg.
Hivatkozások
- Smithsonian Rock and Gem ISBN 0-7566-0962-3