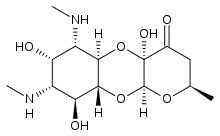
Spektinomicin - Spectinomycin
 | |
| Klinikai adatok | |
|---|---|
| Kereskedelmi nevek | Trobicin |
| Más nevek | (2 R , 4a R , 5a R , 6 S , 7 S , 8 R , 9 S , 9a R , 10a S ) -4a, 7,9-trihidroxi-2-metil-6,8- bisz (metil-amino) dekahidro -4 H -pirano [2,3- b ] [1,4] benzo-dioxin-4-on |
| AHFS / Drugs.com | Monográfia |
| Az adminisztráció módjai |
IM |
| ATC kód | |
| Jogi státusz | |
| Jogi státusz | |
| Azonosítók | |
| |
| CAS -szám | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| CHEMBL | |
| CompTox műszerfal ( EPA ) | |
| ECHA InfoCard |
100.015.374 |
| Kémiai és fizikai adatok | |
| Képlet | C 14 H 24 N 2 O 7 |
| Moláris tömeg | 332,353 g · mol −1 |
| 3D modell ( JSmol ) | |
| Olvadáspont | 184–194 ° C (363–381 ° F) |
| |
| |
|
| |
A spektinomicin , amelyet többek között Trobicin márkanéven árusítanak , antibiotikum a gonorrhoea fertőzések kezelésére . Az injekciót izomba adják.
Gyakori mellékhatások: fájdalom az injekció beadásának helyén, kiütés, hányinger, láz és alvászavar. Időnként súlyos allergiás reakciók léphetnek fel. Terhesség alatt általában biztonságos a használata. A penicillinre vagy a cefalosporinokra allergiás betegek használhatják . A gyógyszer az aminociklitolok osztályába tartozik, és bizonyos baktériumok által leállítja a fehérjék termelését.
A spektinomicint 1961 -ben fedezték fel. Az Egészségügyi Világszervezet alapvető gyógyszerek listáján szerepel . Az Egyesült Államokban nem áll rendelkezésre emberi felhasználásra. A Streptomyces spectabilis baktériumból készül .
Orvosi felhasználás
Ez adott intramuszkuláris injekció kezelésére gonorrhoea , különösen azokban a betegekben, akik allergiás a penicillinek .
Ez az antibiotikum az Egyesült Államokban már nem áll rendelkezésre emberi felhasználásra, de továbbra is elérhető állatgyógyászati használatra.
Mellékhatások
A mellékhatások közé tartozik a viszketés , hidegrázás , gyomorfájdalom és vörös kiütés .
A cselekvés mechanizmusa
A spektinomicin kötődik a bakteriális riboszóma 30S alegységéhez, és megszakítja a fehérjeszintézist. A Pasteurella multocida 16S riboszómális RNS -ben a rezisztencia egyik formája alakult ki .
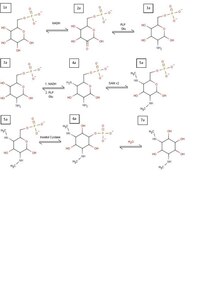
Bioszintetikus mechanizmus
A spektinomicin bioszintézise minden aminoglikozidhoz hasonlóan kezdődik, inozitolgyűrű képződésével . A különbség a kezdeti módosítás, amely a spektinomicin inozitgyűrűjét képezi. A folyamat glükóz-6-foszfáttal (1a) kezdődik , amelyet a NAD + oxidál, és ketont képez C2-nél (2a). Ezt a ketont ezután piridoxál -foszfát (PLP) és glutamin -transzaminálás (3a) révén primer amincsoporttá alakítják . Ezt az eljárást ismételten megismételjük C4 -nél, hogy egy második primer amint (4a) kapjunk. Ha ez a két amin jelen van, a glükózgyűrű két S-adenozil-metionin- molekulán keresztül metilezhető (5a). Ezzel a metilezéssel a glükózgyűrű végre készen áll arra, hogy inozit -ciklázon (6a) keresztül inozitgyűrűvé alakítsa át. Ezt hidrolizálva lehet megszabadulni a foszfátcsoporttól, így az inozitgyűrű szükségessé válik a spektinomicinhez (7a).
Miközben mindez megtörténik, alternatív útvonalon történik a cukor funkcionális csoportjának létrehozása hasonló kiindulási termékből. Ezen az úton glükóz-1-foszfátot használnak kiindulási termékként (1b). Ez TDP-glükózzá alakul át a TDP- szintázon keresztül (2b). A TDP glükóz ezután a hidroxilcsoportot eltávolítja a C6 -ból egy hidratáz enzimmel (3b), amelyet ezután a NADH -n keresztül redukálnak C4 -en, és új terméket hoznak létre (4b). Ha jelen van a keton, a PLP és a glutamin bejöhetnek, hogy átalakítsák azt primer aminná (5b), amelyet ezután egy deaminázon (6b) keresztül eltávolíthatnak. Ez a 6b -re való átalakulás kettős redukcióval jár együtt C4 -nél és C3 -nál még két NADH -molekulán keresztül, így kapva az aminoglikozid képzéséhez szükséges végterméket. Ezzel a 7a. És a 6b.
Természet
Az aminociklitol osztályba tartozik, szoros rokonságban áll az aminoglikozidokkal . A spektinomicint iparilag állítják elő a Streptomyces spectabilis baktérium fermentációjával . A spektinomicint a természetben számos szervezet termeli, beleértve a cianobaktériumokat és a különböző növényfajokat. Sok plasztid genomjában vagy plasztómájában jelen van spc operonként , amely általában 2-10 gén hosszú. A méretkülönbség oka lehet az elavult gének megszüntetése vagy funkciójának nukleáris gének általi átvétele. A spektinomicint főként a szervezetek állítják elő, mint védekező mechanizmus a ragadozók ellen.
Történelem
A spektinomicint 1961 -ben fedezték fel. Az ellátás zavara 2001 -ben következett be.
Hivatkozások
Külső linkek
- "Spektinomicin" . Gyógyszerinformációs portál . Amerikai Országos Orvostudományi Könyvtár.