Tetrahidrokannabinolsav szintáz - Tetrahydrocannabinolic acid synthase
| Tetrahidrokannibinolsav szintáz | |||||||||
|---|---|---|---|---|---|---|---|---|---|

| |||||||||
| Azonosítók | |||||||||
| EK sz. | 1.21.3.7 | ||||||||
| Adatbázisok | |||||||||
| IntEnz | IntEnz nézet | ||||||||
| BRENDA | BRENDA bejegyzés | ||||||||
| ExPASy | NiceZyme kilátás | ||||||||
| KEGG | KEGG bejegyzés | ||||||||
| MetaCyc | anyagcsereút | ||||||||
| PRIAM | profil | ||||||||
| PDB struktúrák | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
Tetrahydrocannabinolic sav (THCA) szintáz (teljes név Δ 1 -tetrahydrocannabinolic-szintáz ) egy enzim, felelős katalizálja a kialakulását THCA származó cannabigerolic sav (CBGA). A THCA a tetrahidrokannabinol (THC) közvetlen előanyaga , a kannabisz fő pszichoaktív összetevője , amelyet a Cannabis sativa különböző törzseiből állítanak elő . Ezért a THCA -szintázt a kannabisz pszichoaktivitását szabályozó kulcsfontosságú enzimnek tekintik. A THCA szintáz polimorfizmusai a THC különböző szintjeit eredményezik a kannabisz növényekben, ami "drog típusú" és "rost típusú" C. sativa fajtákat eredményez.
Szerkezet
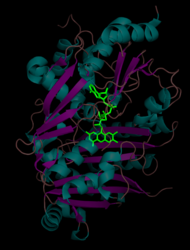
A THCA szintáz egy 60 kDa (~ 500 aminosav) monomer enzim, amelynek izoelektromos pontja 6,4. A poszt-transzlációs N-kapcsolt glikozilezés a teljes tömeget körülbelül 74 kDa-ra növeli. A harmadlagos szerkezet két doménre (I és II domén) oszlik, a flavin -adenin -dinukleotid (FAD) a két domén között helyezkedik el. Az I. tartomány nyolc alfa -hélixet és nyolc bétalapot tartalmaz, és kovalensen kötődik a FAD -hez. A II tartomány öt alfa -hélixet tartalmaz, amelyeket nyolc bétalap vesz körül. A hasonló aminosav -szekvenciákat megosztó enzimek közé tartozik a flavoproteinek berberine bridge enzim (BBE), a glüko -oligoszacharid -oxidáz (GOOX) és az aclacinomicin -oxidoreduktáz (AknOx).
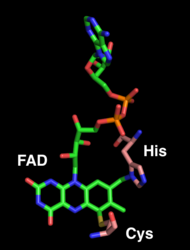
A FAD rész az enzimatikus aktivitás helye, és kovalensen kötődik a His114 -hez és a Cys176 -hoz. A FAD -t hidrogénkötések is kötik a szomszédos aminosav fő- és oldalláncokkal. A THCA szintáz és a szubsztrát vagy termék együttes kristályosítása még nem történt meg.
Reakciós mechanizmus
A THCA-szintáz, egy flavoprotein , használ egy flavin-adenin-dinukleotid (FAD) kofaktor , hogy katalizálják a oxidatív ciklizációs a monoterpén molekularész a cannabigerolic sav (CBGA). Hasonló ciklizációs reakciók fordulnak elő a geranil -pirofoszfátból származó monoterpén bioszintézisben , de nem oxidatívak. A THCA szintáz nem mutat katalitikus aktivitást a kannabigerol ellen , amelynek a CBGA -hoz képest nincs karboxilcsoportja , ami arra utal, hogy a CBGA karboxilcsoportja szükséges a reakció bekövetkezéséhez.
A teljes kémiai reakció a következő: CBGA + O 2 THCA + H 2 O 2

A CBGA -ból egy hidridet visznek át a FAD csökkentésére, egy hidroxilcsoport tirozinmaradék általi deprotonálásával . A CBGA monoterpénrészét ezután úgy helyezik el, hogy befejezze a ciklizációt THCA -vá. A redukált FAD O 2 termel hidrogén-peroxid (H 2 O 2 ) .
Biológiai funkció
A THCA-szintáz kifejeződik mirigyes szőrök a Cannabis sativa . A THCA szintáz hozzájárulhat a kannabisz növények önvédeleméhez azáltal, hogy THCA-t és hidrogén-peroxidot termel , amelyek egyaránt citotoxikusak . Mivel ezek a termékek mérgezőek a növényre, a THCA -szintáz kiválasztódik a trichome tároló üregébe. A THCA nekrózist kiváltó tényezőként is működik, mivel megnyitja a mitokondriális permeabilitási átmeneti pórusokat , gátolja a mitokondriális életképességet, és öregedést eredményez a levélszövetekben.
A THCA nem enzimatikus dekarboxilezése tárolás vagy dohányzás közben THC-t képez , amely a kannabisz fő pszichoaktív összetevője. A hőmérséklet, az auto-oxidáció és a fény további bomlása kannabinolt képez. A THC és más kannabinoidok közismerten csökkentik az émelygést és a hányást, valamint serkentik az éhséget, különösen a rákos kemoterápiában részesülő betegeknél .
A THCA szintázhoz hasonló enzimek katalizálják más kannabinoidok képződését. Például a kannabidiolsav (CBDA) szintáz egy flavoprotein, amely katalizálja a CPGA hasonló oxidatív ciklizálódását CBDA-vé, a szál típusú C. sativa domináns kannabinoid alkotórészévé . A CBDA hasonló dekarboxilezésen megy keresztül, és kannabidiolt képez .
Jelentőség
A gyógyszerészeti minőségű THC és más kannabinoidok iránti kereslet magas a lehetséges terápiás felhasználásuk iránti érdeklődés miatt , de sok országban akadályozzák a C. sativa termesztésére vonatkozó jogszabályok . A THC közvetlen kémiai szintézise nehéz a magas költségek és az alacsony hozam miatt. Ezért megvizsgálták a THCA szintáz felhasználását THC előállítására, mivel a CBGA könnyen szintetizálható, és a THCA könnyen dekarboxilál, hogy THC -t képezzen. A THCA bioszintézisét a THCA -szintáz szervezetekben történő expressziójával kísérletezték baktériumokban, rovarokban és dohánynövényekben korlátozott sikerrel. A THCA milligrammos skálán történő termelését két független vizsgálat bizonyította Pichia pastoris élesztősejtekben.