ATP szintáz - ATP synthase
| ATP szintézis | |||||||||
|---|---|---|---|---|---|---|---|---|---|
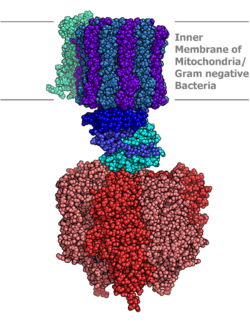 Az ATP-szintáz molekuláris modellje röntgenkristályos módszerrel . Az állórész itt nem látható.
| |||||||||
| Azonosítók | |||||||||
| EK sz. | 7.1.2.2 | ||||||||
| CAS -szám | 9000-83-3 | ||||||||
| Adatbázisok | |||||||||
| IntEnz | IntEnz nézet | ||||||||
| BRENDA | BRENDA bejegyzés | ||||||||
| ExPASy | NiceZyme kilátás | ||||||||
| KEGG | KEGG bejegyzés | ||||||||
| MetaCyc | anyagcsereút | ||||||||
| PRIAM | profil | ||||||||
| PDB struktúrák | RCSB PDB PDBe PDBsum | ||||||||
| Gén ontológia | AmiGO / QuickGO | ||||||||
| |||||||||
Az ATP szintáz egy fehérje, amely katalizálja az adenozin -trifoszfát (ATP) energiatároló molekula képződését adenozin -difoszfát (ADP) és szervetlen foszfát (P i ) segítségével. Ligázokba sorolják, mivel a PO kötés (foszfodiészter kötés) képződésével megváltoztatja az ADP -t. Az ATP szintáz által katalizált teljes reakció a következő:
- ADP + P i + 2H + kimenet ⇌ ATP + H 2 O + 2H + be
Az ATP ADP -ből és P i -ből történő képződése energetikailag kedvezőtlen, és általában fordított irányban haladna. Annak érdekében, hogy vezetni ez a reakció előrehalad, az ATP-szintetáz párok ATP szintézis során a sejtlégzést egy elektrokémiai gradiens által létrehozott különbség proton (H + ) koncentrációja az egész belső mitokondriális membrán az eukariótákban vagy a plazma membrán baktériumokban. A növények fotoszintézise során az ATP szintetizálódik az ATP szintetáz segítségével, a tylakoid lumenben létrejövő proton gradiens segítségével, a tylakoid membránon keresztül és a kloroplasztisz strómába .
Az eukarióta ATP-szintázok F-ATPázok , amelyek "fordítva" futnak az ATPáz esetében . Ez a cikk elsősorban ezzel a típussal foglalkozik. Az F-ATPáz két fő alegységből áll, F O és F 1 , amelyek forgó motoros mechanizmussal lehetővé teszik az ATP termelését. Az ATP szintáz egy molekuláris gép .
Elnevezéstan
Az F 1 frakció nevét az " 1. frakció" kifejezésből származtatja, és az F O ("o", és nem "nulla" betűs betűként írva) nevét az oligomicin kötő frakciójából származik, amely egy természetes eredetű antibiotikum, amely képes gátolni az F O egység ATP szintáz. Ezek a funkcionális régiók különböző fehérje alegységekből állnak - lásd a táblázatokat. Ezt az enzimet az ATP szintézisében használják aerob légzéssel.
Szerkezet és funkció
A thylakoid membránon és a belső mitokondriális membránon belül található ATP szintáz két F O és F 1 régióból áll . Az F O az F 1 forgását okozza, és c-gyűrűből és az a, két b, F6 alegységből áll. Az F 1 α, β, γ és δ alegységekből áll. Az F 1 vízoldható részből áll, amely hidrolizálja az ATP-t. Az F O -nak viszont főként hidrofób régiói vannak. Az F O F 1 utat teremt a protonok mozgására a membránon keresztül.
F 1 régió
Az ATP szintáz F 1 része hidrofil, és felelős az ATP hidrolíziséért. Az F 1 egység a mitokondriális mátrix térbe nyúlik ki. Az α és β alegységek hexamert alkotnak 6 kötési hellyel. Három közülük katalitikusan inaktív, és megkötik az ADP -t.
Három másik alegység katalizálja az ATP szintézist. A többi F 1 alegység γ, δ és ε egy forgó motoros mechanizmus (rotor/tengely) része. A γ alegység lehetővé teszi, hogy a β konformációs változásokon menjen keresztül (azaz zárt, félig nyitott és nyitott állapotokban), amelyek lehetővé teszik az ATP megkötését és felszabadítását a szintetizálás után. Az F 1 részecske nagy, és negatív festéssel látható az átviteli elektronmikroszkópban. Ezek 9 nm átmérőjű részecskék, amelyek borsozzák a belső mitokondriális membránt.
| Alegység | Emberi gén | jegyzet |
|---|---|---|
| alfa | ATP5A1 , ATPAF2 | |
| béta | ATP5B , ATPAF1 , C16orf7 | |
| gamma | ATP5C1 | |
| delta | ATP5D | A mitokondriális "delta" bakteriális/kloroplasztikus epsilon. |
| epsilon | ATP5E | A mitokondriumokra jellemző. |
| OSCP | ATP5O | "Delta" -nak nevezik bakteriális és kloroplasztikus változatokban. |
F O régió
Az F O vízben oldhatatlan fehérje, nyolc alegységgel és transzmembrán gyűrűvel. A gyűrű tetramer alakú, helix hurok hélix fehérjével, amely protonált és deprotonált konformációs változásokon megy keresztül, és a szomszédos alegységeket forgatni kényszeríti, ami az F O pörgését okozza, ami az F 1 konformációját is befolyásolja , ami az alfa állapotok váltását eredményezi és béta alegységek. A F O régióban ATP szintáz egy proton pórus amely be van ágyazva a mitokondriális membrán. Három fő alegységből áll, a, b és c. Hat c alegység alkotja a rotorgyűrűt, és a b alegység egy szárát az F 1 OSCP -hez, amely megakadályozza az αβ hexamer forgását. Az a alegység összeköti a b -t a c gyűrűvel. Az embereknek hat további alegysége van, d , e , f , g , F6 és 8 (vagy A6L). Az enzim ezen része a mitokondriális belső membránban helyezkedik el, és a proton transzlokációt a forgáshoz kapcsolja, ami az ATP szintézist okozza az F 1 régióban.
Az eukariótákban a mitokondriális F O membrán hajlító dimereket képez. Ezek a dimerek a kriszták végén hosszú sorokba rendeződnek , valószínűleg a kriszták kialakulásának első lépése. A dimer élesztő F O régiójának atommodelljét cryo-EM határoztuk meg, 3,6 Å általános felbontással.
| Alegység | Emberi gén |
|---|---|
| a | MT-ATP6 , MT-ATP8 |
| b | ATP5F1 |
| c | ATP5G1 , ATP5G2 , ATP5G3 |
Kötési modell

Az 1960-as és 1970-es években Paul Boyer , az UCLA professzora kifejlesztette a kötési változás vagy flip-flop mechanizmuselméletet, amely azt feltételezte, hogy az ATP szintézis az ATP szintáz konformációs változásától függ, amelyet a gamma alegység forgása generál. A kutatócsoport a John E. Walker , majd a MRC Laboratory of Molecular Biology in Cambridge , kristályosítjuk az F 1 katalitikus-doménjét ATP szintáz. A szerkezet, amely akkoriban a legnagyobb ismert aszimmetrikus fehérjeszerkezet, azt jelezte, hogy Boyer rotációs katalízis modellje lényegében helyes. Ennek tisztázására Boyer és Walker megosztották az 1997 -es kémiai Nobel -díj felét .
Az F 1 kristályszerkezete váltakozó alfa- és béta -alegységeket mutatott (mindegyikből 3 -at ), amelyek narancsszegmensekként rendeződtek egy forgó aszimmetrikus gamma alegység körül. Az ATP szintézis jelenlegi modellje (váltakozó katalitikus modell) néven az elektronszállító lánc által szállított (H+) protonkationok által létrehozott transzmembrán potenciál a (H+) protonkationokat a membránok közötti térből a membránon keresztül hajtja. F O régióban ATP szintáz. Az F O egy része (a c-alegységek gyűrűje ) forog, amikor a protonok áthaladnak a membránon. A c-gyűrű szorosan kapcsolódik az aszimmetrikus központi szárhoz (amely elsősorban a gamma alegységből áll), és ennek következtében forogni kezd az F 1 alfa 3 béta 3-ban, és ezáltal a 3 katalitikus nukleotid-kötőhely konformációs változásokon megy keresztül. ATP szintézishez vezet. A fő F 1 alegységeket a központi szárrotorral rokonszenvben el nem forgatja egy perifériás szár, amely az alfa 3 béta 3-at az F O nem forgó részéhez köti . Az ép ATP-szintáz szerkezete jelenleg alacsony felbontású , a komplex elektronkriomikroszkópos (cryo-EM) vizsgálatai alapján ismert. Az ATP-szintáz krio-EM modellje azt sugallja, hogy a perifériás szár rugalmas szerkezet, amely körülveszi a komplexet, amikor az F 1-et az F O-hoz kapcsolja . Megfelelő körülmények között az enzimreakció fordítva is végrehajtható, az ATP hidrolízis hajtja a protont a membránon keresztül.
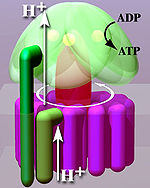
A kötési változási mechanizmus magában foglalja a β alegység három állapot közötti ciklusának aktív helyét. "Laza" állapotban az ADP és a foszfát belép az aktív helyre; a szomszédos diagramon ez rózsaszínnel látható. Az enzim ezután alakváltozáson megy keresztül, és összekényszeríti ezeket a molekulákat, és az aktív hely a kapott "szűk" állapotban (pirossal jelölt) nagyon nagy affinitással köti az újonnan előállított ATP -molekulát . Végül az aktív hely visszatér a nyitott állapotba (narancssárga), felszabadítva az ATP -t, és több ADP -t és foszfátot kötve, készen az ATP -termelés következő ciklusára.
Fiziológiai szerep
Más enzimekhez hasonlóan az F 1 F O ATP szintáz aktivitása reverzibilis. Nagy elegendő mennyiségű ATP oka, hogy hozzon létre egy transzmembrán proton gradiens , ezt használják a fermentáló baktériumok, amelyek nem rendelkeznek elektrontranszport lánc, hanem hidrolizálnak ATP, hogy a proton gradiens, amely az általuk használt vezetni csilló és szállítására tápanyagok kerülnek a sejtbe.
A baktériumok lélegeztetésénél fiziológiai körülmények között az ATP -szintáz általában az ellenkező irányba fut, és ATP -t hoz létre, miközben energiaforrásként használja az elektronszállító lánc által létrehozott proton -mozgatóerőt . Az ilyen módon történő energiatermelés általános folyamatát oxidatív foszforilációnak nevezzük . Ugyanez a folyamat zajlik a mitokondriumokban is , ahol az ATP szintáz a belső mitokondriális membránban helyezkedik el, és az F 1 rész a mitokondriális mátrixba vetül . Az ATP-szintézis általi ATP-fogyasztás protonkationokat szivattyúz a mátrixba.
Evolúció
Úgy gondolják, hogy az ATP -szintáz fejlődése moduláris volt, amellyel két funkcionálisan független alegység társult és új funkciókat nyert. Úgy tűnik, hogy ez az összefüggés az evolúciós történelem elején következett be, mivel lényegében ugyanaz az ATP -szintáz enzimek szerkezete és aktivitása van jelen az élet minden királyságában. Az F-ATP szintáz nagy funkcionális és mechanikai hasonlóságot mutat a V-ATPázzal . Míg azonban az F-ATP szintáz ATP-t állít elő protongradiens felhasználásával, addig a V-ATPáz protongradienst hoz létre az ATP rovására, és akár 1-es pH-értékeket generál.
Az F 1 régió szintén jelentős hasonlóságot mutat a hexamerikus DNS helikázokkal (különösen a Rho faktorral ), és a teljes enzimrégió némi hasonlóságot mutat a H+
-powered T3SS vagy flagelláris motor komplexek. Az F 1 régió α 3 β 3 hexamerje jelentős szerkezeti hasonlóságot mutat a hexamer DNS helikázokkal; mindkettő 3-szoros forgási szimmetriájú gyűrűt képez, központi pórusokkal. Mindkettő szerepe a makromolekula póruson belüli relatív forgásától függ; a DNS -helikázok a DNS spirális alakját használják a mozgásuk irányítására a DNS -molekula mentén és a szupertekercselés kimutatására, míg az α 3 β 3 -hexamer a konformációs változásokat használja a γ alegység forgása révén, hogy enzimatikus reakciót vezessen be.
A H+
az F O részecske motorja nagy funkcionális hasonlóságot mutat a H -val+
motorok, amelyek flagellát hajtanak. Mindkettőben sok kis alfa-spirális fehérje van, amelyek a közeli álló fehérjékhez képest forognak, H-t használva+
potenciális gradiens, mint energiaforrás. Ez a kapcsolat azonban gyenge, mivel a zászlós motorok általános szerkezete sokkal összetettebb, mint az F O részecskéé, és a körülbelül 30 forgó fehérjét tartalmazó gyűrű sokkal nagyobb, mint az F O 10, 11 vagy 14 spirális fehérje összetett. Az újabb szerkezeti adatok azonban azt mutatják, hogy a gyűrű és a szár szerkezetileg hasonló az F 1 részecskéhez.
Az ATP szintézis eredetére vonatkozó moduláris evolúciós elmélet azt sugallja, hogy két független funkciójú alegység, egy ATPáz aktivitású DNS -helikáz és egy H+
motor, képesek voltak megkötni, és a motor forgása fordítottan hajtotta a helikáz ATPáz aktivitását. Ez a komplex nagyobb hatékonyságot fejlesztett, és végül a mai bonyolult ATP szintézisekké fejlődött. Alternatív megoldásként a DNS -helikáz/ H+
motorkomplexumban lehetett H+
szivattyútevékenység a H -t hajtó helikáz ATPáz aktivitásával+
motor hátramenetben. Ez a fordított reakció végrehajtásához és ATP -szintázként működhet.
Gátlók
Számos természetes és szintetikus ATP -szintáz inhibitorot fedeztek fel. Ezeket az ATP szintáz szerkezetének és mechanizmusának vizsgálatára használták. Néhányuk terápiás célra is hasznos lehet. Az ATP szintáz inhibitorok több osztálya létezik, beleértve a peptid inhibitorokat, polifenolos fitokemikáliákat, poliketideket, ónorganikus vegyületeket, polién α-piron származékokat, kationos inhibitorokat, szubsztrát analógokat, aminosav módosítókat és egyéb vegyi anyagokat. A leggyakrabban használt ATP szintáz inhibitorok közül néhány az oligomicin és a DCCD .
Különféle szervezetekben
Baktériumok
Az E. coli ATP szintáz az ATP szintetáz legegyszerűbb ismert formája, 8 különböző alegységtípussal.
A bakteriális F-ATPázok időnként fordítva is működhetnek, és ATPázzá alakítják őket. Néhány baktériumnak nincs F-ATPáza, kétirányú A/V típusú ATPáz segítségével.
Élesztő
Az élesztő ATP szintáz az egyik legjobban tanulmányozott eukarióta ATP szintáz; és öt F 1 , nyolc F O alegységet és hét kapcsolódó fehérjét azonosítottak. A legtöbb ilyen fehérje homológ más eukariótákban.
Növény
A növényekben az ATP szintáz a kloroplasztokban is jelen van (CF 1 F O -ATP szintáz). Az enzim a tilakoid membránba van integrálva ; a CF 1 -rész a sztrómába tapad , ahol a fotoszintézis sötét reakciói (más néven fényfüggetlen reakciók vagy Calvin -ciklus ) és az ATP -szintézis zajlik. A kloroplasztisz ATP szintáz általános szerkezete és katalitikus mechanizmusa majdnem megegyezik a bakteriális enzimével. A kloroplasztokban azonban a proton mozgatóerőt nem a légző elektron transzportlánc, hanem az elsődleges fotoszintetikus fehérjék generálják. A szintáz 40 mm-es inszertet tartalmaz a gamma alegységben, hogy sötétben gátolja a pazarló tevékenységet.
Emlős
A szarvasmarha ( Bos taurus ) szív-mitokondriumokból izolált ATP-szintáz biokémiai és szerkezeti szempontból a legjobban jellemzett ATP-szintáz. A marhaszívet az enzim forrásaként használják, mivel a szívizomban magas a mitokondrium -koncentráció. Génjeik szoros homológiát mutatnak az emberi ATP -szintázokkal.
Az ATP szintézis összetevőit kódoló emberi gének:
- ATP5A1
- ATP5B
- ATP5C1 , ATP5D , ATP5E , ATP5F1 , ATP5G1 , ATP5G2 , ATP5G3 , ATP5H , ATP5I , ATP5J , ATP5J2 , ATP5L , ATP5O
- MT-ATP6 , MT-ATP8
Más eukarióták
Az egyes származási vonalhoz tartozó eukariótáknak nagyon különleges szervezeteik vannak az ATP szintázban. Az euglenozoa ATP szintáz egy bumeráng alakú F 1 fejű dimert képez, mint más mitokondriális ATP szintázok, de az F O alkomplex számos egyedi alegységgel rendelkezik. Kardiolipint használ . A gátló IF 1 is másként kötődik, a trypanosomatida -val közös módon .
Archaea
Az Archaea-ban általában nincs F-ATPáz. Ehelyett az ATP-t szintetizálják az A-ATPáz/szintáz segítségével, amely egy rotációs gép, amely szerkezetileg hasonlít a V-ATPázhoz, de elsősorban ATP szintázként működik. Az F-ATPáz baktériumokhoz hasonlóan úgy gondolják, hogy ATPázként is működik.
Lásd még
- A mitokondriális ATPáz komplex F O szektorának összeállításához szükséges ATP10 fehérje .
- Kloroplaszt
- Elektronátviteli lánc
- Flavoprotein
- Mitokondrium
- Oxidatív foszforiláció
- P-ATPáz
- Proton szivattyú
- Forgó mozgás élő rendszerekben
- Transzmembrán ATPáz
- V-ATPáz
Hivatkozások
További irodalom
- Nick Lane: A létfontosságú kérdés: energia, evolúció és a komplex élet eredete , Ww Norton, 2015-07-20, ISBN 978-0393088816 (A link az ATP-szintáz modelljét bemutató 10. ábrára mutat)
Külső linkek
- Boris A. Feniouk: "ATP szintáz - csodálatos molekuláris gép"
- Jól illusztrált ATP szintézis előadás Antony Crofts -tól, az Illinois -i Egyetemről, Urbana – Champaign .
- Proton és nátrium transzlokáló F-, V- és A-típusú ATPázok az OPM adatbázisban
-
A kémiai Nobel -díjat 1997 Paul D. Boyer és John E. Walker az ATP szintézisének enzimatikus mechanizmusáért; és Jens C. Skou-nak, egy ionszállító enzim, a Na+
, K+
-ATPáz. - Harvard Multimédia Gyártóhely - Videók - ATP szintézis animáció
- David Goodsell: "ATP szintézis- A hónap molekulája"