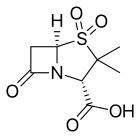
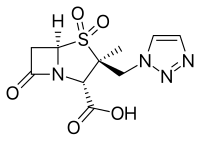
β -laktamáz inhibitor - β-Lactamase inhibitor
A béta-laktamázok olyan enzimcsalád , amelyek részt vesznek a baktériumok rezisztenciájában a béta-laktám antibiotikumokkal szemben . A béta -laktámgyűrű feltörésével hatnak, amely lehetővé teszi a penicillin -szerű antibiotikumok működését. A rezisztencia ezen formájának leküzdésére irányuló stratégiák között szerepelt az új béta-laktám antibiotikumok kifejlesztése, amelyek jobban ellenállnak a hasításnak, valamint a béta-laktamáz inhibitoroknak nevezett enzimgátlók osztályának kifejlesztése . Bár a β-laktamáz inhibitorok kis antibiotikum aktivitással rendelkeznek, megakadályozzák a béta-laktám antibiotikumok bakteriális lebomlását, és így kiterjesztik azon baktériumok körét, amelyek ellen a gyógyszerek hatékonyak.
Orvosi felhasználás
A béta-laktamáz inhibitorok legfontosabb felhasználása olyan fertőzések kezelésében van, amelyekről ismert vagy feltételezhető, hogy azokat Gram-negatív baktériumok okozzák , mivel a béta-laktamáz termelés fontos szerepet játszik a béta-laktám rezisztencia kialakulásában ezekben a kórokozókban. Ezzel szemben a gram-pozitív baktériumokban a legtöbb béta-laktám-rezisztencia a penicillin-kötő fehérjék eltéréseinek köszönhető, amelyek a béta-laktámhoz való kötődés csökkenéséhez vezetnek. A Staphylococcus aureus gram-pozitív kórokozó béta-laktamázokat termel, de a béta-laktamáz inhibitorok kisebb szerepet játszanak ezen fertőzések kezelésében, mivel a legrezisztensebb törzsek ( meticillin-rezisztens Staphylococcus aureus ) is használnak penicillin-kötő variánsokat.
A cselekvés mechanizmusa
Az Ambler osztályozási rendszer az ismert béta-laktamáz enzimeket négy csoportba sorolja a szekvenciahomológia és a feltételezett filogenetikai összefüggések szerint. Az A, C és D osztály a béta-laktámokat a szerin proteázok mechanizmusához hasonló többlépcsős mechanizmuson keresztül hasítja . Kötődéskor a béta-laktamáz aktív helyén lévő szerin-hidroxil-csoport átmeneti kovalens kötést képez a béta-laktámgyűrű karbonilcsoporthoz, és a folyamat során hasítja a béta-laktámgyűrűt. Második lépésben a vízmolekula nukleofil támadása megszakítja a kovalens kötést az enzim és a korábbi béta-laktám karbonilcsoportja között. Ez lehetővé teszi a lebontott béta-laktám diffúzióját, és felszabadítja az enzimet további béta-laktám-molekulák feldolgozására.
A jelenleg rendelkezésre álló béta-laktamáz inhibitorok hatékonyak az Ambler A osztályú béta-laktamázok (tazobaktám, klavulanát és szulbaktám) vagy az Ambler A, C osztály és egyes D osztályú béta-laktamázok (avibaktám) ellen. A béta-laktám antibiotikumokhoz hasonlóan ezeket is béta-laktamázok dolgozzák fel, hogy kiindulási kovalens köztiterméket képezzenek. A béta-laktám antibiotikumoktól eltérően az inhibitorok öngyilkossági szubsztrátok (tazobaktám és szulbaktám) működnek, ami végül a béta-laktamáz lebomlásához vezet. Az Avibactam viszont nem tartalmaz béta-laktámgyűrűt (nem béta-laktám-béta-laktamáz inhibitor), hanem visszafordíthatóan kötődik .
Az Ambler B osztályú béta-laktamázok a metalloproteázokhoz hasonló mechanizmussal hasítják a béta-laktámokat . Mivel kovalens intermedier nem képződik, a forgalomba hozott béta-laktamáz inhibitorok hatásmechanizmusa nem alkalmazható. Így a metallo-béta-laktamázokat expresszáló baktériumtörzsek, mint például az új-delhi metallo-béta-laktamáz 1, terjedése komoly aggodalomra ad okot.
Gyakran használt szerek
A jelenleg forgalmazott β-laktamáz inhibitorok nem különálló gyógyszerek. Ehelyett egy hasonló szérum felezési idővel rendelkező β-laktám antibiotikummal készítik őket. Ez nemcsak az adagolás kényelme érdekében történik, hanem annak érdekében is, hogy minimálisra csökkentsük az egyik vagy másik gyógyszer különböző expozíciója következtében fellépő rezisztencia kialakulását. A gram-negatív bakteriális fertőzések kezelésére használt β-laktám antibiotikumok fő osztályai közé tartozik (a béta-laktamázok általi hasítással szembeni belső rezisztencia megközelítő sorrendjében) a penicillinek (különösen az aminopenicillinek és az ureidopenicillinek), a 3. generációs cefalosporinok és a karbapenemek. Az egyes β-laktamáz variánsok ezen gyógyszerosztályok közül egyet vagy többet célozhatnak meg, és csak egy alcsoportot gátol egy adott β-laktamáz inhibitor. A β-laktamáz inhibitorok kibővítik ezen β-laktám antibiotikumok hasznos spektrumát azáltal, hogy gátolják a baktériumok által termelt β-laktamáz enzimeket, hogy inaktiválják őket.
- β-laktamáz inhibitorok β-laktám maggal:
- A tebipenem az első karbapenem, amelyet orálisan tebipenem-pivoxil formájában adnak be. A tebipenem szerkezeti és kinetikai vizsgálatai rendelkezésre állnak M. tuberculosis béta-laktamázzal (BlaC).
- A klavulánsav vagy klavulanát, általában együtt amoxicillin ( Augmentin ) vagy ticarcillin ( Timentint )
- Sulbaktám , általában ampicillinnel ( Unasyn ) vagy cefoperazonnal ( Sulperazon ) kombinálva
- Tazobactam , általában együtt piperacillin ( Zosyn és Tazocin )
- β-laktamáz inhibitorok diazabiciklo-oktán maggal:
- Az Avibactam , amelyet ceftazidim -szel ( Avycaz ) kombinálva engedélyeztek , jelenleg klinikai vizsgálatok alatt állnak a ceftarolinnal való kombinációban
- Relebactam , imipenem/cilastatin ( Recarbrio ) kombinációban alkalmazva .
- β-laktamáz inhibitorok más típusú nem β-laktám magokkal:
- Vaborbactam , meropenemmel ( Vabomere ) kombinálva . Van egy boronsav magot.
Béta-laktamázt termelő baktériumok
A béta-laktamázokat termelő baktériumok közé tartoznak, de nem kizárólagosan:
-
Staphylococcus
- MRSA (Meticillin-rezisztens Staphylococcus aureus)
- Enterobacteriaceae :
- Haemophilus influenzae
- Neisseria gonorrhoeae
- Pseudomonas aeruginosa
- Mycobacterium tuberculosis
Kutatás
Egyes baktériumok kiterjesztett spektrumú β-laktamázokat (ESBL) termelhetnek, ami megnehezíti a fertőzés kezelését, és további rezisztenciát biztosít a penicillinekkel , cefalosporinokkal és monobaktámokkal szemben . A bórsavszármazékokat jelenleg széles körű és kiterjedt kutatások végzik, mint a béta-laktamázok új aktív gátlói, mivel olyan helyet tartalmaznak, amely utánozza azt az átmeneti állapotot, amelyen a béta-laktámok keresztülmennek, amikor béta-laktamázokon keresztül hidrolizálnak. Általában azt találták, hogy jól illeszkednek sok béta-laktamáz aktív helyéhez, és kényelmes tulajdonságuk, hogy nem képesek hidrolizálni, és ezért használhatatlanná teszik őket. Ez kedvező gyógyszerkészítmény számos, klinikailag használt, egymással versengő szerrel szemben, mivel ezek többsége, például a klavulánsav, hidrolizálódik, és ezért csak véges ideig használható. Ez általában azt eredményezi, hogy szükség van egy magasabb koncentrációjú kompetitív inhibitorra, mint egy nem hidrolizálható inhibitor esetében. A különböző bórsavszármazékokat a béta-laktamázok sokféle izoformájához lehet igazítani, ezért képesek a béta-laktám antibiotikumok hatékonyságának helyreállítására.
Hivatkozások
Külső linkek
- Xu H, Hazra S, Blanchard JS (2012. június). "Az NXL104 visszafordíthatatlanul gátolja a Mycobacterium tuberculosis β-laktamázt" . Biokémia . 51 (22): 4551–7. doi : 10.1021/bi300508r . PMC 3448018 . PMID 22587688 .
- Kurz SG, Wolff KA, Hazra S, Bethel CR, Hujer AM, Smith KM, Xu Y, Tremblay LW, Blanchard JS, Nguyen L, Bonomo RA (2013. december). "A Mycobacterium tuberculosis β-Lactamase BlaC gátlóanyag-rezisztens szubsztitúciói vezethetnek-e a klavulanát-rezisztenciához ?: biokémiai indoklás a β-laktám-β-laktamáz inhibitor kombinációk alkalmazására" . Antimikrobiális szerek és kemoterápia . 57. (12): 6085–96. doi : 10.1128/AAC.01253-13 . PMC 3837893 . PMID 24060876 .