Klavulánsav - Clavulanic acid
 | |
 | |
| Klinikai adatok | |
|---|---|
| Kiejtés | / ˌ k l æ v j ʊ l æ n ɪ k / |
| AHFS / Drugs.com | Nemzetközi gyógyszernevek |
| Terhességi kategória |
|
| Utak ügyintézés |
Szóbeli, IV |
| ATC kód | |
| Jogi státusz | |
| Jogi státusz | |
| Farmakokinetikai adatok | |
| Biológiai hozzáférhetőség | "Jól felszívódik" |
| Anyagcsere | Máj (kiterjedt) |
| Felszámolási felezési idő | 1 óra |
| Kiválasztás | Vese (30–40%) |
| Azonosítók | |
| |
| CAS-szám | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox műszerfal ( EPA ) | |
| ECHA InfoCard |
100,055,500 |
| Kémiai és fizikai adatok | |
| Képlet | C 8 H 9 N O 5 |
| Moláris tömeg | 199,162 g · mol −1 |
| 3D modell ( JSmol ) | |
| |
| |
| (ellenőrizni) | |
A klavulánsav egy β-laktám gyógyszer , amely mechanizmus alapú β-laktamáz inhibitorként működik . Noha önmagában nem hatékony, mint antibiotikum , penicillin- csoport antibiotikumokkal kombinálva képes legyőzni az β-laktamázt szekretáló baktériumok antibiotikum-rezisztenciáját , amely egyébként inaktiválja a penicillinek nagy részét.
Leggyakoribb készítményeiben a kálium-klavulanátot (a klavulánsavat káliumsóként) kombinálják:
- amoxicillin ( ko- amoxiclav, Augmentin, Tyclav, Clavamox ( állat-egészségügyi ), Synulox ( állat-egészségügyi ) és mások kereskedelmi nevek )
- licarcillin ( co-ticarclav , kereskedelmi név Timentin)
A klavulánsavat 1974-ben szabadalmaztatták.
Orvosi felhasználás
Az amoxicillin-klavulánsav sokféle fertőzés első vonalbeli kezelése, beleértve a sinusfertőzéseket és a húgyúti fertőzéseket, beleértve a pyelonephritist is . Ez részben annak a gram-pozitív baktériumokkal szembeni hatékonyságának köszönhető, amelyeket általában nehezebb ellenőrizni, mint kemoterápiás antibiotikumokkal végzett gram-negatív baktériumokat .
Káros hatások
A klavulánsav és penicillinek együttes alkalmazását a kolesztatikus sárgaság és az akut hepatitis előfordulásának növekedésével társítják a terápia során vagy röviddel azután. A kapcsolódó sárgaság általában önkorlátozó és nagyon ritkán végzetes.
Az Egyesült Királyság Gyógyszerbiztonsági Bizottsága (CSM) azt javasolja, hogy az olyan kezeléseket, mint az amoxicillin / klavulánsav készítmények, tartsák fenn olyan bakteriális fertőzések számára, amelyeket valószínűleg az amoxicillin-rezisztens β-laktamázt termelő törzsek okoznak, és a kezelés általában nem haladhatja meg a 14 napot.
Allergiáról számoltak be.
Források
Az elnevezés a Streptomyces clavuligerus törzséből származik , amely klavulánsavat termel.
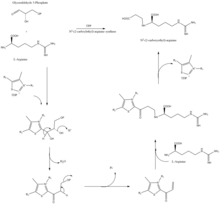
Bioszintézis
A klavulánsav β-laktám- szerű szerkezete szerkezetileg hasonló a penicillinhez , de ennek a molekulának a bioszintézise más biokémiai utat foglal magában. A klavulánsavat baktérium által termelt Streptomyces clavuligerus , felhasználásával a gliceraldehid-3-foszfát- és L -arginin kiindulási anyagként. Jóllehet az út minden közbenső terméke ismert, az összes enzimatikus reakció pontos mechanizmusa nem teljesen ismert. Az eljárás elsősorban magában 3 enzimek: clavaminate szintáz , β-laktám-szintetáz, és N 2 - (2-karboxi-etil) -L-arginin (CEA) szintáz . A klavaminát-szintáz egy nem hem-oxigenáz, amely a vastól és az α-keto-glutaráttól függ, és amelyet a klavulánsav-génfürt orf5 kódol . Az enzim működésének specifikus mechanizmusa nem teljesen ismert, de ez az enzim a klavulánsav teljes szintézisének 3 lépését szabályozza. Mindhárom lépés a katalitikus, vas-tartalmú reakcióközpont ugyanazon régiójában történik, de nem sorozatosan fordul elő és befolyásolja a klavulánsav-szerkezet különböző területeit.
A β-laktám-szintetáz egy 54,5 kDa-os fehérje, amelyet a klavulánsav-génfürt orf3 kódol, és hasonlóságot mutat az aszparagin-szintáz - B osztályú enzimekkel. Annak pontos mechanizmusa, hogy ez az enzim hogyan működik a β-laktám szintetizálásában , nem bizonyított, de feltételezhető, hogy a CEA szintázzal és az ATP- vel együttműködve fordul elő .
A CEA-szintáz egy 60,9 kDA fehérje, és ez az első gén, amely a klavulánsav-bioszintézis géncsoportban található, és amelyet a klavulánsav-gén-klaszter orf2 kódol. Az enzim működésének konkrét mechanizmusát még vizsgálják; azonban ismert, hogy ez az enzim képes a glicerinaldehid-3-foszfátot L-argininnel összekapcsolni tiamin-difoszfát (TDP vagy tiamin-pirofoszfát ) jelenlétében , ami a klavulánsav bioszintézisének első lépése.
Történelem
A klavulánsavat 1974-75 körül fedezték fel a Beecham gyógyszercégnél dolgozó brit tudósok a Streptomyces clavuligerus baktériumtól . Több kísérlet után, Beecham végül beadta a US szabadalmi védelmet a kábítószer-1981-ben, és az amerikai szabadalmak 4.525.352, 4.529.720, és 4.560.552 kaptak 1985.
A klavulánsav elhanyagolható belső mikrobaellenes aktivitással rendelkezik, annak ellenére, hogy megosztja a β-laktám gyűrűt, amely a β-laktám antibiotikumokra jellemző . A kémiai szerkezet hasonlósága azonban lehetővé teszi, hogy a molekula kölcsönhatásba lépjen bizonyos baktériumok által kiválasztott β-laktamáz enzimmel , hogy rezisztenciát teremtsen a β-laktám antibiotikumokkal szemben.
A klavulánsav öngyilkos inhibitor , kovalens kapcsolódáshoz egy szerin maradékot a aktív helyén a β-laktamáz. Ez átalakítja a klavulánsavmolekulát, létrehozva egy sokkal reaktívabb fajt, amely megtámadja az aktív hely másik aminosavat, véglegesen inaktiválja azt, és így inaktiválja az enzimet.
Ez a gátlás helyreállítja a β-laktám antibiotikumok antimikrobiális aktivitását a laktamázt szekretáló rezisztens baktériumok ellen. Ennek ellenére kialakultak olyan baktériumtörzsek, amelyek még az ilyen kombinációk ellen is rezisztensek.