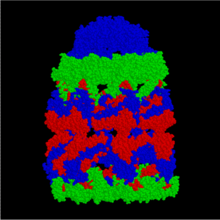
Chaperonin - Chaperonin
| TCP-1/cpn60 chaperonin család | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 A GroEL bakteriális chaperonin szerkezete.
| |||||||||||
| Azonosítók | |||||||||||
| Szimbólum | Cpn60_TCP1 | ||||||||||
| Pfam | PF00118 | ||||||||||
| InterPro | IPR002423 | ||||||||||
| PROSITE | PDOC00610 | ||||||||||
| CATH | 5GW5 | ||||||||||
| SCOP2 | 1 gr / SCOPe / SUPFAM | ||||||||||
| CDD | cd00309 | ||||||||||
| |||||||||||
A HSP60 , más néven chaperonins ( Cpn ), a hősokk fehérjék családja, eredetileg 60 kDa molekulatömegük szerint válogatva. Megakadályozzák a fehérjék hibás összecsukódását stresszes helyzetekben, például nagy melegben, segítve a fehérje hajtogatását. A HSP60 a fehérjék hajtogatását segítő molekulák nagy osztályába tartozik, az úgynevezett molekuláris chaperonoknak .
Az újonnan előállított fehérjék általában kell szeres a lineáris láncban az aminosavak háromdimenziós harmadlagos szerkezetet . A fehérjék hajtogatásához szükséges energiát az egyes fehérjék aminosav-oldalláncai közötti nem kovalens kölcsönhatások és az oldószer hatása biztosítja. A legtöbb fehérje spontán módon a legstabilabb háromdimenziós konformációjába hajlik, ami általában a funkcionális konformációjuk is, de esetenként a fehérjék rosszul hajlanak össze. A molekuláris chaperonok katalizálják a fehérje újrahajtogatását azáltal, hogy felgyorsítják a rosszul összehajtott fehérjék részleges kibontakozását, amit az adenozin -trifoszfát (ATP) hidrolíziséből származó energia segít . A chaperonin fehérjék a rosszul hajtogatott fehérjéket is lebonthatják.
Szerkezet
Ezeknek a chaperonineknek a szerkezete két fánkra hasonlít, amelyeket egymásra helyezve hordót hoznak létre. Minden gyűrű 7, 8 vagy 9 alegységből áll, attól függően, hogy milyen szervezetben található a chaperonin. Minden ~ 60 kDa peptidlánc három doménre osztható: apikális, köztes és egyenlítői.
Az eredeti chapronin javasoljuk, hogy alakult egy peroxiredoxin .
Osztályozás
I. csoport
Az I. csoport chaperoninjai (Cpn60) megtalálhatók a baktériumokban , valamint az endoszimbiotikus eredetű organellákban : kloroplasztokban és mitokondriumokban .
Az E. coli -ban található GroEL/GroES komplex egy I. csoportú chaperonin és a legjobban jellemzett nagy (~ 1 MDa) chaperonin komplex.
- A GroEL egy kettős gyűrűs, 14 méteres, zsíros hidrofób folttal a nyílásánál, és képes befogadni a 15-60 kDa méretű szubsztrátumok natív hajtogatását.
- GroES (egygyűrűs heptamer, amely a GroEL-hez kötődik ATP vagy az ATP hidrolízis átmeneti állapotú analógjai, például az ADP-AlF 3. jelenlétében . Olyan, mint a GroEL-t borító fedél (doboz/palack).
Előfordulhat, hogy a GroEL/GroES nem képes visszavonni a fehérjeaggregátumokat, de kinetikailag verseng a rossz összehajtogatás és aggregáció útján, ezáltal megakadályozva az aggregátumok képződését.
A Cpn60 alcsaládot 1998 -ban fedezték fel. 1992 -ben szekvenálták. A cpn10 és cpn60 oligomerekhez Mg 2+ -ATP is szükséges , hogy kölcsönhatásba lépjenek egy funkcionális komplex létrehozásához. A cpn10 kötődése a cpn60 -hoz gátolja a cpn60 gyenge ATPáz aktivitását.
A RuBisCO alegységet megkötő fehérje ennek a családnak a tagja. Az Escherichia coli GroEL kristályszerkezete 2,8 Å -re oldódott fel.
Egyes baktériumok több példányban használják ezt a chaperonint, valószínűleg különböző peptidekhez.
II. Csoport
Az eukarióta citoszolban és az archae- ban található II. Csoportbeli chaperoninok (TCP-1) rosszabb jellemzésűek.
- A komplexum archaea nevezik thermosome . A homo-16mer néhány archeában, a prototípusos II. Típusú chaperoninnak tekinthető.
- A TRiC , az eukarióta chaperonin, nyolc különböző, bár rokon alegységből álló két gyűrűből áll , amelyek mindegyike nyolctagú gyűrűnként egyszer szerepel. A TRiC eredetileg azt hitték, hogy csak a citoszkeletális fehérjéket, az aktint és a tubulint hajtogatja, de ma már ismert, hogy tucatnyi szubsztrátot hajtogat.
A Methanococcus maripaludis chaperonin (Mm cpn) tizenhat azonos alegységből áll (gyűrűnként nyolc). Kimutatták, hogy hajtogatja a mitokondriális fehérjét (rodán); természetes szubsztrátokat azonban még nem azonosítottak.
A II. Csoportba tartozó chaperoninek nem gondolják, hogy GroES-típusú kofaktorokat használnak szubsztrátumuk hajtogatására. Ehelyett "beépített" fedelet tartalmaznak, amely ATP-függő módon záródik, hogy beágyazhassa szubsztrátjait, ami szükséges az optimális fehérjehajtási aktivitáshoz. Ezenkívül kölcsönhatásba lépnek egy társkísérővel, prefoldinnal , amely elősegíti az aljzat bejutását .
Más családok
A III. Csoportba tartoznak a II. Csoporthoz kapcsolódó bakteriális Cpns -ek. Van fedelük, de a fedélnyílás nem együttműködő bennük. Úgy gondolják, hogy ősi rokona a II.
Az EL fágból származó I. csoport chapronin gp146 nem használ fedőt, és a fánk interfész jobban hasonlít a II. Ez egy másik ősi típusú chapronin lehet.
A cselekvés mechanizmusa
A chaperoninok nagy konformációs változásokon mennek keresztül a hajtogatási reakció során, az ATP enzimatikus hidrolízisének , valamint a szubsztrátproteinek és a cochaperoninok, például a GroES kötődésének függvényében. Ezek a konformációs változások lehetővé teszik a chaperonin számára, hogy megkötjön egy kihajtott vagy rosszul összehajtott fehérjét, beágyazva ezt a fehérjét a két gyűrű által kialakított üregek egyikébe, és visszaengedve a fehérjét az oldatba. A felszabadulás után a szubsztrátfehérje vagy hajtogatott, vagy további hajtogatási köröket igényel, ebben az esetben ismét egy chaperonin kötheti meg.
A pontos mechanizmus, amellyel a chaperoninek megkönnyítik a szubsztrátfehérjék hajtogatását, nem ismert. A legutóbbi, különböző kísérleti technikákkal végzett elemzések szerint a GroEL-hez kötött szubsztrátproteinek tömör és lokálisan kitágult állapotok együttesét töltik be, amelyek nem rendelkeznek stabil tercier kölcsönhatással. A chaperonin hatásának számos modelljét javasolták, amelyek általában a chaperonin belső két (nem egymást kizáró) szerepére összpontosítanak: a passzívra és az aktívra. A passzív modellek a chaperonin ketrecet közömbös formaként kezelik, befolyásolva a fehérje szubsztrát számára hozzáférhető konformációs tér csökkentését vagy az intermolekuláris kölcsönhatások megakadályozását, például az aggregáció megelőzésével. Az aktív chaperonin szerep viszont specifikus chaperonin -szubsztrát kölcsönhatásokhoz kapcsolódik, amelyek a chaperonin konformációs átrendeződéséhez kapcsolódhatnak.
A chaperonin aktív szerepének valószínűleg a legnépszerűbb modellje az iteratív lágyító mechanizmus (IAM), amely az iteratív és hidrofób jellegű, a fehérje szubsztrát chaperoninhoz való kötődésének hatására összpontosít. Számítási szimulációs tanulmányok szerint az IAM termelékenyebb hajtogatáshoz vezet azáltal, hogy kibontja a szubsztrátot a rosszul összehajtogatott konformációkból, vagy megakadályozza a fehérje félrehajtását a hajtogatási útvonal megváltoztatásával.
A szerkezeti és funkcionális homológia megőrzése
Mint említettük, minden sejt tartalmaz chaperonint.
- A baktériumok archetípusa az E. coli- ból származó, jól jellemzett chaperonin GroEL .
- Az archaea -ban a chaperonint termoszómának nevezik .
- Az eukariában a citoplazmatikus chaperonint CCT -nek (más néven TRiC ) nevezik .
Ezek a fehérjekomplexek elengedhetetlenek az E. coli , a Saccharomyces cerevisiae és a magasabb eukarióták életéhez . Bár vannak különbségek az eukarióta, bakteriális és archeális chaperoninek között, az általános szerkezet és mechanizmus megőrződött.
Bakteriofág T4 morfogenezis
A T4 bakteriofág 31 génterméke (gp31) a bakteriofág morfogeneziséhez szükséges fehérje, amely katalitikusan hat , nem pedig beépül a bakteriofág szerkezetébe. Az E. coli baktérium a T4 bakteriofág gazdája. Úgy tűnik, hogy a bakteriofág által kódolt gp31 fehérje homológ az E. coli cochaperonin GroES fehérjével, és képes helyettesíteni a T4 fág virionok összeállításában a fertőzés során. Mint GroES, gp31 stabil komplexet képez a GroEL chaperon, hogy feltétlenül szükséges az összecsukható és összeszerelés in vivo a T4 bakteriofág fő kapszidfehérje gp23.
A fő oka annak, hogy a fágnak szüksége van saját GroES homológjára, az, hogy a gp23 fehérje túl nagy ahhoz, hogy elférjen egy hagyományos GroES ketrecben. A gp31 hosszabb hurokkal rendelkezik, amelyek magasabb tárolót hoznak létre.
Klinikai jelentőség
Emberi GroEL az immundomináns antigén betegek Légiós betegség , és úgy gondolják, hogy szerepet játszik a védelme a Legionella baktériumok oxigén gyökök belül makrofágok . Ez a hipotézis azon a megállapításon alapul, hogy a cpn60 gént felülszabályozzák a hidrogén -peroxid , az oxigéngyök forrása hatására. A Cpn60 -ról azt is kimutatták, hogy számos baktériumfajban erős antigenitást mutat, és potenciálisan immunválaszt válthat ki a nem kapcsolódó bakteriális fertőzések ellen.
Példák
Az ezt a domént tartalmazó fehérjéket kódoló emberi gének a következők:
- BBS10
- CCT1 ; CCT2 ; CCT3 ; CCT4 ; CCT5 ; CCT6A ; CCT6B ; CCT7 ; CCT8
- CESK1
- HSPD1
- KCNMB3L
- CCT8L1 ; LOC401329
- MKKS
- PIP5K3
Lásd még
Megjegyzések
Hivatkozások
Külső linkek
- további részletek ... Archiválva 2011-03-01 a Wayback Machine-nél
- Chaperoninek az amerikai National Library of Medicine orvosi tárgyszórendszere (mm)
- cpnDB: chaperonin adatbázis
- A Chaperonins aktivitásának animációi
- NIH anyag a HSP60 -on
- HSP60 Archiválva 2008-03-16, a Wayback Machine-nél
- HSP60 legyekben
- A Chaperonin honlap
- A fehérje adatbank
- Enzim adatbázis a HSP60 -on
- HSP60 a Pub Med
- HSP60 génjelentés
- HSP60+hősokk+fehérjék az Egyesült Államok Országos Orvostudományi Könyvtárának orvosi tantárgyaiban (MeSH)