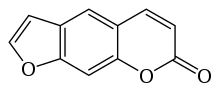
Psoralen - Psoralen
|
|
| Nevek | |
|---|---|
|
Előnyben részesített IUPAC név
7 H -furo [3,2- g ] [1] benzopirán-7-on |
|
| Azonosítók | |
|
3D modell ( JSmol )
|
|
| 152784 | |
| ChEBI | |
| CHEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.000.581 |
| EK -szám | |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
CompTox műszerfal ( EPA )
|
|
|
|
|
|
| Tulajdonságok | |
| C 11 H 6 O 3 | |
| Moláris tömeg | 186,16 g/mol |
| Olvadáspont | 158 - 161 ° C (316 - 322 ° F; 431 - 434 K) |
| Veszélyek | |
| GHS piktogramok |

|
| GHS Jelszó | Figyelem |
| H302 , H315 , H319 , H335 | |
| P261 , P264 , P270 , P271 , P280 , P301+312 , P302+352 , P304+340 , P305+351+338 , P312 , P321 , P330 , P332+313 , P337+313 , P362 , P403+233 , P405 , P501 | |
|
Eltérő rendelkezés hiányában az adatok a szabványos állapotú anyagokra vonatkoznak (25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Infobox hivatkozások | |
A psoralen (más néven psoralene ) az anyavegyület a természetben előforduló szerves vegyületek családjában, amelyeket lineáris furanokumarinoknak neveznek . Szerkezetileg a kumarinhoz kapcsolódik egy kondenzált furángyűrű hozzáadásával , és az umbelliferon származékának tekinthető . A Psoralen természetesen megtalálható a Psoralea corylifolia magjában , valamint a közönséges füge , zeller , petrezselyem , nyugat -indiai szaténfa és minden citrusfélében . Széles körben használják a PUVA (psoralen + UVA ) kezelésében pikkelysömör , ekcéma , vitiligo és bőr T-sejtes limfóma kezelésére ; ezek az alkalmazások jellemzően olyan gyógyszerek használatával, mint a Methoxsalen . Sok furanokumarin rendkívül mérgező a halakra, és néhányat Indonéziában patakokban raknak le halak fogására.
Felhasználások
A Psoralen mutagén , és erre a célra használják a molekuláris biológiai kutatásokban. A psoralen DNS- be interkalálódik , és ultraibolya (UVA) sugárzásnak kitéve monoadduktumokat és kovalens interstrand keresztkötéseket (ICL) képezhet a timinekkel, előnyösen a genom 5'-TpA helyein, apoptózist indukálva . A Psoralen plus UVA (PUVA) terápia alkalmazható hiperproliferatív bőrbetegségek, például pikkelysömör és bizonyos bőrrákok kezelésére . Sajnos maga a PUVA -kezelés magasabb bőrrák kockázathoz vezet.
A psoralen fontos felhasználása a PUVA kezelésében olyan bőrproblémáknál, mint a pikkelysömör, és kisebb mértékben az ekcéma és a vitiligo . Ez kihasználja a psoralen magas UV -abszorbanciáját. A psoralen -t először a bőr érzékenyítésére alkalmazzák, majd UVA -fényt alkalmaznak a bőrprobléma tisztítására. A Psoralen alopecia kezelésére is ajánlott . Psoralenek is használják fotoferézis , ahol össze vannak keverve az extrahált leukociták, mielőtt az UV sugárzást alkalmazunk.
A psoralen fotokarcinogén tulajdonságai ellenére 1996 -ig barnító aktivátorként használták a fényvédőkben. A psoraleneket barnulásgyorsítókban használják, mivel a psoralen növeli a bőr fényérzékenységét. Néhány beteg súlyos bőrvesztést szenvedett a psoralen tartalmú barnító aktivátorokkal való napozás után. A világosabb bőrszínű betegek négyszer annyit szenvednek a psoralének melanoma-generáló tulajdonságaitól, mint a sötétebb bőrűek. A Psoralens rövid távú mellékhatásai közé tartozik a hányinger, hányás, eritéma, viszketés, xerosis, bőrfájdalom a dermális ideg fototoxikus károsodása miatt, és bőr- és nemi szervek bőrének rosszindulatú daganatait okozhatja.
Az optimalizált psoralenek további felhasználása a kórokozók inaktiválása a vérkészítményekben. A szintetikus amino-psoralen, amotosalen HCl a fertőző kórokozók (baktériumok, vírusok, protozoonok) inaktiválására lett kifejlesztve a vérlemezkékben és a plazma vérkomponensekben, amelyeket a betegek transzfúziójának támogatására készítettek. A klinikai alkalmazást megelőzően az amotosalénnel kezelt vérlemezkéket tesztelték, és megállapították, hogy nem karcinogének, amikor a kialakult p53 kiütéses egérmodellt alkalmazták. A technológia jelenleg rutinszerűen használatos bizonyos európai vérközpontokban, és nemrégiben jóváhagyták az Egyesült Államokban.
Kémia
Psoralen interkaiáiódik be a DNS kettős spirál ahol ideális helyzetben, hogy így egy vagy több adduktok szomszédos pirimidin-bázisok, előnyösen timin, gerjesztés hatására ultraibolya foton.
Számos fizikai-kémiai módszert alkalmaztak a psoralen-DNS kölcsönhatások kötési állandóinak levezetésére. Klasszikusan a psoralén és a pufferolt DNS-oldat két kamráját féligáteresztő membrán választja el ; a psoralen DNS -hez való affinitása közvetlenül összefügg a psoralen DNS -kamrában lévő egyensúlyi koncentrációjával. A vízben való oldhatóság két okból fontos: a gyógyszer vérben való oldhatóságának farmakokinetikája és szerves oldószerek (pl. DMSO ) alkalmazása. A psoralen -ek hosszú hullámhosszú UV -fénnyel történő besugárzással is aktiválhatók. Míg az UVA sugárzású fény a klinikai standard, az UVB hatékonyabb a fotoduktumok képzésében, azt sugallja, hogy használata nagyobb hatékonysághoz és rövidebb kezelési időhöz vezethet.
A pszoralének fotokémiailag reakcióképes helyei az alkénszerű szén-szén kettős kötések a furángyűrűben (az öttagú gyűrű) és a pirongyűrű (a hattagú gyűrű). Ha egy pirimidin-bázis szomszédságában megfelelően interkalálódik, egy négyközpontú fényciklus-addíciós reakció két ciklobutil-típusú monoadukt képződéséhez vezethet. Rendszerint a furán oldali monoadduktumok nagyobb arányban képződnek. A furán-monoadduktum képes elnyelni egy második UVA-fotont, ami egy második négyközpontú fényciklus-addícióhoz vezet a molekula pironvégén, és ezáltal diaduktust vagy keresztkötést hoz létre. A piron monoadduktok nem szívódnak fel az UVA tartományba, és így nem képezhetnek keresztkötéseket további UVA besugárzással.
Ennek a vegyületosztálynak egy másik fontos jellemzője, hogy szingulett oxigént képes előállítani , bár ez a folyamat közvetlen versenyben áll az addukt képződésével, és alternatív útja lehet a gerjesztett állapotú energia eloszlatásának.
A psoralen kutatása történelmileg a DNS -sel és az RNS -sel való kölcsönhatásokra összpontosított (különösen az ICL kialakulására). A Psoralenről azonban kimutatták, hogy gátolja az ErbB2 receptor jelátvitelét is, amely bizonyos agresszív típusú emlőrákban túlexpresszálódik. A bergapten szintetikus származéka , az 5- (4-fenoxibutoxi) psoralen ígéretes immunszuppresszánsként, mivel gátolja a specifikus káliumcsatornát . Szerkezete megakadályozza a DNS -be interkalációt, és csak nagyon gyengén termel szingulett oxigént, jelentősen csökkentve a nemkívánatos toxicitást és mutagén hatást in vivo . Ez hatással van a különböző autoimmun betegségek (pl. Szklerózis multiplex , 1-es típusú cukorbetegség és reumatoid artritisz ) kezelésére . Míg a sejtfelszín módosítása és az ioncsatorna-blokkolás két újonnan felfedezett hatásmechanizmus, sok kutatás vár még.
Szerkezet
A legtöbb furokumarin tekinthető származékai vagy pszoralént vagy angelicin . A pszoralént és származékait gyakran lineáris furanokumarinoknak nevezik, így nevezik őket, mivel lineáris kémiai szerkezetük van. Fontos lineáris furokumarin közé xanthotoxin (más néven methoxsalen ) bergaptén , imperatorin és nodakenetin .
A psoralén szerkezetét eredetileg a bomlási reakciók termékeinek azonosításával vonták le. Ez mutatja a szokásos reakciók a lakton kumarin, mint a gyűrű felnyitása a lúggal , így egy kumarin sav vagy kumarinsav származékot. A kálium-permanganát a furángyűrű oxidációját okozza, míg más oxidációs módszerek furán-2,3-karbonsavat termelnek.
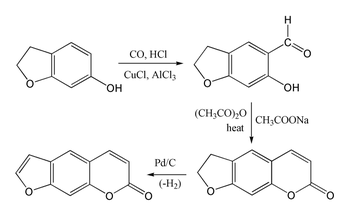
Szintézis
A Psoralen-t nehéz szintetizálni, mert az umbelliferon a 8-as helyzetben szubsztitúción megy keresztül , nem pedig a kívánt 6-os pozíción. A benzofurán inkább a furángyűrűben reagál , mint a benzolgyűrűben . Azonban a 7-hidroxi-származékot 2,3-dihidrobenzofurán (más néven coumaran) nem vetik alá szubsztitúció a kívánt 6-helyzetben, amely lehetővé teszi a következő szintézisét a kumarin-rendszer keresztül Gattermann-Koch-reakció , majd egy Perkin kondenzációs alkalmazásával ecetsavanhidrid . A szintézist ezután az öttagú gyűrű dehidrogénezésével fejezzük be , és így a furángyűrűt állítjuk elő.
Bioszintézis
Pszoralént származik kumarinok a sikimát út; bioszintézisét az alábbi ábra mutatja. A 6 -os aromás gyűrű a hidroxilcsoporttal szembeni orto pozícióban aktiválódik, és 5 -ös alkilezőszerrel alkileződik . A 7. képletű dimetil-allil-csoportot ezután ciklizáljuk a fenolcsoporttal, így kapjuk a 8. Ezt az átalakulást katalizálja egy citokróm P-450-függő monooxigenáz17 (psoralén-5-monooxigenáz), valamint kofaktorok ( NADPH ) és molekuláris oxigén.
A bioszintetikus útvonalat, amelyben a psoralen képződik, az alábbi ábra mutatja. Egy második P -450 -függő monooxigenáz enzim ( psoralen -szintáz ) ezután 10 -et (11 -es formában) lehasít 8 -ról 1 -re. Ez az útvonal nem tartalmaz hidroxilezett köztiterméket, és a hasítást gyökös reakcióval kell elindítani .
Növényi források
A Ficus carica (füge) valószínűleg a legelterjedtebb psoralénforrás. Kis mennyiségben megtalálhatók továbbá az Ammi visnaga (bisnaga), a Pastinaca sativa (paszternák), a Petroselinum crispum ( petrezselyem ), a Levisticum officinale (lovage), a Foeniculum vulgare (gyümölcs, azaz édesköménymag), a Daucus carota (sárgarépa), a Psoralea corylifolia (babchi), Apium graveolens (zeller), bergamott olaj ( bergapten , bergamottin ).
Psoralen DNS adduktumok javítása
PUVA-kezelés egyaránt termel DNS szálak közötti keresztkötések (ICL) és monoadducts. A psoralen által bevezetett ICL -ek erősen genotoxikusak az aktívan replikálódó sejtekre. A kovalens kapcsolat gátolja a replikációs villa előrehaladását. Így az ICL leválasztása szükséges a replikáció folytatása előtt. A javítás kezdeti lépései általában metszéseket tartalmaznak az egyik szülői szálban a térhálósítás mindkét oldalán. Ezt követően a sérülés helyreállítása pontos vagy pontatlan eljárással történhet.
A keresztkötések javításának pontos folyamata a homológ rekombinációs javítás (HRR). Ez magában foglalja a sérült információ cseréjét ugyanazon sejt másik homológ kromoszómájának ép információjának felhasználásával . A HRR-hiányos Escherichia coli sejtek a vad típusú sejtekhez képest nagyon érzékenyek a PUVA-ra. A HRR hatékonynak tűnik. Az E. coli-ban , annak ellenére, hogy egy vagy két javítatlan keresztkötés elegendő a sejt inaktiválásához, a vad típusú sejt képes helyreállítani, és ezért 53-71 psoralen keresztkötést helyreállítani. A Saccharomyces cerevisiae élesztőben a HRR a fő útvonal a psoralen-keresztkötések pontos eltávolítására. A vad típusú élesztőben a HRR által keresztkötéses eltávolítással összefüggő rekombinációs események túlnyomórészt nem kereszteződő génkonverziós események. Úgy tűnik, hogy a vírus DNS -ben lévő psoralen keresztkötéseket rekombinációs javítási eljárással is eltávolítják, ahogy az SV40 vírussal fertőzött sejtekben és a herpes simplex vírussal fertőzött sejtekben is előfordul.
Úgy tűnik, hogy a psoralen keresztkötések javításának egyik pontatlan folyamata DNS -polimerázt használ, hogy kitöltse a szálban kialakult rést a két bemetszéssel. Ez a folyamat pontatlan, mert a komplementer, bemetszetlen szál még mindig megtartja a térhálósodás egy részét, és így nem szolgálhat megfelelő sablonként a pontos javítási szintézishez. A pontatlan javító szintézis mutációt okozhat . A templát DNS -szálában található psoralen monoadduktumok szintén pontatlan replikációs bypass -t (transzleziós szintézist ) okozhatnak , ami mutációhoz vezethet. A T4 fágban a PUVA-kezelés után megfigyelt mutációnövekedésről azt találták, hogy tükrözi a vad típusú DNS-polimeráz transzlézis szintézisét, valószínűleg a hibás leolvasási képesség miatt.
A nukleinsavak szerkezetének elemzése
A psoralenek visszafordíthatóan térhálósíthatják a nukleinsavak kettős hélixét, ezért széles körben alkalmazták mind a DNS, mind az RNS kölcsönhatásainak és szerkezetének elemzésére.
Hivatkozások
További irodalom
- Dean, FM (1963). Természetben előforduló oxigéngyűrű vegyületek . London: Butterworths.
- A Merck -index (7. kiadás). Rahway NJ: Merck. 1960.