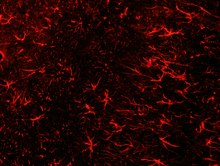
Astrogliosis - Astrogliosis
| Astrogliosis | |
|---|---|
 Reaktív asztrociták kialakulása a központi idegrendszer (CNS) sérülése után
| |
| Anatómiai terminológia |
Az asztrogliózis (más néven asztrocitózis vagy reaktív asztrogliózis ) az asztrociták számának abnormális növekedése a közeli idegsejtek központi idegrendszeri (CNS) traumából , fertőzésből , iszkémiából , stroke -ból , autoimmun válaszokból vagy neurodegeneratív betegségből származó pusztulása miatt . Az egészséges idegszövetben az asztrociták kritikus szerepet játszanak az energiaellátásban, a véráramlás szabályozásában, az extracelluláris folyadék homeosztázisában, az ionok és adók homeosztázisában, a szinapszis működésének szabályozásában és a szinaptikus átalakításban. Az asztrogliózis megváltoztatja az asztrociták molekuláris expresszióját és morfológiáját, például fertőzés hatására, súlyos esetekben gliális hegek kialakulását idézve elő , amelyek gátolhatják az axonregenerációt .
Okoz
A reaktív asztrogliózis az asztrocitákban bekövetkező változások spektruma, amelyek a központi idegrendszeri sérülések és betegségek minden formájára reagálva jelentkeznek. A reaktív asztrogliózis miatti változások a központi idegrendszeri sérülés súlyosságától függően változnak a molekuláris expresszió progresszív változásainak, a progresszív sejtes hipertrófiának , a proliferációnak és a hegek kialakulásának fokozatos folytonossága mentén .
A központi idegrendszer idegsejtjeinek fertőzés, trauma, ischaemia, stroke, ismétlődő rohamok, autoimmun válaszok vagy más neurodegeneratív betegségek által okozott sértése reaktív asztrocitákat okozhat.
Ha az asztrogliózis maga patológiás, a kóros problémára adott normális válasz helyett asztrocitopátiának nevezik .
Funkciók és hatások
A reaktív asztrociták előnyösek vagy károsíthatják a környező idegi és nem idegi sejteket. Számos változáson mennek keresztül, amelyek megváltoztathatják az asztrociták aktivitását az idegvédelemhez és -javításhoz, a gliás hegesedéshez és a központi idegrendszer gyulladásának szabályozásához szükséges funkciók megszerzése vagy elvesztése révén .
Idegvédelem és javítás
A szaporodó reaktív asztrociták kulcsfontosságúak a hegek kialakulásához és működéséhez, csökkentve a gyulladásos sejtek terjedését és perzisztenciáját , fenntartva a vér-agy gát (BBB) helyreállítását, csökkentve a szövetkárosodást és az elváltozás méretét, valamint csökkentve az idegsejtek elvesztését és a demielinizációt.
A reaktív asztrociták glutation -termelés révén védekeznek az oxidatív stressz ellen, és felelősek a központi idegrendszer sejtjeinek NH 4 + toxicitás elleni védelméért . Különféle módszerekkel védik a központi idegrendszeri sejteket és szöveteket, például a potenciálisan excitotoxikus glutamát felvételével , az adenozin felszabadulásával és az amiloid β peptidek lebontásával . A vér -agy gát megszakadásának helyreállítását a reaktív asztrociták is elősegítik, mivel közvetlen végtagjaik (az asztrociták jellemző szerkezete ) kölcsönhatásba lépnek az érfalakkal, amelyek vér -agy gátló tulajdonságokat indukálnak .
Azt is kimutatták, hogy csökkentik a vazogén ödémát trauma, stroke vagy obstruktív hydrocephalus után .
Hegek kialakulása
Szaporodó reaktív hegképző asztrociták következetesen megtalálhatók az egészséges szövetek, valamint a sérült szövetek és gyulladásos sejtek zsebei mentén. Ez általában a gerincvelő és az agy akut traumás sérülésére adott gyors, helyileg kiváltott gyulladásos válasz után fordul elő . Szélsőséges formájában a reaktív asztrogliózis újonnan elszaporodott asztrociták megjelenéséhez és hegek kialakulásához vezethet súlyos szövetkárosodás vagy gyulladás hatására.
A hegképződéshez vezető molekuláris kiváltó tényezők közé tartozik az epidermális növekedési faktor (EGF), a fibroblaszt növekedési faktor (FGF), az endotelin 1 és az adenozin -trifoszfát (ATP). Az érett asztrociták újra beléphetnek a sejtciklusba és szaporodhatnak a hegképződés során. Néhány szaporodó reaktív asztrocita a helyi parenchymában található NG2 progenitor sejtekből származhat ependimális sejt -progenitorokból sérülés vagy stroke után. A szubpendimális szövetekben is vannak multipotens progenitorok, amelyek gliafibrilláris savas fehérjét ( GFAP ) expresszálnak, és utódsejteket hoznak létre, amelyek trauma vagy stroke után a sérülés helyei felé vándorolnak.
A gyulladás szabályozása
A reaktív asztrociták az asztrociták normál működéséhez kapcsolódnak. Az asztrociták részt vesznek a központi idegrendszer gyulladásának komplex szabályozásában, amely valószínűleg kontextustól függ, és amelyet multimodális extra- és intracelluláris jelátviteli események szabályoznak. Képesek különböző típusú, akár gyulladáscsökkentő, akár gyulladáscsökkentő molekulákat előállítani különböző típusú stimulációk hatására. Az asztrociták nagymértékben kölcsönhatásba lépnek a mikrogliákkal, és kulcsszerepet játszanak a központi idegrendszer gyulladásában. A reaktív asztrociták ezután az asztrociták rendellenes működéséhez vezethetnek, és befolyásolhatják azok szabályozását és gyulladásra adott válaszát.
A gyulladáscsökkentő hatásokkal összefüggésben a reaktív hegképző asztrociták segítenek csökkenteni a gyulladásos sejtek terjedését a traumás sérülésekre adott helyi gyulladásos válaszok vagy a perifériásan induló adaptív immunválaszok során. Ami a gyulladást elősegítő potenciált illeti, bizonyos molekulák az asztrocitákban a gyulladás növekedésével járnak a traumás sérülés után.
A sértések utáni korai szakaszban az asztrociták nemcsak a gyulladást aktiválják, hanem erős sejtvándorlási akadályokat is képeznek az idő múlásával. Ezek az akadályok jelzik azokat a területeket, ahol intenzív gyulladásra van szükség, és korlátozzák a gyulladásos sejtek és fertőző ágensek terjedését a közeli egészséges szövetekre. A központi idegrendszeri sérülésekre adott válaszok olyan mechanizmusokat részesítettek előnyben, amelyek megóvják a kis sérüléseket. A gyulladásos sejtek és a fertőző ágensek migrációjának gátlása az axonregeneráció gátlásának véletlen melléktermékéhez vezetett, a sejttípusok közötti migrációs jelek közötti redundancia miatt.
Biológiai mechanizmusok
Az asztrogliózisból eredő változásokat kontextus-specifikus módon szabályozzák specifikus jelzőesemények, amelyek képesek megváltoztatni e változások jellegét és mértékét. Különböző stimulációs feltételek mellett az asztrociták sejtek közötti effektor molekulákat termelhetnek, amelyek megváltoztatják a molekulák expresszióját a sejt szerkezetében, az energia metabolizmusában, az intracelluláris jelátvitelben, valamint a membrán transzporterekben és szivattyúkban. A reaktív asztrociták különböző jelek szerint reagálnak, és befolyásolják az idegsejtek működését. A molekuláris mediátorokat neuronok , mikroglia , oligodendrocita törzssejtek, endothelia , leukociták és más asztrociták szabadítják fel a központi idegrendszer szövetében, válaszul a finom sejtzavaroktól az intenzív szöveti sérülésig terjedő sértésekre. Az ebből eredő hatások a véráramlás szabályozásától az energiaellátáson át a szinaptikus funkcióig és az idegi plaszticitásig terjedhetnek .
Jelző molekulák
Az ismert jelzőmolekulák közül keveset és azok hatásait értjük a különböző sértésekre reagáló reaktív asztrociták összefüggésében.
Az FGF , a TGFB és a ciliáris neurotróf faktor (CNTF) által indukált GFAP -szabályozás a reaktív gliozis klasszikus markere. Az axonregeneráció nem fordul elő olyan területeken, ahol a GFAP és a vimentin emelkedik . Paradox módon a GFAP -termelés növekedése is specifikus a lézió méretének minimalizálására, valamint az autoimmun encephalomyelitis és a stroke kockázatának csökkentésére .
Szállítók és csatornák
Az asztrocita glutamát transzporterek jelenléte a rohamok számának csökkenésével és a neurodegeneráció csökkenésével jár, míg az asztrocita réscsomópont Cx43 fehérje hozzájárul a hipoxia előkezelésének neuroprotektív hatásához . Ezenkívül az AQP4 , egy asztrocita vízcsatorna, döntő szerepet játszik a citotoxikus ödémában és súlyosbítja a stroke utáni kimenetelt .
Neurológiai patológiák
Elvesztése vagy zavara funkciók rendesen a asztrociták vagy reaktív asztrociták a folyamat során a reaktív asztrogliózis megvan a lehetőség a hátterében neurális diszfunkció és patológia különböző körülmények között, beleértve a trauma , sztrók , sclerosis multiplex , és mások. Néhány példa a következő:
- A véredényeket érintő és beburkoló asztrocita végtagok autoimmun pusztulása a központi idegrendszer gyulladásával és a szklerózis multiplex egyik formájával jár együtt
- A Rasmussen -szindróma asztrociták autoantitest -pusztulása görcsöket okoz
- Az Alexander-betegség , a domináns, nyereség-of-function mutáció kódoló gén GFAP társul makro- encephalopathia , görcsrohamok , pszichomotoros zavarok és a korai halál.
- Az amyotróp laterális szklerózis ( ALS ) családi formájában a szuperoxid-diszmutázt (SOD) kódoló gén domináns funkciójavító mutációja a motoros idegsejtekre toxikus molekulák reaktív asztrocitáinak képződéséhez vezet.
A reaktív asztrocitákat specifikus jelző kaszkádok is stimulálhatják, hogy olyan káros hatásokat érjenek el, mint például:
- Súlyosbodása gyulladás keresztül citokin termelés
- Reaktív oxigénfajok neurotoxikus szintjének termelése és felszabadítása
- Potenciálisan excitotoxikus glutamát felszabadulása
- A lehetséges hozzájárulás a rohamok kialakulásához
- A vér-agy gátfunkció veszélyeztetése a vaszkuláris endoteliális növekedési faktor termelés következtében
- Citotoxikus ödéma a trauma és a stroke során az AQP4 túlműködés révén
- Lehetőség van az asztrociták krónikus citokinaktivációjára , amely hozzájárul a krónikus fájdalomhoz
A reaktív asztrociták előidézhetik az idegi toxicitást citotoxikus molekulák, például nitrogén -monoxid gyökök és más reaktív oxigénfajok révén , amelyek károsíthatják a közeli idegsejteket. A reaktív asztrociták elősegíthetik a központi idegrendszeri sérülés utáni másodlagos degenerációt is.
Új terápiás technikák
Az asztrogliózis romboló hatásai miatt, amelyek magukban foglalják a megváltozott molekuláris expressziót, a gyulladásos tényezők felszabadulását, az asztrociták proliferációját és az idegrendszeri diszfunkciót, a kutatók jelenleg új módszereket keresnek az asztrogliózis és a neurodegeneratív betegségek kezelésére. Különböző tanulmányok kimutatták az asztrociták szerepét olyan betegségekben, mint az Alzheimer -kór, az amiotrófiás laterális szklerózis ( ALS ), a Parkinson -kór és a Huntington -kór . A reaktív asztrogliózis okozta gyulladás sok ilyen neurológiai betegséget fokoz. A jelenlegi tanulmányok a reaktív gliózis okozta gyulladás gátlásának lehetséges előnyeit kutatják annak neurotoxikus hatásainak csökkentése érdekében.
A neurotropinokat jelenleg kutatják, mint lehetséges gyógyszereket az idegsejtek védelmére, mivel kimutatták, hogy helyreállítják az idegsejtek működését. Például néhány tanulmány idegnövekedési faktorokat alkalmazott bizonyos kolinerg funkciók visszanyerésére az Alzheimer -kórban szenvedő betegeknél .
A BB14 gliózis elleni funkciója
Az egyik specifikus gyógyszerjelölt a BB14, amely egy ideg növekedési faktorhoz hasonló peptid, amely TrkA agonistaként működik . Kimutatták, hogy a BB14 csökkenti a reaktív asztrogliózist patkányokban a perifériás ideg sérülései miatt, a DRG és a PC12 sejtek differenciálódására hatva. Bár további kutatásokra van szükség, a BB14 számos neurológiai betegség kezelésére képes. A neurotrofinok további kutatása potenciálisan egy nagyon szelektív, erős és kicsi neurotrofin kifejlődéséhez vezethet, amely a reaktív gliozist célozza egyes neurodegeneratív betegségek enyhítésére.
A TGFB szabályozó funkciója
A TGFB egy szabályozó molekula, amely részt vesz a proteoglikán előállításában. Ez a termelés fokozódik bFGF vagy Interleukin 1 jelenlétében . Egy anti-TGFβ antitest potenciálisan csökkentheti a GFAP felszabályozását a központi idegrendszer sérülései után, elősegítve az axonális regenerációt.
Etiidium -bromid kezelés
Az etidium -bromid injekciója elpusztítja az összes központi idegrendszeri gliát ( oligodendrocitákat és asztrocitákat ), de nem hagyja érintetlenül az axonokat, az ereket és a makrofágokat . Ez körülbelül négy napig kedvező környezetet biztosít az axonális regenerációhoz. Négy nap elteltével a központi idegrendszer glia újra behatol az injekció területére, és ennek következtében gátolja az axonális regenerációt. Ez a módszer kimutatták, hogy csökkenti a gliás hegesedést a központi idegrendszeri sérülést követően.
Metalloprotineáz aktivitás
Az oligodendrocita prekurzor sejtek és a C6 glioma sejtek metalloproteinázt termelnek , amelyről kimutatták, hogy inaktiválja a Schwann -sejtek által kiválasztott gátló proteoglikán egy típusát . Következésképpen a megnövekedett metalloproteináz az axonok körüli környezetben megkönnyítheti az axonális regenerációt a gátló molekulák lebomlása révén a fokozott proteolitikus aktivitás miatt.