Citokróm c oxidáz - Cytochrome c oxidase
| Citokróm c oxidáz | |||||||||
|---|---|---|---|---|---|---|---|---|---|
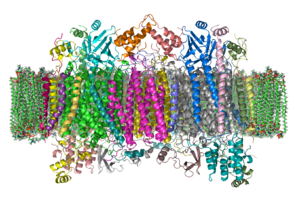 A szarvasmarha citokróm c oxidáz kristályszerkezete egy foszfolipid kettős rétegben. A membránok közötti tér a kép tetején található. Az EKT -ból kiigazítva : 1OCC (ebben a szerkezetben homo dimer)
| |||||||||
| Azonosítók | |||||||||
| EK sz. | 1.9.3.1 | ||||||||
| CAS -szám | 9001-16-5 | ||||||||
| Adatbázisok | |||||||||
| IntEnz | IntEnz nézet | ||||||||
| BRENDA | BRENDA bejegyzés | ||||||||
| ExPASy | NiceZyme kilátás | ||||||||
| KEGG | KEGG bejegyzés | ||||||||
| MetaCyc | anyagcsereút | ||||||||
| PRIAM | profil | ||||||||
| PDB struktúrák | RCSB PDB PDBe PDBsum | ||||||||
| Gén ontológia | AmiGO / QuickGO | ||||||||
| |||||||||
| Citokróm c oxidáz | |
|---|---|

| |
| Azonosítók | |
| Szimbólum | Citokróm c oxidáz |
| OPM szupercsalád | 4 |
| OPM fehérje | 2dyr |
| Membranóm | 257 |
A enzim citokróm c-oxidáz vagy komplex IV , EC 1.9.3.1 , egy nagy transzmembrán fehérje komplex megtalálható baktériumok , archaea , és a mitokondriumok a eukarióták .
Ez az utolsó enzim a légzési elektron transzport lánc a sejtek található a membrán. Mind a négy citokróm c molekulából egy -egy elektronot kap , és átviszi őket egy dioxigénmolekulába, átalakítva a molekuláris oxigént két vízmolekulává. Ebben a folyamatban kötődik négy protonok a belső vizes fázisban, hogy két molekula vizet, és áthelyeződnek a másik négy protonok a membránon keresztül, növelve a transzmembrán különbség proton elektrokémiai potenciál , amely az ATP-szintáz , majd használ szintetizálni ATP .
Szerkezet
A komplexum
A komplex egy nagyméretű, integrált membránfehérje, amely több fém protézishelyből és 14 fehérje alegységből áll emlősökben. Az emlősökben tizenegy alegység nukleáris eredetű, három pedig a mitokondriumokban szintetizálódik. A komplexum tartalmaz két hem molekulákat , egy citokróm egy és citokróm egy 3 , és a két réz központok, a Cu A és Cu B központok. Valójában a citokróm a 3 és a Cu B binukleáris központot képez, amely az oxigén redukciója. A citokróm c , amelyet a légzőlánc előző alkotóeleme (citokróm bc1 komplex, III. Komplex) redukál, a Cu A binukleáris központ közelében dokkol, és átad neki egy elektronot, és újra oxidálódik Fe 3+ tartalmú citokróm c -vé . A redukált Cu A binukleáris központ most továbbít egy elektronot a citokróm a -ba , amely viszont továbbít egy elektronot a citokróm a 3 -Cu B binukleáris központba. A két fémion ebben a binukleáris központban 4,5 Å távolságra van egymástól, és koordinálják a hidroxidionokat teljesen oxidált állapotban.
A citokróm c oxidáz kristálytani vizsgálatai szokatlan transzláció utáni módosulást mutatnak, amely összeköti Tyr (244) C6-ját és His (240) ε-N-jét (szarvasmarha enzimek számozása). Ez alapvető szerepet játszik abban, hogy a citokróm egy 3 - Cu B kétmagvú központ elfogadja négy elektron csökkentésében molekuláris oxigént , hogy a víz . A redukciós mechanizmusról korábban azt gondolták, hogy egy peroxid -köztiterméket tartalmaz, amelyről feltételezték, hogy szuperoxid -termeléshez vezet . A jelenleg elfogadott mechanizmus azonban gyors négyelektronos redukciót foglal magában, azonnali oxigén-oxigén kötés lehasadással, elkerülve minden olyan köztiterméket, amely valószínűleg szuperoxidot képez.
A konzervált alegységek
| Nem. | Az alegység neve | Emberi fehérje | Fehérje leírás az UniProt -tól | Pfam család humán fehérjével |
|---|---|---|---|---|
| 1 | Cox1 | COX1_HUMAN | Citokróm c oxidáz 1. alegység | Pfam PF00115 |
| 2 | Cox2 | COX2_HUMAN | Citokróm c oxidáz 2. alegység | Pfam PF02790 , Pfam PF00116 |
| 3 | Cox3 | COX3_HUMAN | Citokróm c oxidáz alegység 3 | Pfam PF00510 |
| 4 | Cox4i1 | COX41_HUMAN | Citokróm c oxidáz 4. alegység 1. izoforma, mitokondriális | Pfam PF02936 |
| 5 | Cox4a2 | COX42_HUMAN | Citokróm c oxidáz 4. alegység 2. izoforma, mitokondriális | Pfam PF02936 |
| 6 | Cox5a | COX5A_HUMAN | Citokróm c oxidáz 5A alegység, mitokondriális | Pfam PF02284 |
| 7 | Cox5b | COX5B_HUMAN | Citokróm c oxidáz 5B alegység, mitokondriális | Pfam PF01215 |
| 8 | Cox6a1 | CX6A1_HUMAN | Citokróm c oxidáz 6A1 alegység, mitokondriális | Pfam PF02046 |
| 9 | Cox6a2 | CX6A2_HUMAN | Citokróm c oxidáz 6A2 alegység, mitokondriális | Pfam PF02046 |
| 10 | Cox6b1 | CX6B1_HUMAN | Citokróm c oxidáz 6B1 alegység | Pfam PF02297 |
| 11 | Cox6b2 | CX6B2_HUMAN | Citokróm c oxidáz 6B2 alegység | Pfam PF02297 |
| 12 | Cox6c | COX6C_HUMAN | Citokróm c oxidáz 6C alegység | Pfam PF02937 |
| 13 | Cox7a1 | CX7A1_HUMAN | Citokróm c oxidáz 7A1 alegység, mitokondriális | Pfam PF02238 |
| 14 | Cox7a2 | CX7A2_HUMAN | Citokróm c oxidáz 7A2 alegység, mitokondriális | Pfam PF02238 |
| 15 | Cox7a3 | COX7S_HUMAN | Feltételezett citokróm c oxidáz 7A3 alegység, mitokondriális | Pfam PF02238 |
| 16 | Cox7b | COX7B_HUMAN | Citokróm c oxidáz 7B alegység, mitokondriális | Pfam PF05392 |
| 17 | Cox7c | COX7C_HUMAN | Citokróm c oxidáz 7C alegység, mitokondriális | Pfam PF02935 |
| 18 | Cox7r | COX7R_HUMAN | Citokróm c oxidáz 7A alegységhez kapcsolódó fehérje, mitokondriális | Pfam PF02238 |
| 19 | Cox8a | COX8A_HUMAN | Citokróm c oxidáz alegység 8A, mitokondriális P | Pfam PF02285 |
| 20 | Cox8c | COX8C_HUMAN | Citokróm c oxidáz 8C alegység, mitokondriális | Pfam PF02285 |
| Gyülekezeti alegységek | ||||
| 1 | Coa1 | COA1_HUMAN | Citokróm c oxidáz összeállítási faktor 1 homológ | Pfam PF08695 |
| 2 | Coa3 | COA3_HUMAN | Citokróm c oxidáz összeállítási 3. faktor homológ, mitokondriális | Pfam PF09813 |
| 3 | Coa4 | COA4_HUMAN | Citokróm c oxidáz összeállítási 4. faktor homológ, mitokondriális | Pfam PF06747 |
| 4 | Coa5 | COA5_HUMAN | Citokróm c oxidáz összeállítási tényező 5 | Pfam PF10203 |
| 5 | Coa6 | COA6_HUMAN | Citokróm c oxidáz összeállítási faktor 6 homológ | Pfam PF02297 |
| 6 | Coa7 | COA7_HUMAN | Citokróm c oxidáz összeállítási tényező 7, | Pfam PF08238 |
| 7 | Cox11 | COX11_HUMAN | Citokróm c oxidáz összeszerelő fehérje COX11 mitokondriális | Pfam PF04442 |
| 8 | Cox14 | COX14_HUMAN | Citokróm c oxidáz összeszerelő fehérje | Pfam PF14880 |
| 9 | Cox15 | COX15_HUMAN | Citokróm c oxidáz összeszerelő fehérje COX15 homológ | Pfam PF02628 |
| 10 | Cox16 | COX16_HUMAN | Citokróm c oxidáz összeszerelő fehérje COX16 homológ mitokondriális | Pfam PF14138 |
| 11 | Cox17 | COX17_HUMAN | Citokróm c oxidáz réz chaperone | Pfam PF05051 |
| 12 | Cox18 | COX18_HUMAN | Mitokondriális belső membránfehérje (citokróm c oxidáz összeszerelő fehérje 18) | Pfam PF02096 |
| 13 | Cox19 | COX19_HUMAN | Citokróm c oxidáz összeszerelő fehérje | Pfam PF06747 |
| 14 | Cox20 | COX20_HUMAN | Citokróm c oxidáz fehérje 20 homológ | Pfam PF12597 |
Összeszerelés
A COX összeszerelése az élesztőben egy összetett folyamat, amely nem teljesen érthető a holoenzim -komplexet alkotó hidrofób alegységek gyors és visszafordíthatatlan aggregációja, valamint a mutáns alegységek és a hidrofób foltok együttesének köszönhetően. A COX alegységek mind a nukleáris, mind a mitokondriális genomban vannak kódolva. A COX katalitikus magot alkotó három alegységet a mitokondriális genom kódolja.
A heemeket és a kofaktorokat az I és II alegységekbe illesztjük. A két hem -molekula az I. alegységben található, segítve a szállítást a II. Alegységbe, ahol két rézmolekula segíti az elektronok folyamatos átvitelét. Az I. és IV alegység kezdeményezi az összeszerelést. Különböző alegységek társulhatnak alkomplex köztitermékekhez, amelyek később más alegységekhez kötődve COX-komplexet képeznek. Az összeszerelés utáni módosítások során a COX homodimert képez. Ez szükséges a tevékenységhez. Mindkét dimert egy kardiolipin molekula köti össze , amelyről kiderült, hogy kulcsszerepet játszik a holoenzim komplex stabilizálásában. A VIIa és III alegységek disszociációja a kardiolipin eltávolításával együtt az enzimaktivitás teljes elvesztését eredményezi. Ismert, hogy a nukleáris genomban kódolt alegységek szerepet játszanak az enzim dimerizációjában és stabilitásában. Ezeknek az alegységeknek a mutációi megszüntetik a COX funkciót.
Ismeretes, hogy az összeszerelés legalább három különböző sebesség meghatározó lépésben történik. Ezeknek a lépéseknek a termékeit megtaláltuk, bár konkrét alegység -összetételeket nem határoztak meg.
A COX I., II. És III. Alegységek szintézisét és összeszerelését transzlációs aktivátorok segítik, amelyek kölcsönhatásba lépnek a mitokondriális mRNS -átiratok 5 'nem lefordított régióival. A transzlációs aktivátorok a sejtmagban vannak kódolva. Működhetnek akár közvetlen, akár közvetett kölcsönhatásban a fordítógép más alkotóelemeivel, de a pontos molekuláris mechanizmusok nem tisztázottak a transzlációs gépek in vitro szintetizálásával kapcsolatos nehézségek miatt. Bár a mitokondriális genomban kódolt I., II. És III. Alegységek közötti kölcsönhatások kisebb mértékben járulnak hozzá az enzim stabilitásához, mint a bigenomikus alegységek közötti kölcsönhatások, ezek az alegységek konzerváltabbak, jelezve az enzimaktivitás lehetséges feltáratlan szerepét.
Biokémia
Összefoglaló reakció:
- 4 Fe 2+ -citokróm c + 4 H + be + O 2 → 4 Fe 3+ -citokróm c + 2 H 2 O + 4 H + kimenet
Két elektronok jutnak el két citokróm c-k, a Cu A és a citokróm-A helyek a citokróm egy 3 - Cu B kétmagvú, így az fémek a Fe 2+ formájában és Cu + . A hidroxid ligandum protonálódik és vízként veszik el, üreget teremtve a fémek között, amelyet O 2 tölt be . Az oxigén gyorsan redukálódik, két elektron érkezik a Fe 2+ citokróm a 3 -ból, amely ferry -oxo formává alakul (Fe 4+ = O). A Cu B -hez közeli oxigénatom felvesz egy elektronot a Cu + -ból , és egy másik elektronot és egy protont a Tyr (244) hidroxilcsoportjából , amely tirozilgyökké válik. A második oxigént két elektron és egy proton felvételével hidroxidionná alakítják át. Egy harmadik elektron eredő más citokróm c átvezetjük az első két elektron-hordozóként a citokróm egy 3 - Cu B kétmagvú Center, és ez elektron és két proton átalakítani a tirozil-csoport vissza Tyr, és a hidroxid kötött Cu B 2+ egy vízmolekulához. A negyedik elektron másik citokróm c átfolyik Cu A és a citokróm egy a citokróm egy 3 - Cu B kétmagvú, így az Fe 4+ = O, hogy Fe 3+ , az oxigénatommal felvett egy proton egyidejűleg, regeneráló Ez az oxigén hidroxidionként, amely a citokróm a 3 - Cu B középpontjában koordinálódott, mint a ciklus elején. A nettó eljárás szerint négy redukált citokróm c -t használnak, 4 protonnal együtt, hogy az O 2 -t két vízmolekulává redukálják .
Gátlás
A COX három konformációs állapotban létezik: teljesen oxidált (pulzáló), részben redukált és teljesen redukált. Minden inhibitor nagy affinitással rendelkezik egy másik állapothoz. Pulzáló állapotban mind a a 3 , mind a Cu B nukleáris centrumok oxidálódnak; ez a legnagyobb aktivitású enzim konformációja. A kételektronos redukció konformációs változást indít el, amely lehetővé teszi az oxigén kötődését az aktív helyen a részben redukált enzimhez. Négy elektron kötődik a COX -hoz, hogy teljes mértékben csökkentse az enzimet. Teljesen redukált állapota, amely a citokróm a 3 hem csoportban lévő redukált Fe 2+ -ból és egy csökkent Cu B + binukleáris központból áll, az enzim inaktív vagy nyugalmi állapotának tekinthető.
A cianid , azid és a szén -monoxid mind a citokróm c oxidázhoz kötődik, gátolja a fehérje működését, és a sejtek kémiai fulladásához vezet. Magasabb molekuláris oxigénkoncentrációra van szükség a növekvő inhibitor koncentrációk kompenzálására, ami a metabolikus aktivitás teljes csökkenéséhez vezet a sejtben inhibitor jelenlétében. Más ligandumok, például a nitrogén -monoxid és a hidrogén -szulfid is gátolhatják a COX -t azáltal, hogy kötődnek az enzim szabályozó helyeihez, csökkentve a sejtlégzés sebességét.
A cianid nem versenyképes COX-inhibitor, nagy affinitással kötődik az enzim részben csökkent állapotához, és gátolja az enzim további redukcióját. Pulzáló állapotban a cianid lassan, de nagy affinitással kötődik. A ligandum feltételezi, hogy egyszerre elektrosztatikusan stabilizálja mindkét fémet azáltal, hogy közéjük helyezi magát. A magas nitrogén -monoxid -koncentráció, például az enzimhez exogén módon hozzáadott, megfordítja a COX cianid gátlását.
A salétrom -oxid reverzibilisen kötődhet a binukleáris központ bármelyik fémionjához, hogy nitrité oxidálódjon. NO és CN - az oxigénnel versenyezve kötődnek a helyszínen, csökkentve a sejtlégzés sebességét. Az endogén NO azonban, amely előállított alacsonyabb szinten, gyarapítja CN - gátlás. A magasabb NO -szint, amely összefüggésben áll azzal, hogy több enzim van redukált állapotban, a cianid nagyobb gátlásához vezet. Ezeknél az alapkoncentrációknál ismert, hogy a IV komplex NO gátlásának jótékony hatásai vannak, például növeli az erek szöveteinek oxigénszintjét. Az enzim képtelensége az oxigén vízre redukálására oxigén felhalmozódását eredményezi, amely mélyebben diffundálhat a környező szövetekbe. A IV komplex NO gátlása nagyobb hatást fejt ki alacsonyabb oxigénkoncentráció esetén, növelve annak értelemben vett értágító alkalmazhatóságát a rászoruló szövetekben.
A hidrogén -szulfid , a szén -monoxidhoz hasonlóan, nem versenyképes módon megköti a COX -t az enzim szabályozó helyén. A szulfid a legnagyobb affinitással rendelkezik az enzim pulzáló vagy részben redukált állapotaihoz, és képes az enzim részleges redukciójára a 3 -as heme központjában. Nem világos, hogy az endogén H 2 S szint elegendő -e az enzim gátlásához. Nincs kölcsönhatás a hidrogén -szulfid és a COX teljesen csökkent konformációja között.
Metanol a metilezett szesz alakítjuk hangyasav , amely szintén gátolja azonos oxidáz rendszert. A magas ATP szint alloszterikusan gátolhatja a citokróm c oxidázt, amely a mitokondriális mátrixon belül kötődik.
Extramitochondriális és szubcelluláris lokalizációk
A citokróm c oxidáz 3 alegységek által kódolt mitokondriális DNS (citokróm c oxidáz alegység I , A alegységet II , és alegység III ). Ebből a 3 alegységből, amelyeket mitokondriális DNS kódol, kettőt az extramitochondriális helyeken azonosítottak. A hasnyálmirigy acináris szövetében ezeket az alegységeket zimogén granulátumokban találták . Ezenkívül az agyalapi mirigy elülső részében ezeknek az alegységeknek viszonylag nagy mennyiségét találtuk növekedési hormon szekréciós granulátumokban. Ezen citokróm c oxidáz alegységek extramitochondriális funkcióját még nem jellemezték. A citokróm c oxidáz alegységeken kívül számos más mitokondriális fehérje esetében is megfigyeltek extramitochondriális lokalizációt. Ez felveti annak lehetőségét, hogy léteznek még azonosítatlan specifikus mechanizmusok a fehérjék transzlokációjához a mitokondriumokból más sejthelyekre.
Genetikai rendellenességek és rendellenességek
A citokróm c oxidáz (COX) működését vagy szerkezetét megváltoztató genetikai mutációkkal járó hibák súlyos, gyakran halálos anyagcserezavarokhoz vezethetnek . Az ilyen rendellenességek általában kora gyermekkorban jelentkeznek, és túlnyomórészt a nagy energiaigényű szöveteket (agy, szív, izom) érintik. A sok minősített mitokondriális betegség közül a diszfunkcionális COX összeszerelést érintő betegségeket tartják a legsúlyosabbnak.
A COX rendellenességek túlnyomó része a nukleáris kódolású fehérjék mutációihoz kapcsolódik, amelyeket összeszerelési faktoroknak vagy összeszerelő fehérjéknek neveznek. Ezek az összeszerelési tényezők hozzájárulnak a COX szerkezetéhez és működéséhez, és számos alapvető folyamatban vesznek részt, beleértve a mitokondriumok által kódolt alegységek átírását és transzlációját, az előproteinek feldolgozását és a membrán behelyezését, valamint a kofaktorok bioszintézisét és beépülését.
Jelenleg hét COX összeállítási faktorban mutációkat azonosítottak: SURF1 , SCO1 , SCO2 , COX10 , COX15 , COX20 , COA5 és LRPPRC . Ezeknek a fehérjéknek a mutációi az alkomplex összeszerelés, a rézszállítás vagy a transzlációs szabályozás megváltozott funkcionalitását eredményezhetik. Minden génmutáció egy adott betegség etiológiájához kapcsolódik, némelyiknek több rendellenességre van hatása. A COX összeszerelését génmutációkon keresztül érintő rendellenességek közé tartozik a Leigh -szindróma , a cardiomyopathia , a leukodystrophia , a vérszegénység és a szenzineurális süketség .
Hisztokémia
A neuronok fokozott függése az oxidatív foszforilációtól energiához megkönnyíti a COX hisztokémia alkalmazását az állatok regionális agyi anyagcseréjének feltérképezésében, mivel közvetlen és pozitív összefüggést hoz létre az enzimaktivitás és a neuronális aktivitás között. Ez látható a COX enzim mennyiségének és aktivitásának összefüggésében, ami a COX génexpressziós szinten történő szabályozását jelzi. A COX eloszlás inkonzisztens az állati agy különböző régióiban, de eloszlási mintája állatok között konzisztens. Ezt a mintát a majom, egér és borjú agyában figyelték meg. Az agy hisztokémiai elemzésében következetesen kimutatták a COX egyik izozimját.
Ilyen agyi feltérképezést végeztek kisagyi betegségben szenvedő, spontán mutáns egerekben, mint például a reeler és az Alzheimer -kór transzgenikus modellje . Ezt a technikát alkalmazták az állati agyban végzett tanulási tevékenység feltérképezésére is.
További képek
Lásd még
Hivatkozások
Külső linkek
- A citokróm -oxidáz honlapja a Rice Egyetemen
- A citokróm c oxidáz interaktív molekuláris modellje ( MDL csipogó szükséges )
- A fehérjék UMich orientációja membráncsaládokban /szupercsalád-4
- Citokróm-c+oxidáz az Egyesült Államok Országos Orvostudományi Könyvtárának orvosi tantárgyaiban (MeSH)



