Hasnyálmirigy -szigetek - Pancreatic islets
| Hasnyálmirigy -szigetek/ langerhans -szigetek | |
|---|---|
 A hasnyálmirigy -szigetek a hasnyálmirigyben található sejtek csoportjai, amelyek hormonokat szabadítanak fel
| |
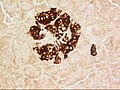
 Hasnyálmirigy -szigetek egérből, tipikus helyzetben, közel az erekhez; inzulin piros, magjai kék színűek.
| |
| Részletek | |
| Része | Hasnyálmirigy |
| Rendszer | Endokrin |
| Azonosítók | |
| latin | insulae pancreaticae |
| Háló | D007515 |
| TA98 | A05.9.01.019 |
| TA2 | 3128 |
| FMA | 16016 |
|
A mikroanatómia anatómiai feltételei | |
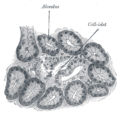
A hasnyálmirigy-szigetek vagy Langerhans-szigetek a hasnyálmirigy azon régiói, amelyek tartalmazzák az endokrin (hormontermelő) sejtjeit, amelyeket 1869-ben Paul Langerhans német patológiás anatómus fedezett fel . A hasnyálmirigy -szigetek a hasnyálmirigy térfogatának 1-2% -át teszik ki, és véráramának 10-15% -át kapják. A hasnyálmirigy -szigetek az emberi hasnyálmirigyben sűrű útvonalakon helyezkednek el, és fontosak a glükóz metabolizmusában .
Szerkezet
Körülbelül 1 millió szigetecske található sűrű útvonalak formájában az egészséges felnőtt ember hasnyálmirigyében, és mindegyik átlagosan körülbelül 0,2 mm átmérőjű. : 928 Mindegyiket elválasztja a környező hasnyálmirigy -szövetektől egy vékony rostos kötőszövet -kapszula, amely folytonos a hasnyálmirigy többi részében átszőtt rostos kötőszövetekkel. : 928
Mikroanatómia
A hasnyálmirigy -szigeteken termelt hormonokat (legalább) ötféle sejt választja ki közvetlenül a véráramba. Patkányszigeteken az endokrin sejttípusok a következőképpen oszlanak meg:
- Alpha sejteket termelő glukagon (20% a teljes sziget-sejtek)
- Béta-sejtek előállítására inzulin és amilin (≈70%)
- Delta sejteket termelő szomatosztatin (<10%)
- Epsilon sejteket termelő ghrelin (<1%)
- Hasnyálmirigy -polipeptidet termelő PP -sejtek (gamma- vagy F -sejtek) (<5%)
Felismerték, hogy a hasnyálmirigy -szigetek citoarchitektúrája fajonként eltérő. Különösen, míg a rágcsáló szigetekre jellemző, hogy az inzulint termelő béta-sejtek túlnyomó része a klaszter magjában van, és a periférián kevés alfa-, delta- és PP-sejt található, az emberi szigeteken az alfa- és béta-sejtek szoros kapcsolatban állnak egymással az egész klaszterben.
A béta -sejtek aránya a szigeteken fajtól függően változik, emberben körülbelül 40-50%. Az endokrin sejteken kívül vannak stromasejtek (fibroblasztok), vaszkuláris sejtek (endoteliális sejtek, periciták), immunsejtek (granulociták, limfociták, makrofágok, dendritikus sejtek) és idegsejtek.
Nagy mennyiségű vér áramlik át a szigeteken, 5-6 ml/perc per 1 g szigetecske. Akár 15 -ször több, mint a hasnyálmirigy exokrin szövetében.
A szigetek parakrin és autokrin kommunikáción keresztül befolyásolhatják egymást , és a béta -sejtek elektromosan kapcsolódnak hat -hét másik béta -sejthez, de más sejttípusokhoz nem.
Funkció
A hasnyálmirigy -szigetek parakrin visszacsatolási rendszere a következő felépítésű:
- Glükóz/inzulin: aktiválja a béta -sejteket és gátolja az alfa -sejteket
- Glikogén/glukagon: aktiválja az alfa -sejteket, amelyek aktiválják a béta- és delta -sejteket
- Szomatosztatin: gátolja az alfa- és a béta -sejteket
Számos G-fehérjéhez kapcsolt receptor (GPCR) szabályozza az inzulin, a glukagon és a szomatosztatin szekrécióját a hasnyálmirigy-szigetekről, és ezen GPCR-ek egy része a 2-es típusú cukorbetegség kezelésére használt gyógyszerek célpontja (ref GLP-1 receptor agonisták, DPPIV inhibitorok).
Elektromos tevékenység
A hasnyálmirigy -szigetek elektromos aktivitását patch clamp technikákkal vizsgálták . Kiderült, hogy a sejtek viselkedése ép szigeteken jelentősen eltér a diszpergált sejtek viselkedésétől.
Klinikai jelentőség
Cukorbetegség
A hasnyálmirigy -szigetek béta -sejtjei inzulint választanak ki , és így jelentős szerepet játszanak a cukorbetegségben . Úgy gondolják, hogy az immunrendszer megsemmisíti őket. Vannak azonban arra utaló jelek is, hogy a béta-sejtek nem pusztultak el, hanem csak működésképtelenné váltak.
Átültetés
Mivel a hasnyálmirigy -szigetek béta -sejtjeit szelektíven elpusztítja az 1 -es típusú cukorbetegség autoimmun folyamata , az orvosok és a kutatók aktívan folytatják a szigetek transzplantációját a fiziológiai béta -sejtműködés helyreállításának eszközeként, amely alternatívát kínálna a teljes hasnyálmirigy -transzplantáció vagy mesterséges hasnyálmirigy . A szigettranszplantáció a hetvenes évek elején vált életképes lehetőségnek a cukorbetegséget igénylő inzulin kezelésében, és a következő három évtizedben folyamatosan fejlődött. A közelmúltbeli klinikai vizsgálatok kimutatták, hogy az inzulinfüggetlenség és a jobb anyagcsere -szabályozás reprodukálható módon érhető el a kadaverikus donorszigetek átültetése után instabil 1 -es típusú cukorbetegségben szenvedő betegekbe .
A magas testtömeg -indexű (BMI) emberek alkalmatlan hasnyálmirigy -donorok a transzplantáció során fellépő nagyobb technikai komplikációk miatt. Lehetséges azonban nagyobb szigetek elkülönítése a nagyobb hasnyálmirigy miatt, és ezért alkalmasabbak a szigetek donorjaira.
A sziget -transzplantáció csak a béta -sejtekből álló szövet átvitelét jelenti, amelyek e betegség kezeléséhez szükségesek. Ez tehát előnyt jelent a teljes hasnyálmirigy -transzplantációval szemben, amely technikailag nagyobb igényeket támaszt, és veszélyt jelent például a hasnyálmirigy -gyulladásra, amely szervvesztéshez vezet. További előny, hogy a betegek nem igényelnek általános érzéstelenítést.
Az 1 -es típusú cukorbetegség esetében a szigetecskék átültetése jelenleg erőteljes immunszuppressziót igényel, hogy megelőzze a gazdaszervezet donor szigetek elutasítását .
A szigeteket átültetik egy portális vénába , amelyet ezután a májba ültetnek. Fennáll a portális vénás ág trombózisának kockázata és a szigetek túlélésének alacsony értéke néhány perccel a transzplantáció után, mivel ezen a helyen az érrendszeri sűrűség a műtét után néhány hónappal alacsonyabb, mint az endogén szigeteken. Így a neovaszkularizáció kulcsfontosságú a szigetek túlélésében, amelyet például a szigetek és vaszkuláris endotélsejtek által termelt VEGF támogat. Az intraportális transzplantációnak azonban vannak más hiányosságai is, ezért más alternatív helyeket is vizsgálnak, amelyek jobb mikrokörnyezetet biztosítanak a szigetek beültetéséhez. A szigettranszplantációs kutatások középpontjában a szigetek beágyazódása, a CNI-mentes (kalcineurin-inhibitor) immunszuppresszió, a szigetek károsodásának biomarkerei vagy a szigetsejtek hiánya is áll.
A béta-sejtek alternatív forrása, például a felnőtt őssejtekből vagy progenitor sejtekből származó inzulintermelő sejtek hozzájárulnának a transzplantációs donorszervek hiányának leküzdéséhez. A regeneratív orvoslás területe rohamosan fejlődik, és nagy reményt ad a közeljövőre. Az 1 -es típusú cukorbetegség azonban a hasnyálmirigy béta -sejtjeinek autoimmun pusztulásának eredménye. Ezért a hatékony gyógyításhoz szekvenciális, integrált megközelítésre van szükség, amely kombinálja a megfelelő és biztonságos immunbeavatkozásokat a béta -sejtek regeneráló megközelítésével. Azt is kimutatták, hogy az alfa -sejtek spontán módon megváltoztathatják a sorsot, és béta -sejtekké differenciálódhatnak mind az egészséges, mind a cukorbeteg emberi és egér hasnyálmirigy -szigeteken, amelyek a béta -sejtek regenerációjának lehetséges jövőbeli forrásai. Valójában azt találták, hogy a szigetek morfológiája és az endokrin differenciálódása közvetlenül összefügg. Az endokrin őssejtek differenciálódnak, ha kohézióban vándorolnak, és rügyszerű szigetek-prekurzorokat vagy "félszigeteket" képeznek, amelyekben az alfa-sejtek alkotják a félsziget külső rétegét, és később béta-sejtek képződnek alattuk.
További képek
Szerkezeti különbségek a patkányszigetek (felül) és az emberi szigetek (alul), valamint a hasnyálmirigy hasi része (bal) és a hátsó része (jobb) között . A különböző sejttípusok színkóddal vannak ellátva. A rágcsáló szigetek, az emberekkel ellentétben, a jellegzetes inzulinmagot mutatják .
Lásd még
- Betatrophin
- Neuroendokrin tumor
- Hasnyálmirigy neuroendokrin tumor
- Sodródva csak le a Langerhans-szigetek , a kisregény a Harlan Ellison