Pretomanid - Pretomanid
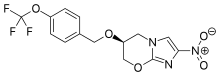 | |
| Klinikai adatok | |
|---|---|
| Kereskedelmi nevek | Dovprela |
| Más nevek | PA-824 |
| AHFS / Drugs.com | Monográfia |
| MedlinePlus | a619056 |
| Licenc adatok | |
| Utak ügyintézés |
Szájjal |
| ATC kód | |
| Jogi státusz | |
| Jogi státusz | |
| Azonosítók | |
| |
| CAS szám | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| CompTox műszerfal ( EPA ) | |
| Kémiai és fizikai adatok | |
| Képlet | C 14 H 12 F 3 N 3 O 5 |
| Moláris tömeg | 359,261 g · mol −1 |
| 3D modell ( JSmol ) | |
| |
| |
A pretomanid egy antibiotikum, amelyet a tüdőt érintő, multirezisztens tuberkulózis kezelésére használnak . Általában bedakilinnel és linezoliddal együtt alkalmazzák . Szájon át szedik .
A leggyakoribb mellékhatások közé tartoznak az idegkárosodások , pattanások , hányás, fejfájás, alacsony vércukorszint , hasmenés és májgyulladás . A gyógyszerek nitroimidazol csoportjába tartozik.
A pretomanidot 2019 augusztusában engedélyezték orvosi felhasználásra az Egyesült Államokban, 2020 júliusában pedig az Európai Unióban. A pretomanidot a TB Alliance fejlesztette ki . Az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hivatala (FDA) első osztályú gyógyszernek tartja .
Orvosi felhasználás
A pretomanid felnőtteknél bedakvilinnel és linezoliddal kombinációban javallt a tüdőben széleskörűen gyógyszerrezisztens (XDR), vagy kezelés-intoleráns vagy nem reagáló multirezisztens (MDR) tuberkulózis (TB) kezelésére.
Történelem
A pretomanid az új, korábban PA-824 nevű antibakteriális gyógyszervegyület általános, nem védett neve. A pretomanidot "Pa" -nak nevezik az adagolás rövidítéseiben, például a BPaL-ben. A vegyület nevének "preto" előtagja tiszteli a dél-afrikai Pretoriát, a TB Alliance klinikai fejlesztési irodájának otthont, ahol a gyógyszer fejlesztésének nagy része végbement. A "manid" utótag hasonló vegyi szerkezetű vegyületek csoportosítására szolgál. Ezt a gyógyszercsoportot különféle nevezzük nitroimidazoloknak , nitroimidazooxazineknek vagy nitroimidazopiránoknak. Ennek a vegyületnek a kifejlesztését azért kezdeményezték, mert sürgős szükség van új, antibakteriális gyógyszerekre, amelyek hatékonyak a rezisztens tuberkulózis törzsek ellen. Ezenkívül a jelenlegi TBC-ellenes gyógyszerek főleg a replikálódó és metabolikusan aktív baktériumok ellen hatékonyak, szükségessé teszik a tartósan vagy látensen jelentkező bakteriális fertőzések ellen hatékony gyógyszereket, amelyek gyakran előfordulnak a tuberkulózisban szenvedő betegeknél.
Felfedezés és preklinikai fejlesztés
A pretomanidot először 2000-ben azonosították a PathoGenesis (ma a Novartis leányvállalata) szintetizált és antituberkuláris aktivitására tesztelt 100 nitroimidazopirán-származék sorozatában. Fontos, hogy a pretomanid olyan statikus M. tuberculosis izolátumok ellen hat , amelyek anaerob körülmények között túlélnek, és a baktericid aktivitás összehasonlítható a meglévő metronidazol gyógyszerével . A pretomanid metabolikus aktiválást igényel a Mycobacterium által az antibakteriális aktivitáshoz. A pretomanid nem volt a leghatásosabb vegyület a M. tuberculosis tenyészeteivel szembeni sorozatban , de orális beadás után a legaktívabb a fertőzött egerekben. Az orális pretomanid biztonságosan tolerálható dózisokban, legfeljebb 28 napig, aktív volt a tuberkulózis ellen egerekben és tengerimalacokban.
Korlátozott FDA jóváhagyás
Az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hivatala (FDA) csak a bedakvilinnel és linezoliddal kombinálva engedélyezte a pretomanid kezelését olyan felnőttek korlátozott és specifikus populációjának kezelésében, akiknél extenzíven gyógyszer-rezisztens , kezelés-intoleráns vagy nem reagál multidrug-rezisztens tüdő-tuberkulózis. A pretomanidot a Limited Population Pathway (LPAD) útján engedélyezték antibakteriális és gombaellenes gyógyszerek esetében. Az LPAD Pathway-t a kongresszus hozta létre a 21. századi kúrákról szóló törvény alapján, hogy felgyorsítsa az antibakteriális és gombaellenes gyógyszerek kifejlesztését és jóváhagyását súlyos vagy életveszélyes fertőzések kezelésére kielégítetlen szükségletű betegek korlátozott populációjában. A pretomanid csak a harmadik tuberkulózis elleni gyógyszer, amely több mint 40 év alatt megkapta az FDA jóváhagyását.
Az FDA megadta a Pretomanid prioritási felülvizsgálatot és a ritka betegségek gyógyszereinek megnevezését. Az FDA megadta a globális szövetségnek a TB Drug Development ( TB Alliance ) számára a Pretomanid jóváhagyását és a trópusi betegségek kiemelt felülvizsgálati utalványát.
Hivatkozások
Külső linkek
- "Pretomanid" . Kábítószer-információs portál . Amerikai Országos Orvostudományi Könyvtár.
