Elektronszállító lánc - Electron transport chain

A elektrontranszport lánc ( ETC; légzési lánc ) egy sor protein komplexek , hogy transzfer elektronok a elektron donorok , hogy elektron befogadására keresztül redox reakciók (mind redukciós és oxidációs egyszerre előforduló ), és csatlakoztatja ezt elektrontranszfer az átutalást a protonok (H + ionok ) egy membránon keresztül . Az elektronszállító lánc peptidekből , enzimekből és más molekulákból épül fel .
Az elektronok áramlása az elektronszállító láncon exergonikus folyamat . A redox reakciókból származó energia elektrokémiai protongradienst hoz létre, amely hajtja az adenozin -trifoszfát (ATP) szintézisét . Az aerob légzés során az elektronok áramlása véget ér, és a molekuláris oxigén a végső elektronakceptor. Az anaerob légzés során más elektronakceptorokat használnak, például szulfátot .
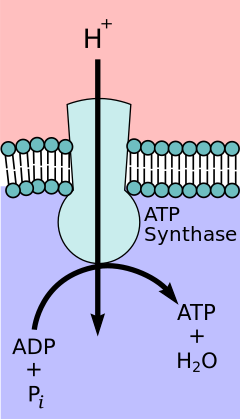
Az elektronszállító láncban a redoxreakciókat a reagensek és termékek Gibbs -mentes energiájának különbsége vezérli . A Gibbs -mentes energia a redox -potenciálnak nevezett mennyiséghez köthető. Az elektronszállító lánc komplexei legyűjtik azoknak a redoxreakcióknak az energiáját, amelyek akkor fordulnak elő, amikor a nagy energiájú reaktánsok alacsonyabb energiájú termékekké alakulnak át, és az elektronok az alacsonyabb redoxpotenciálból a magasabb redoxpotenciálba kerülnek át, az ionok elektrokémiai gradiensének létrehozásával. Ez az elektrokémiai gradiens hajtja az ATP szintézisét az ATP szintetázzal végzett oxidatív foszforilezéssel való összekapcsolás révén .
Az eukarióta szervezetekben az elektronszállító lánc és az oxidatív foszforiláció helye a belső mitokondriális membránon található . Az oxigén és a redukált vegyületek, például a citokróm c, valamint (közvetve) a NADH és a FADH reakciójában felszabaduló energiát az elektronszállító lánc protonok szivattyúzására használja a membránok közötti térbe , elektrokémiai gradienst generálva a belső mitokondriális membránon. A fotoszintetikus eukariótákban az elektronszállító lánc a tilakoid membránon található. Itt a fényenergia hajtja az elektronszállító lánc összetevőinek redukcióját, és ezért az ATP későbbi szintézisét okozza. A baktériumokban az elektronszállító lánc fajonként változhat, de mindig redoxreakciók halmazát képezi, amelyek az ATP szintéziséhez kapcsolódnak, elektrokémiai gradiens létrehozása és oxidatív foszforiláció révén ATP szintázon keresztül.
Mitokondriális elektronszállító láncok
A legtöbb eukarióta sejt mitokondriumokkal rendelkezik , amelyek ATP -t termelnek a citromsav -ciklus , a zsírsav -oxidáció és az aminosav -oxidáció termékeiből . A belső mitokondriális membránon a NADH és a FADH 2 elektronjai áthaladnak az elektronszállító láncon az oxigénhez, amely biztosítja az energiát, amely a folyamatot vízzé redukálja. Az elektronszállító lánc elektron donorok és akceptorok enzimatikus sorozatából áll. Minden elektrondonor átadja az elektronokat egy elektronegatívabb akceptornak , amely viszont ezeket az elektronokat egy másik akceptornak adományozza. Ez a folyamat addig folytatódik, amíg az elektronokat el nem juttatják az oxigénhez, a lánc legerősebb és leggazdagabb elektronakceptorához. A donor és az akceptor közötti minden reakció energiát szabadít fel, amelyet az átvitt elektronokon keresztül protongradiens generálására használnak a mitokondriális membránon keresztül úgy, hogy "pumpálják" a protonokat a membránközi térbe, és magasabb szabad energia állapotot hoznak létre, amely képes megtenni munka. Ezt az egész folyamatot oxidatív foszforilációnak nevezik, mivel az ADP -t ATP -ként foszforilezzük az elektronszállító lánc redoxreakciói által létrehozott elektrokémiai gradiens használatával.
Mitokondriális redox hordozók
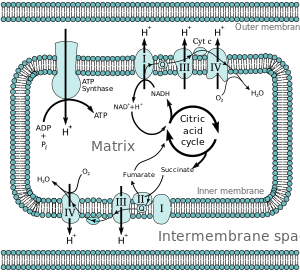
Az elektronok transzportláncon belüli átviteléhez kapcsolódó energiát a protonok szivattyúzására használják a mitokondriális mátrixból a membránok közötti térbe, elektrokémiai protongradienst ( ΔpH ) hozva létre a belső mitokondriális membránon keresztül. Ez a protongradiens nagyrészt, de nem kizárólagosan felelős a mitokondriális membránpotenciálért (ΔΨ M ). Lehetővé teszi az ATP -szintáz számára, hogy a H + -áramot az enzimen keresztül visszajuttassa a mátrixba, hogy ATP -t állítson elő az adenozin -difoszfátból (ADP) és a szervetlen foszfátból . Az I komplex (NADH koenzim Q reduktáz; jelzett I) elektronokat fogad el a Krebs -ciklusú elektronhordozó nikotinamid -adenin -dinukleotidból (NADH) , és átadja őket a Q -koenzimnek (ubiquinone; jelölt Q), amely szintén a II -es komplexből ( szukcinát -dehidrogenáz ; címkével ellátott II). A Q átadja az elektronokat a III komplexnek ( citokróm bc 1 komplex ; jelölt III), amely átadja őket a citokróm c -nek (cyt c ). A Cyt c elektronokat továbbít a IV komplexhez ( citokróm c oxidáz ; IV jelzéssel), amely az elektronok és a hidrogénionok felhasználásával felszabadítja a molekuláris oxigén energiáját, amikor vízre redukálódik.
A mitokondriumokban négy membránhoz kötött komplexet azonosítottak. Mindegyik rendkívül összetett transzmembrán szerkezet, amely a belső membránba van ágyazva. Közülük három protonszivattyú. A szerkezeteket elektromosan lipidben oldódó elektronhordozók és vízben oldódó elektronhordozók kötik össze. A teljes elektronszállító lánc a következőképpen foglalható össze:
NADH+H+ → Complex I → Q
↑
Complex II
↑
Succinate → Complex III → cytochrome c → Complex IV → H2O
↑
Complex II
↑
Succinate
Komplex I.
Az I. komplexben (NADH ubikinon-oxireduktáz, I. típusú NADH-dehidrogenáz vagy mitokondriális komplex I; EC 1.6.5.3. ) Két elektronot eltávolítunk a NADH-ból, és átvisszük egy lipidben oldódó hordozóba, ubikinonba (Q). A redukált termék, az ubiquinol (QH 2 ) szabadon diffundál a membránon belül, és az I komplex négy protont (H + ) transzlokál a membránon, így protongradienst hoz létre. Az I. komplex az egyik fő hely, ahol idő előtt elektronszivárgás következik be az oxigénbe, így ez az egyik fő szuperoxid -termelőhely.
Az elektronok útvonala a következő:
NADH oxidálódik NAD + , azáltal, hogy csökkenti a flavin-mononukleotid , hogy FMNH 2 egy két-elektron lépésben. Az FMNH 2- t ezután két egyelektronos lépésben, egy félkinon köztiterméken keresztül oxidálják . Így minden elektron átkerül az FMNH 2-ből egy Fe-S klaszterbe , a Fe-S klaszterből az ubikinonba (Q). Az első elektron átvitele Q szabad gyökös ( félkinon ) formáját eredményezi, a második elektron átvitele pedig csökkenti a félkinon formát a QH 2 ubikinol formává . E folyamat során négy protont helyeznek át a mitokondriális mátrixból az intermembrán térbe. Amint az elektronok áthaladnak a komplexen, elektronáram keletkezik a komplex 180 Angstrom szélessége mentén a membránon belül. Ez az áram biztosítja a négy proton aktív transzportját a membránok közötti térbe két elektrononként a NADH -ból.
Komplex II
A II. Komplexben ( szukcinát-dehidrogenáz vagy szukcinát-CoQ-reduktáz; EC 1.3.5.1. ) További elektronokat juttatnak a szukcinátból származó kinonkészletbe (Q), és ( flavin-adenin-dinukleotidon (FAD) keresztül ) továbbítják a Q-ba. A II. fehérje alegységek: szukcinát -dehidrogenáz, (SDHA); szukcinát-dehidrogenáz [ubikinon] vas-kén alegység, mitokondriális, (SDHB); szukcinát dehidrogenáz komplex C alegység, (SDHC) és szukcinát dehidrogenáz komplex, D alegység, (SDHD). Más elektrondonorok (pl. Zsírsavak és glicerin-3-foszfát) szintén elektronokat irányítanak a Q-ba (FAD-on keresztül). A II komplex egy párhuzamos elektronszállító útvonal az 1. komplexhez, de az 1. komplexumtól eltérően ezen az úton nem szállítanak protonokat a membránok közötti térbe. Ezért a komplex II útja kevesebb energiával járul hozzá a teljes elektronszállító lánc folyamatához.
Komplex III
A III. Komplexben ( citokróm bc 1 komplex vagy CoQH 2 -citokróm c reduktáz; EC 1.10.2.2 ) a Q -ciklus a protonok aszimmetrikus abszorpciójával/felszabadulásával járul hozzá a protongradienshez . Két elektronot eltávolítunk a QH 2 -ből a Q O helyen, és egymás után átvisszük a citokróm c két molekulájába , egy vízoldható elektronhordozóba, amely a membránok közötti térben található. A másik két elektron egymás után halad át a fehérjén a Q i helyre, ahol az ubikinon kinon része kinolra redukálódik. Egy protongradienst egy kinol ( ) oxidáció képez a Q o helyen, és egy kinont ( ) képez a Q i helyen. (Összesen négy proton transzlokálódik: két proton kinolrá redukálja a kinont, és két proton szabadul fel két ubiquinol molekulából.)
Ha az elektronátvitel csökken (nagy membránpotenciál vagy légzőszervi inhibitorok, például antimycin A), a III komplex elektronokat szivárogtathat a molekuláris oxigénhez, ami szuperoxid képződését eredményezi.
Ezt a komplexet a dimerkaprol (British Antilewisite, BAL), a naptokinon és az antimicin gátolja.
Komplex IV
A IV komplexben ( citokróm c oxidáz ; EC 1.9.3.1 ), amelyet néha citokróm AA3 -nak is neveznek, négy elektronot távolítanak el a citokróm c négy molekulájából, és molekuláris oxigénbe (O 2 ) és négy protonba helyezik át, két vízmolekulát állítva elő. A komplexum koordinált rézionokat és több hemcsoportot tartalmaz. Ugyanakkor nyolc protont eltávolítanak a mitokondriális mátrixból (bár csak négy transzlokálódik a membránon), hozzájárulva a proton gradienshez. A komplex IV protonpumpálásának pontos részletei még tanulmányozás alatt állnak. A cianid a IV komplex inhibitora.
Párosítás oxidatív foszforilezéssel
A kemiozmotikus kapcsolási hipotézist , által javasolt Kémiai Nobel-díj győztes Peter D. Mitchell , az elektron transzport lánc és az oxidatív foszforiláció modulok egy proton gradiens át a belső mitokondrium-hártyán. A protonok kiáramlása a mitokondriális mátrixból elektrokémiai gradienst (protongradienst) hoz létre . Ezt a gradienst használja fel az F O F 1 ATP szintáz komplex, hogy oxidatív foszforilezés útján ATP -t állítson elő. Az ATP -szintázt néha az elektronszállító lánc komplexének V -ként írják le . A F O komponense ATP szintáz viselkedik, mint egy ioncsatorna , amely biztosítja a proton fluxus vissza a mitokondriális mátrixban. A, b és c alegységekből áll. A mitokondriumok membránközi terében lévő protonok először egy alegység csatornán keresztül jutnak be az ATP szintáz komplexbe . Ezután a protonok a c alegységekhez költöznek. Száma c alegységek meghatározza, hogy hány protonok van szükség, hogy az F O viszont egy teljes fordulatot. Például az emberekben 8 c alegység van, így 8 protonra van szükség. Miután c alegységek, protonok végül a mátrixba jutnak be keresztül egy alegység csatornát, amely megnyitja a mitokondriális mátrixban. Ez a reflux szabad energiát szabadít fel az elektronhordozók oxidált formái (NAD + és Q) keletkezése során. A szabad energiát az ATP szintézis meghajtására használják, amelyet a komplex F 1 komponense katalizál .
Az oxidatív foszforilezéssel való összekapcsolás kulcsfontosságú lépés az ATP termelésében. Bizonyos esetekben azonban a két folyamat leválasztása biológiailag hasznos lehet. A szétkapcsolódó fehérje, a termogenin - a barna zsírszövet belső mitokondriális membránjában - alternatív protonáramlást biztosít a belső mitokondriális mátrixba. A tiroxin természetes leválasztó is. Ez az alternatív áramlás termogenezist eredményez, nem pedig ATP termelést.
Fordított elektronáramlás
A fordított elektronáramlás az elektronok átvitele az elektronszállító láncon keresztül a fordított redox reakciókon keresztül. Általában jelentős mennyiségű energiát igényel, ez csökkentheti az elektrondonorok oxidált formáit. Például a NAD + NADH -ra redukálható az I. komplex segítségével. Számos tényező bizonyította, hogy fordított elektronáramlást indukál. Ennek megerősítésére azonban további munkára van szükség. Az egyik példa az ATP-szintáz elzáródása, ami protonok felhalmozódását és ezáltal nagyobb proton-mozgatóerőt eredményez , fordított elektronáramlást indukálva.
Bakteriális elektronszállító láncok
Az eukariótákban a NADH a legfontosabb elektrondonor. A kapcsolódó elektronszállító lánc az
NADH → I komplex → Q → III. Komplex → citokróm c → IV. Komplex → O 2, ahol az I., III. És IV . Komplex protonpumpa, míg a Q és a citokróm c mobil elektronhordozó. Az elektronakceptor a molekuláris oxigén.
A prokariótákban ( baktériumok és archaea ) a helyzet bonyolultabb, mivel több különböző elektrondonor és több különböző elektronakceptor létezik. A baktériumok általános elektronszállító lánca a következő:
Donor Donor Donor
↓ ↓ ↓
dehydrogenase → quinone → bc1 → cytochrome
↓ ↓
oxidase(reductase) oxidase(reductase)
↓ ↓
Acceptor Acceptor
Az elektronok három szinten léphetnek be a láncba: egy dehidrogenáz szintjén, a kinonkészlet szintjén vagy egy mobil citokróm elektronhordozó szintjén . Ezek a szintek egymás után pozitívabb redoxpotenciáloknak vagy a terminális elektronakceptorhoz képest csökkenő potenciálkülönbségeknek felelnek meg. Más szavakkal, ezek az egymást követő kisebb Gibbs szabad energiaváltozásoknak felelnek meg a teljes redoxreakcióban.
Az egyes baktériumok több elektronszállító láncot használnak, gyakran egyszerre. A baktériumok számos különböző elektrondonort, számos különböző dehidrogenázt, számos különböző oxidázt és reduktázt, valamint számos különböző elektronakceptort használhatnak fel. Például az E. coli (amikor aerob módon termeszt, glükózt és oxigént használva energiaforrásként) két különböző NADH -dehidrogenázt és két különböző kinol -oxidázt használ, összesen négy különböző elektronszállító láncot működtetve egyidejűleg.
Minden elektronszállító lánc közös jellemzője, hogy protonpumpa van jelen, amely elektrokémiai gradienst hoz létre a membránon. A bakteriális elektronszállító láncok, akár a mitokondriumok, akár három protonszivattyút is tartalmazhatnak, vagy kettőt vagy legalább egyet.
Elektron donorok
A jelenlegi bioszférában a leggyakoribb elektrondonorok a szerves molekulák. Azokat a szervezeteket, amelyek szerves molekulákat használnak elektronforrásként, organotrófoknak nevezzük . A kemoorganotrófok (állatok, gombák, protisták) és a fotolitotrófok (növények és algák) alkotják az összes ismert életforma túlnyomó részét.
Néhány prokarióta szervetlen anyagot használhat elektronként és energiaforrásként. Az ilyen szervezetet (kemo) litotrófnak (" kőfalónak " ) nevezik . A szervetlen elektrondonorok közé tartozik a hidrogén, szén -monoxid, ammónia, nitrit, kén, szulfid, mangán -oxid és vasvas. Lithotrófokat találtak a sziklaalakzatokban, több ezer méterrel a Föld felszíne alatt. Eloszlási volumenük miatt a litotrófok valójában meghaladhatják a bioszféránk organotrófjait és fototrófjait.
A szervetlen elektrondonorok, például a hidrogén energiaforrásként történő felhasználása különösen érdekes az evolúció tanulmányozásában. Ez a fajta anyagcsere logikusan megelőzte a szerves molekulák és az oxigén energiaforrásként történő felhasználását.
Az I. és II
A baktériumok több különböző elektron donort is használhatnak. Ha a szerves anyag az elektronforrás, akkor a donor lehet NADH vagy szukcinát, ebben az esetben az elektronok NADH -dehidrogenázon keresztül lépnek be az elektronszállító láncba (hasonlóan az I. komplexhez a mitokondriumokban) vagy szukcinát -dehidrogenázon (hasonlóan a II . Komplexhez ). Egyéb dehidrogenázok lehet használni, hogy feldolgozza a különböző energiaforrások: formiát-dehidrogenáz, laktát-dehidrogenáz, gliceraldehid-3-foszfát-dehidrogenáz, H 2 -dehidrogenáz ( hidrogenáz ), elektrontranszport lánc. Egyes dehidrogenázok protonpumpák is; mások elektronokat töltenek a kinonmedencébe. A legtöbb dehidrogenáz indukált expressziót mutat a baktériumsejtekben, válaszul a sejtek növekedési környezete által kiváltott anyagcsere -szükségletekre. Az E. coli -ban található laktát -dehidrogenáz esetében az enzimet aerob módon és más dehidrogenázokkal kombinálva alkalmazzák. Indukálható, és akkor fejeződik ki, ha a DL-laktát koncentrációja a sejtben magas.
Kinon hordozók
A kinonok mobil, zsírban oldódó hordozók, amelyek elektronokat (és protonokat) szállítanak a membránba ágyazott nagy, viszonylag mozdulatlan makromolekuláris komplexek közé. A baktériumok ubikinont (koenzim Q, ugyanaz a kinon, amit a mitokondriumok használnak) és rokon kinonokat, például menaquinont (K 2 -vitamin ) használnak. A Sulfolobus nemzetségbe tartozó Archaea caldariellaquinone -t használ. A különböző kinonok használata a kissé megváltozott redoxpotenciáloknak köszönhető. A redoxpotenciál ezen változásait a kinon szerkezetének megváltozása okozza. Ezen kinonok redoxpotenciáljainak változása alkalmas lehet az elektronakceptorok változásaira vagy a redoxpotenciálok variációira a bakteriális komplexekben.
Proton szivattyúk
A protonpumpa minden olyan folyamat, amely protongradienst hoz létre egy membránon. A protonok fizikailag mozgathatók egy membránon; ez látható az I. és IV . mitokondriális komplexben . Ugyanez a hatás érhető el elektronok ellentétes irányú mozgatásával. Az eredmény egy proton eltűnése a citoplazmából és egy proton megjelenése a periplazmában. A mitokondriális komplex III ezt a második típusú protonpumpát használja, amelyet egy kinon közvetít (a Q ciklus ).
Néhány dehidrogenáz protonpumpa; mások nem. A legtöbb oxidáz és reduktáz protonszivattyú, de néhány nem. A citokróm bc 1 egy protonpumpa, amely sok, de nem minden baktériumban található (nem E. coliban ). Ahogy a neve is sugallja, a bakteriális bc 1 hasonló a mitokondriális bc 1 -hez ( III . Komplex ).
Citokróm elektronhordozók
A citokromok vasat tartalmazó pigmentek. Két nagyon különböző környezetben találhatók.
Néhány citokróm vízben oldódó hordozó, amely elektronokat szállít a membránba ágyazott nagy, mozdulatlan makromolekuláris struktúrákba. A mobil citokróm elektronhordozó a mitokondriumokban a citokróm c . A baktériumok számos különböző mobil citokróm elektronhordozót használnak.
Más citokrómok találhatók a makromolekulákban, mint például a komplex III és a komplex IV . Elektronhordozóként is működnek, de nagyon eltérő, intramolekuláris, szilárdtest-környezetben.
Az elektronok egy mobil citokróm vagy kinon hordozó szintjén léphetnek be az elektronszállító láncba. Például a szervetlen elektrondonorok elektronjai (nitrit, vasvas, elektronszállító lánc) citokróm szinten lépnek be az elektronszállító láncba. Amikor az elektronok a NADH-nál nagyobb redoxszinten lépnek be, az elektronszállító láncnak fordítva kell működnie, hogy ezt a szükséges, nagyobb energiájú molekulát előállítsa.
Terminális oxidázok és reduktázok
Amikor a baktériumok aerob környezetben szaporodnak , a terminális elektron -akceptor (O 2 ) egy oxidáz nevű enzimmel válik vízzé . Amikor a baktériumok anaerob környezetben szaporodnak , a terminális elektron -akceptor egy reduktáz nevű enzim által redukálódik. A mitokondriumokban a terminális membránkomplex ( IV . Komplex ) citokróm -oxidáz. Az aerob baktériumok számos különböző terminális oxidázt használnak. Például az E. coli (fakultatív anaerob) nem tartalmaz citokróm -oxidázt vagy bc 1 komplexet. Aerob körülmények között két különböző terminális kinol -oxidázt (mindkét protonszivattyút) használ az oxigén vízre redukálására.
A bakteriális komplex IV osztályokba sorolható aszerint, hogy a molekulák terminális elektronakceptorként működnek. Az I. osztályú oxidázok citokróm -oxidázok, és oxigént használnak terminális elektronakceptorként. A II. Osztályba tartozó oxidázok kinol -oxidázok, és különféle terminális elektronakceptorokat használhatnak. Mindkét osztály kategóriákra osztható aszerint, hogy milyen redox aktív összetevőket tartalmaznak. Pl. A Heme aa3 1. osztályú terminális oxidázok sokkal hatékonyabbak, mint a 2. osztályú terminális oxidázok
Az anaerob baktériumok , amelyek nem használnak oxigént terminális elektron -akceptorként, a terminális reduktázokat a terminális akceptorukra szabják. Például az E. coli fumarát-reduktázt, nitrát-reduktázt, nitrit-reduktázt, DMSO-reduktázt vagy trimetil-amin-N-oxid-reduktázt használhat, attól függően, hogy ezek az akceptorok rendelkezésre állnak-e a környezetben.
A legtöbb terminális oxidáz és reduktáz indukálható . Ezeket a szervezet szükség szerint szintetizálja, adott környezeti feltételekre reagálva.
Elektronakceptorok
Ahogyan számos különböző elektrondonor létezik (szerves anyag az organotrófokban, szervetlen anyag a litotrófokban), úgy számos különböző elektronakceptor létezik, mind szerves, mind szervetlen. Ha rendelkezésre áll oxigén, akkor azt véglegesen elektron -akceptorként használják aerob baktériumokban és fakultatív anaerobokban, mivel ez generálja a legnagyobb Gibbs szabad energiaváltozást és a legtöbb energiát.
Anaerob környezetben különböző elektronakceptorokat használnak, beleértve a nitrátot, nitritet, vasvasat, szulfátot, szén -dioxidot és kis szerves molekulákat, például fumarátot.
Fotoszintetikus
Az oxidatív foszforiláció során az elektronok egy mérsékelt energiájú elektrondonorból, például NADH-ból egy nagy energiájú akceptorba, például O 2 -ba kerülnek át egy elektronszállító láncon keresztül, felszabadítva az energiát. A fotofoszforiláció során a napfény energiáját nagy energiájú elektrondonor létrehozására használják fel, amely ezt követően képes csökkenteni az oxidált komponenseket, amelyeket az elektronszállító lánc proton transzlokációjával kapcsolnak az ATP szintézishez.
A fotoszintetikus elektronszállító láncok, akárcsak a mitokondriális lánc, a bakteriális rendszerek különleges esetének tekinthetők. Ezek használata mobil, lipid-oldható kinon hordozók ( fillokinon és plasztokinon ) és a mobil, vízoldható hordozóanyagok ( citokrómok , elektrontranszport lánc.). Protonpumpát is tartalmaznak . A protonpumpa minden fotoszintetikus láncban hasonlít a mitokondriális komplex III -ra . A szimbiogenezis általánosan elterjedt elmélete azt javasolja, hogy mindkét organella baktériumból származik.
Lásd még
Hivatkozások
További irodalom
- Fenchel T, King GM, Blackburn TH (2006. szeptember). Bakteriális biogeokémia: Az ásványi kerékpározás ökofiziológiája (2. kiadás). Elsevier. ISBN 978-0-12-103455-9.
- Lengeler JW (1999. január). Drews G; Schlegel HG (szerk.). A prokarióták biológiája . Blackwell Science. ISBN 978-0-632-05357-5.
- Nelson DL, Cox MM (2005. április). Lehninger Principles of Biochemistry (4. kiadás). WH Freeman. ISBN 978-0-7167-4339-2.
- Nicholls DG, Ferguson SJ (2002. július). Bioenergetika 3 . Academic Press. ISBN 978-0-12-518121-1.
- Stumm W; Morgan JJ (1996). Vízi kémia (3. kiadás). John Wiley & Sons . ISBN 978-0-471-51185-4.
- Thauer RK, Jungermann K, Decker K (1977. március). "Energiatakarékosság kemotróf anaerob baktériumokban" . Bakteriológiai vélemények . 41. (1): 100–80. doi : 10.1128/MMBR.41.1.100-180.1977 . PMC 413997 . PMID 860983 .
- Fehér D (1999. szeptember). A prokarióták fiziológiája és biokémiája (2. kiadás). Oxford University Press . ISBN 978-0-19-512579-5.
- Voet D, Voet JG (2004. március). Biokémia . Biokémiai oktatás . 28 (3. kiadás). John Wiley & Sons . 124. o . doi : 10.1016/s0307-4412 (00) 00032-7 . ISBN 978-0-471-58651-7. PMID 10878303 .
- Kim HS, Patel K, Muldoon-Jacobs K, Bisht KS, Aykin-Burns N, Pennington JD, et al. (2010. január). "A SIRT3 egy mitokondriumokban lokalizált daganatszuppresszor, amely a mitokondriális integritás és az anyagcsere fenntartásához szükséges a stressz alatt . " Ráksejt . 17. (1): 41–52. doi : 10.1016/j.ccr.2009.11.023 . PMC 3711519 . PMID 20129246 .
- Raimondi V, Ciccarese F, Ciminale V (2020. január). "Onkogén útvonalak és az elektronszállító lánc: dangeROS összekötő" . Br J Cancer . 122. (2): 168–181. doi : 10.1038/s41416-019-0651-y . PMC 7052168 . PMID 31819197 .
Külső linkek
- Electron + szállítás + Chain + komplex + fehérjék az amerikai National Library of Medicine orvosi tárgyszórendszere (mm)
- Khan Akadémia, videó előadás