Zsírsav anyagcsere - Fatty acid metabolism
A zsírsav -anyagcsere különböző metabolikus folyamatokból áll, amelyek zsírsavakat tartalmaznak , vagy amelyek szorosan kapcsolódnak hozzájuk, a lipid makrotápanyagok kategóriájába tartozó molekulák családjához . Ezek a folyamatok főként (1) katabolikus folyamatokra oszthatók , amelyek energiát termelnek, és (2) anabolikus folyamatokra, ahol építőkövekként szolgálnak más vegyületek számára.
A katabolizmus során a zsírsavak metabolizálódnak, hogy energiát termeljenek, főleg adenozin -trifoszfát (ATP) formájában. Összehasonlítva más makrotápanyag -osztályokkal (szénhidrátok és fehérjék), a zsírsavak adják a legtöbb ATP -t grammonként számított energiára számítva, amikor a béta -oxidáció és a citromsav -ciklus által teljesen oxidálódnak CO 2 -vá és vízzé . Ezért a zsírsavak (főleg trigliceridek formájában ) a legtöbb állatban, és kisebb mértékben a növényekben a tüzelőanyag elsődleges tárolói.
Az anabolizmusban az ép zsírsavak fontos prekurzorai a triglicerideknek, foszfolipideknek, másodlagos hírvivőknek, hormonoknak és ketontesteknek . Például a foszfolipidek olyan foszfolipid kettős rétegeket képeznek , amelyekből a sejt minden membránja zsírsavakból épül fel. A foszfolipidek magukban foglalják a plazmamembránt és más membránokat, amelyek a sejtek összes organelláját körülveszik , például a magot , a mitokondriumokat , az endoplazmatikus retikulumot és a Golgi -készüléket . Egy másik típusú anabolizmusban a zsírsavakat számtalan más vegyületté alakítják. Például néhány második hírvivő és helyi hormonosság . A prosztaglandinok készült arachidonsav tárolt a sejtmembránban, talán a legismertebb ilyen csoportot, a helyi hormonok.
Zsírsav katabolizmus
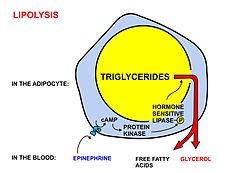


A zsírsavakat trigliceridként tárolják a zsírszövet zsírraktáraiban . Az étkezések között a következőképpen szabadulnak fel:
- A lipolízist , a zsírsavláncok eltávolítását a glicerinből, amelyhez trigliceridként (vagy zsírként) tárolási formában kötődnek, lipázok végzik . Ezeket a lipázokat a vér magas epinefrin- és glukagonszintje (vagy a zsírszövet szimpatikus idegei által kiválasztott norepinefrin) aktiválja, amelyet az étkezés utáni csökkenő vércukorszint okoz, ami egyidejűleg csökkenti a vér inzulinszintjét .
- A glicerinből való felszabadulás után a szabad zsírsavak belépnek a vérbe, amely a plazmaalbuminhoz kötődve szállítja őket a szervezetben.
- A hosszú láncú szabad zsírsavak specifikus transzportfehérjék , például az SLC27 család zsírsavszállító fehérje révén jutnak be a metabolizáló sejtekbe (azaz a legtöbb élő sejtbe a szervezetben, kivéve a vörösvértesteket és a központi idegrendszer neuronjait ) . A vörösvértestek nem tartalmaznak mitokondriumokat , ezért nem képesek zsírsavak metabolizálására; a központi idegrendszer szövetei nem használhatják a zsírsavakat, annak ellenére, hogy mitokondriumokat tartalmaznak, mivel a hosszú láncú zsírsavak (szemben a közepes láncú zsírsavakkal) nem tudnak átjutni a vér -agy gáton az ezeket a sejteket fürdő intersticiális folyadékokba .
- A sejt hosszú láncú zsírsavjába kerülve a CoA ligáz katalizálja a zsírsavmolekula és az ATP közötti reakciót (amely AMP-re és szervetlen pirofoszfátra bomlik ), így egy zsíros acil-adenilátot kap, amely ezután reagál a szabad koenzimmel hogy zsíros acil-CoA molekulát kapjunk .
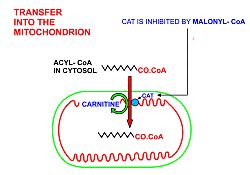
- Annak érdekében, hogy az acil-CoA bejusson a mitokondriumba, a karnitin transzfert kell használni:
- Az acil-CoA-t a karnitin-palmitoiltranszferáz I hordozza a karnitin hidroxilcsoportjába , amely a külső és a belső mitokondriális membrán citoszolikus felületén található .
- Az acil-karnitin belsejében egy karnitin-acil-karnitin transzlokáz vezet , míg a karnitin kívül.
- Az acil-karnitint a karnitin-palmitoiltranszferáz II , amely a belső mitokondriális membrán belső oldalán található, visszaalakítja acil-CoA-vé . A felszabadult karnitin visszavezetődik a citoszolhoz, amikor egy acil-CoA a mitokondriális mátrixba kerül.
- Beta oxidációt , a mitokondriális mátrixban, majd levágja a hosszú szénláncú zsírsavak (formájában acil-CoA-molekulák) egy sorozat két szénatomos ( acetát ) egységek, amelyek együtt ko-enzim-A , forma acetil -CoA molekulák , amelyek oxaloacetáttal kondenzálódva citrátot képeznek a citromsavciklus "elején" . Kényelmes úgy gondolni, hogy ez a reakció a ciklus "kiindulópontját" jelzi, mivel ekkor üzemanyagot - acetil -CoA -t - adnak a ciklushoz, amely CO 2 és H 2 O formájában felszabadul a jelentős mennyiségű energiát rögzítettek ATP formájában a ciklus minden fordulója során.
- Röviden, a béta-oxidáció lépései (a szabad zsírsavak kezdeti bontása acetil-CoA-ra) a következők:
- Dehidrogénezés acil-CoA-dehidrogenázzal , 1 FADH 2-t kapva
- Hidratálás enoil-CoA hidratázzal
- Dehidrogénezés 3-hidroxi-acil-CoA-dehidrogenázzal , így 1 NADH + H +
- A tioláz hasítása 1 acetil-CoA-t és egy zsírsavat eredményez, amelyet most 2 szénnel rövidítettek le (új, rövidített acil-CoA-t képezve )
- Ezt a béta-oxidációs reakciót addig ismételjük, amíg a zsírsav teljesen redukálódik acetil-CoA-ra, vagy-páratlan számú szénatomos zsírsavak esetén- acetil-CoA-ra és 1 molekula propionil-CoA-ra zsírsavmolekulánként. Az acil-CoA molekula minden béta-oxidatív vágása 5 ATP- molekulát eredményez.
- A béta-oxidációval előállított acetil-CoA belép a citromsav-ciklusba a mitokondriumban, oxal-acetáttal kombinálva citrátot képez . Ennek eredményeként az acetil-CoA teljesen elégethető CO 2 -vá és vízzé. Az ebben a folyamatban felszabaduló energiát 1 GTP és 11 ATP molekula formájában rögzítik acetil-CoA molekulánként. Ez az acetil-CoA sorsa mindenütt, ahol a zsírsavak béta-oxidációja történik, kivéve bizonyos körülményeket a májban .
A májban az oxaloacetát teljesen vagy részben a glükoneogén útvonalra terelhető böjt, éhezés, alacsony szénhidráttartalmú étrend, hosszan tartó megerőltető testmozgás és ellenőrizetlen 1 -es típusú diabetes mellitus esetén . Ilyen körülmények között az oxaloacetátot maláttá hidrogénezik, amelyet aztán eltávolítanak a májsejtek mitokondriumaiból, és glükózzá alakítják a májsejtek citoplazmájában, ahonnan a vérbe kerülnek. Ezért a májban az oxaloacetát nem áll rendelkezésre acetil-CoA kondenzációjához, ha jelentős glükoneogenezist serkent az alacsony (vagy hiányzó) inzulin és a vér magas glükagonkoncentrációja . Ilyen körülmények között az acetil-CoA-t acetoacetát és béta-hidroxi-butirát képzésére fordítják . Az acetoacetátot, a béta-hidroxi-butirátot és spontán bomlásterméküket, az acetont gyakran, de zavarosan ketontesteknek nevezik (mivel ezek egyáltalán nem "testek", hanem vízben oldódó kémiai anyagok). A ketonokat a máj bocsátja ki a vérbe. Minden mitokondriummal rendelkező sejt felveheti a ketonokat a vérből, és átalakíthatja őket acetil-CoA-vé, amelyet aztán üzemanyagként használhatnak fel citromsavciklusuk során, mivel más szövetek nem tudják a glükoneogén útvonalra terelni oxaloacetátját. a májban fordulnak elő. A szabad zsírsavakkal ellentétben a ketonok átjuthatnak a vér-agy gáton , ezért üzemanyagként állnak rendelkezésre a központi idegrendszer sejtjei számára , és helyettesítik a glükózt, amelyen ezek a sejtek általában túlélnek. A előfordulása magas szintű ketonok a vérben éhezés során, az alacsony szénhidráttartalmú diéta, elhúzódó nehéz gyakorolni és ellenőrizetlen 1. típusú diabetes mellitus néven ismert ketózis , és, a szélsőséges formájában, out-of-ellenőrzés 1. típusú diabetes mellitus, mint ketoacidózis .
- A lipáz hatására felszabaduló glicerint a glicerin kináz foszforilálja a májban (ez az egyetlen szövet, amelyben ez a reakció előfordulhat), és a kapott glicerin-3-foszfát dihidroxi-aceton -foszfáttá oxidálódik . A glikolitikus enzim, a trióz-foszfát-izomeráz ezt a vegyületet gliceráldehid-3-foszfáttá alakítja , amely glikolízissel oxidálódik , vagy glükoneogenezis útján glükózzá alakul .
Zsírsavak, mint energiaforrás

A szervezetben trigliceridként tárolt zsírsavak fontos energiaforrások, mivel redukáltak és vízmentesek . Az egy gramm zsírsavból származó energiahozam körülbelül 9 kcal (37 kJ), míg a szénhidrátok esetében 4 kcal (17 kJ). Mivel a zsírsavak szénhidrogén része hidrofób , ezek a molekulák viszonylag vízmentes ( vízmentes ) környezetben tárolhatók . A szénhidrátok viszont jobban hidratáltak. Például 1 g glikogén körülbelül 2 g vizet képes megkötni , ami 1,33 kcal/g (4 kcal/3 g). Ez azt jelenti, hogy a zsírsavak több mint hatszoros energiamennyiséget képesek tárolási tömeg egységre számítani. Másként fogalmazva, ha az emberi szervezet szénhidrátra támaszkodik az energia tárolásához, akkor egy személynek 31 kg (67,5 font ) hidratált glikogént kell cipelnie ahhoz, hogy az energia 4,6 kg (10 lb) zsírral egyenértékű legyen .
A hibernált állatok jó példát mutatnak a zsírtartalékok üzemanyagként való felhasználására. Például a medvék körülbelül 7 hónapig hibernálnak, és ebben az egész időszakban az energia a zsírraktárak lebomlásából származik. A vándorló madarak hasonlóan nagy zsírtartalékokat halmoznak fel, mielőtt elindulnak interkontinentális útjaikra.
Így a fiatal felnőtt ember zsírtartalma átlagosan körülbelül 10–20 kg, de nagymértékben változik az életkortól, a nemtől és az egyéni beállítottságtól függően. Ezzel szemben az emberi test csak körülbelül 400 g glikogént tárol , amelyből 300 g a vázizomzatban van, és nem érhető el a szervezet egésze számára. A májban tárolt körülbelül 100 g glikogén az éhezést követő egy napon belül kimerül. Ezt követően a glükózt, amelyet a máj bocsát ki a vérbe a test szöveteinek általános felhasználására, a glükogén aminosavakból és néhány más glükoneogén szubsztrátból kell szintetizálni , amelyek nem tartalmazzák a zsírsavakat. Kérjük, vegye figyelembe, hogy a lipolízis glicerint szabadít fel, amely beléphet a glükoneogenezis útjába.
Szénhidrát szintézis glicerinből és zsírsavakból
Zsírsavak bomlanak acetil-CoA útján béta oxidációs belsejében a mitokondriumok, míg zsírsavak szintetizált acetil-CoA kívül mitokondriumok, a citoszolban. A két útvonal nem csak abban különbözik, hogy hol fordulnak elő, hanem a bekövetkező reakciókban és a felhasznált szubsztrátokban is. A két út kölcsönösen gátolja, és megakadályozza, hogy a béta-oxidáció által termelt acetil-CoA belépjen a szintetikus útba az acetil-CoA karboxiláz reakció révén. Azt sem lehet piruváttá alakítani, mivel a piruvát -dehidrogenáz komplex reakció visszafordíthatatlan. Ehelyett a zsírsavak béta-oxidációjával keletkező acetil-CoA oxaloacetáttal kondenzálódik , és belép a citromsav-ciklusba . A ciklus minden fordulója során két szénatom távozik a ciklusból CO 2 -ként az izocitrát-dehidrogenáz és az alfa-ketoglutarát-dehidrogenáz által katalizált dekarboxilezési reakciók során . Így a citromsavciklus minden fordulata oxidálja az acetil-CoA egységet, miközben regenerálja az oxaloacetát molekulát, amellyel az acetil-CoA eredetileg citromsavat képezett . A dekarboxilezési reakciók a malát képződése előtt jelentkeznek a ciklusban. Csak a növények rendelkeznek olyan enzimekkel, amelyek az acetil-CoA-t oxaloacetáttá alakítják, amelyből malát képződhet, és végül glükózzá alakítható.
Az acetil-CoA azonban átalakítható acetoacetáttá, amely dekarboxilálhat acetonná (akár spontán, akár acetoacetát-dekarboxiláz segítségével ). Ez azután tovább metabolizálódik izopropanolban, amely kiválasztódik a levegőt / vizeletben, vagy CYP2E1 be hidroxi-aceton (acetol). Az acetol propilénglikollá alakítható . Ez átalakítja a formiát és acetát (az utóbbi konvertálás glükóz), vagy piruvát (két alternatív enzimek), vagy propionaldehid , illetve L -lactaldehyde majd L -laktát (a közös laktát izomer). Egy másik útvonal fordulat acetol a metil-glioxál , majd piruvát , vagy D -lactaldehyde (via SD -lactoyl-glutation vagy más módon), majd a D -laktát . A D-laktát anyagcsere (glükózmá) emberben lassú vagy károsodott, ezért a D-laktát nagy része a vizelettel ürül; így az acetonból származó D -laktát jelentősen hozzájárulhat a ketózishoz vagy az izopropanol -mérgezéshez kapcsolódó metabolikus acidózishoz. Az L -laktát befejezheti a zsírsavak glükózzá történő nettó átalakítását. Az első kísérletet, amely az aceton glükózzá való átalakulását mutatta be, 1951 -ben hajtották végre. Ez és a további kísérletek szénizotóp jelölést alkalmaztak . Az emberek éhezése során a glükóz akár 11% -a is származhat acetonból.
A trigliceridek zsírszövetben történő lipolízise során a vérbe felszabaduló glicerint csak a máj tudja felvenni. Itt alakul át a glicerin-3-foszfát hatására a glicerin-kináz , amely hidrolizálja az egyik molekula ATP per glicerin molekula, amely foszforilálja. A glicerin-3-foszfát ezután dihidroxi-aceton-foszfáttá oxidálódik, amelyet a trióz-foszfát-izomeráz enzim glicerál -dehid-3-foszfáttá alakít . Innen a három szénatom az eredeti glicerin lehet oxidált keresztül glikolízis alakíthatjuk vagy a glükóz keresztül glükoneogenezis .
A zsírsavak egyéb funkciói és felhasználása
Intracelluláris jelzés
Zsírsavak szerves részét képezik a foszfolipidek teszik ki a nagy részét a plazma membránok , vagy sejt membránok, sejtek. Ezek a foszfolipidek a sejtmembránhoz kötött foszfolipáz C enzimmel (PLC) a foszfolipid, a foszfatidil-inozitol 4,5-biszfoszfát (PIP 2 ) hidrolízisével diacil-glicerin (DAG) és inozitol-trifoszfát (IP 3 ) bonthatók .
Eikozanoid parakrin hormonok
A zsírsav -anyagcsere egyik terméke a prosztaglandinok , vegyületek, amelyek állatokban különböző hormonszerű hatásokat fejtenek ki. A prosztaglandinok szinte minden szövetben megtalálhatók emberekben és más állatokban. Ezek enzimatikusan származnak az arachidonsavból, egy 20 szénatomos többszörösen telítetlen zsírsavból. Ezért minden prosztaglandin 20 szénatomot tartalmaz, köztük egy 5 szénatomos gyűrűt . Az eikozanoidok alosztályába tartoznak, és a zsírsavszármazékok prosztanoid osztályát alkotják.
A prosztaglandinokat a sejtmembránban szintetizálják az arachidonát hasításával a membránt alkotó foszfolipidekből. Ezt katalizálja vagy a foszfolipáz A 2, amely közvetlenül a membránfoszfolipidre hat, vagy egy lipáz, amely a DAG-ra (diacil-glicerin) hat. Az arachidonátra ezután a prosztaglandin szintáz ciklooxigenáz komponense hat . Ez ciklopentángyűrűt képez a zsírsavlánc nagyjából közepén. A reakció 4 oxigénatomot is hozzáad két O 2 molekulából . A kapott molekula a prosztaglandin G 2, amelyet az enzimkomplex hidroperoxidáz komponense átalakít prosztaglandin H 2 -vé . Ez a rendkívül instabil vegyület gyorsan átalakul más prosztaglandinokká, prosztaciklinné és tromboxánokká. Ezeket aztán az eikozanoid hormont előállító sejteket körülvevő intersticiális folyadékokba engedik.
Ha az arachidonátra ciklooxigenáz helyett lipoxigenáz hat, hidroxi -eicosatetraénsavak és leukotriének keletkeznek. Helyi hormonként is működnek.
A prosztaglandinoknak két származéka van: prosztaciklinek és tromboxánok . A prosztaciklinek erős helyi hatású értágítók, és gátolják a vérlemezkék aggregációját . Az értágításban betöltött szerepük révén a prosztaciklinek részt vesznek a gyulladásban is . Ezek az erek falában szintetizálódnak, és a szükségtelen vérrögképződés megelőzésének fiziológiai funkcióját szolgálják, valamint szabályozzák a simaizomszövet összehúzódását . Ezzel szemben a (vérlemezke -sejtek által termelt) tromboxánok érszűkítő szerek, és elősegítik a vérlemezkék aggregációját. Nevük a vérrögképződésben ( trombózis ) játszott szerepükből származik .
A zsírsavak étrendi forrásai, emésztésük, felszívódásuk, szállításuk a vérben és tárolás

A szervezetben található zsírsavak jelentős része az étrendből származik, állati vagy növényi eredetű trigliceridek formájában. A szárazföldi állatokból nyert zsírok zsírsavai általában telítettek, míg a halak és növények trigliceridjeiben található zsírsavak gyakran többszörösen telítetlenek, ezért olajként vannak jelen.
Ezeket a triglicerideket a bél nem tudja felszívni . Ezeket mono- és di-gliceridekre, valamint szabad zsírsavakra (de nem szabad glicerinre) bontják a hasnyálmirigy-lipáz , amely 1: 1 arányú komplexet képez a kolipáz nevű fehérjével (amely szintén a hasnyálmirigy-lé alkotórésze). tevékenységét. Az aktivált komplex csak víz-zsír felületen működhet. Ezért lényeges, hogy a zsírok először emulgeáljuk által epesók optimális Ezen enzimek aktivitását. Azok az emésztési termékek, amelyek tri-, di- és monogliceridek és szabad zsírsavak keverékéből állnak, amelyek az étrend többi zsírban oldódó tartalmával együtt (pl. Zsírban oldódó vitaminok és koleszterin) és az epesók kevert micellákat képeznek , vizes duodenális tartalom (lásd a jobb oldali ábrákat).
Ezek tartalma micellák (de nem a epesók) adja meg az enterociták (epiteliális sejtek a vékonybélben), ahol azokat újraszintetizáljuk be trigliceridek, és a csomagolt a kilomikronok amelyek felszabadulnak a lacteals (a kapillárisok a nyirokrendszer a belek ). Ezek lacteals ürüljön az mellkasi légcsatorna amely kiüríti a vénás vérben találkozásánál a bal nyaki és a bal kulcscsont alatti vénák a bal alsó oldalon a nyak. Ez azt jelenti, hogy az emésztés zsírban oldódó termékei közvetlenül az általános keringésbe kerülnek, anélkül, hogy előbb átjutnának a májon, mint minden más emésztési termék. Ennek a sajátosságnak az oka ismeretlen.
A chilomikronok keringnek az egész testben, tejes vagy krémes megjelenést kölcsönözve a vérplazmának zsíros étkezés után. Lipoprotein-lipáz a endoteliális felületeken a kapillárisok, különösen a zsírszövetben , de kisebb mértékben is, más szövetekben, részben emészti a kilomikronok szabad zsírsavakká, glicerin és kilomikron maradványai. A zsírsavakat az adipociták felszívják, de a glicerin és a chilomikron maradványai a vérplazmában maradnak, és végül a máj eltávolítja őket a keringésből. A chilomikronok emésztése során felszabaduló szabad zsírsavakat az adipociták felszívják, ahol a glikolitikus úton glükózból származó glicerin felhasználásával újra szintetizálják trigliceridekké . Ezeket a triglicerideket addig tárolják, amíg más szövetek üzemanyagszükségletére szükség van, az adipocita zsírcseppjében .
A máj a glükóz egy részét a bélből érkező portális véna véréből szívja fel . Miután a máj feltöltötte glikogénraktárait (amelyek csak 100 g glikogént tartalmaznak, amikor tele vannak), a fennmaradó glükóz nagy része zsírsavakká alakul át az alábbiak szerint. Ezeket a zsírsavakat glicerinnel kombinálva triglicerideket képeznek, amelyek a chilomikronokhoz nagyon hasonló cseppekbe vannak csomagolva, de nagyon alacsony sűrűségű lipoproteinek (VLDL) néven ismertek . Ezeket a VLDL-cseppeket ugyanúgy kezelik, mint a chilomikronokat, azzal a különbséggel, hogy a VLDL-maradékot köztes sűrűségű lipoproteinek (IDL) néven ismerik , amely képes eltávolítani a koleszterint a vérből. Ez az IDL-t alacsony sűrűségű lipoproteinné (LDL) alakítja át , amelyet olyan sejtek vesznek fel, amelyek koleszterint igényelnek a sejtmembránjukba való beépítéshez vagy szintetikus célokra (pl. A szteroid hormonok képződéséhez ). Az LDL -k maradékát a máj távolítja el.
A zsírszövet és a szoptató emlőmirigyek szintén felveszik a glükózt a vérből, hogy trigliceridekké alakuljanak át. Ez ugyanúgy történik, mint a májban, kivéve, hogy ezek a szövetek nem bocsátják ki az így VLDL -ként előállított triglicerideket a vérbe. A zsírszöveti sejtek a triglicerideket zsírcseppjeikben tárolják, végül szabad zsírsavak és glicerin formájában szabadítják fel őket a vérbe (a fentiekben leírtak szerint ), amikor az inzulin plazmakoncentrációja alacsony, és a glukagon és/vagy az epinefrin magas. . Az emlőmirigyek a zsírt (krémes zsírcseppek formájában) a tejbe ürítik, amelyet az elülső agyalapi mirigy prolaktin hormon hatására termelnek .
A test minden sejtjének elő kell állítania és karban kell tartania a membránjait és az organelláinak membránjait. Nem tudni, hogy teljes mértékben a vérből felszívódó szabad zsírsavakra támaszkodnak -e, vagy képesek a zsírsavak szintézisére a vércukorszintből, nem tudni. A központi idegrendszer sejtjei szinte biztosan képesek lesznek saját zsírsavak előállítására, mivel ezek a molekulák nem tudják elérni őket a vér -agy gáton keresztül , míg másrészt a szervezet egyetlen sejtje sem képes előállítani a szükséges esszenciális zsírsavakat. savak, amelyeket az étrendből kell beszerezni és a vér útján eljuttatni minden sejthez.
Zsírsav szintézis
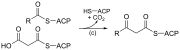
A béta-oxidációhoz hasonlóan az egyenes láncú zsírsavszintézis az alább bemutatott hat ismétlődő reakción keresztül megy végbe, amíg a 16 szénatomos palmitinsav képződik.
A bemutatott diagramok bemutatják, hogyan szintetizálják a zsírsavakat a mikroorganizmusokban, és felsorolják az Escherichia coli -ban található enzimeket . Ezeket a reakciókat végezzük zsírsav szintáz II (FASII), amelyek általában tartalmaznak számos enzim, hogy egyként komplex. A FASII jelen van prokariótákban , növényekben, gombákban és parazitákban, valamint a mitokondriumokban .
Az állatokban, valamint néhány gombában, például az élesztőben, ugyanezek a reakciók fordulnak elő a zsírsavszintetáz I -n (FASI), amely egy nagy dimer fehérje, amely rendelkezik a zsírsav létrehozásához szükséges összes enzimatikus aktivitással. A FASI kevésbé hatékony, mint a FASII; azonban lehetővé teszi több molekula, köztük "közepes láncú" zsírsavak képződését a lánc korai leállítása révén. Az enzimek, az aciltranszferázok és a trancilázok zsírsavakat tartalmaznak foszfolipidekben, triacil -glicerinekben stb., Zsírsavak acil -akceptor és donor közötti átvitelével. Feladatuk továbbá a bioaktív lipidek és prekurzor molekuláik szintetizálása.
Ha egy 16: 0 szénatomos zsírsav képződött, számos módosításon eshet át, ami telítetlenséget és/vagy megnyúlást eredményez. A nyúlást sztearáttal (18: 0) kezdve főként az endoplazmatikus retikulumban végzik több membránhoz kötött enzim. A megnyúlási folyamat enzimatikus lépései alapvetően megegyeznek a zsírsav -szintézissel , de a megnyúlás négy fő egymást követő lépését egyes fehérjék végzik, amelyek fizikailag is társulhatnak egymáshoz.
| Lépés | Enzim | Reakció | Leírás |
|---|---|---|---|
| a) | Acetil -CoA: ACP -transziláz | Aktiválja az acetil-CoA-t, hogy reagáljon a malonyl-ACP-vel | |
| b) | Malonyl CoA: ACP transacylase |
|
Aktiválja a malonil-CoA-t az acetil-ACP-val való reakcióhoz |
| c) | 3-ketoacil-ACP szintáz | Reagál az ACP-hez kötött acil-lánccal a láncot kiterjesztő malonyl-ACP-vel | |
| d) | 3-ketoacil-ACP reduktáz | A szén -3 ketont hidroxilcsoporttá redukálja | |
| e) | 3-hidroxi-acil-ACP-dehidráz | Megszünteti a vizet | |
| f) | Enoil-ACP reduktáz | Csökkenti a C2-C3 kettős kötést. |
Rövidítések: ACP - acil hordozófehérje , CoA - koenzim A , NADP - nikotinamid -adenin -dinukleotid -foszfát .
Vegye figyelembe, hogy a zsírszintézis során a redukálószer a NADPH , míg a NAD a béta-oxidációban (a zsírsavak acetil-CoA-ra bomlása) oxidálószer . Ez a különbség egy általános elvet szemléltet, amely szerint a NADPH-t a bioszintetikus reakciók során fogyasztják, míg a NADH-t energiatermelő reakciók során állítják elő. (Így a NADPH is szükséges az acetil-CoA-ból származó koleszterin szintéziséhez ; míg a NADH a glikolízis során keletkezik .) A NADPH forrása kettős. Amikor a malátot oxidatív módon dekarboxilezik a „NADP + -kapcsolatban lévő alma enzim" piruváttal , CO 2 és NADPH keletkezik. A NADPH -t a pentóz -foszfát út is képezi, amely a glükózt ribózzá alakítja, és amely felhasználható a nukleotidok és nukleinsavak szintéziséhez , vagy piruváttá katabolizálható.
A glikolitikus végtermékeket a szénhidrátok zsírsavakká történő átalakítására használják
Emberben a zsírsavak elsősorban szénhidrátokból képződnek a májban és a zsírszövetben , valamint az emlőmirigyekben a szoptatás alatt. A központi idegrendszer sejtjei valószínűleg a kiterjedt membránjaik foszfolipidjeihez szükséges zsírsavak nagy részét is glükózból állítják elő, mivel a vérből származó zsírsavak nem tudnak átjutni a vér-agy gáton, hogy elérjék ezeket a sejteket. Az azonban nem ismert, hogyan jutnak hozzájuk azok az esszenciális zsírsavak , amelyeket az emlősök nem tudnak szintetizálni, de ennek ellenére fontos összetevői a sejtmembránoknak (és a fent leírt egyéb funkcióknak ).
A glikolízissel előállított piruvát fontos közvetítő a szénhidrátok zsírsavvá és koleszterinné történő átalakításában. Ez a piruvátnak a mitokondriumban acetil-CoA-vé való átalakításával történik. Ezt az acetil -CoA -t azonban citoszolba kell szállítani, ahol a zsírsavak és a koleszterin szintézise történik. Ez nem fordulhat elő közvetlenül. A citoszolos acetil-CoA előállításához a citrátot (amelyet acetil-CoA és oxaloacetát kondenzálásával állítanak elő) eltávolítják a citromsav-ciklusból, és a belső mitokondriális membránon keresztül a citoszolba viszik. Ott az ATP-citrát-liáz acetil-CoA -vá és oxaloacetáttá hasítja . Az oxaloacetát malátként kerül vissza a mitokondriumba (majd oxaloacetáttá alakul, hogy több acetil-CoA-t vigyen át a mitokondriumból). A citoszol acetil-CoA-karboxilezett által acetil-CoA-karboxiláz a malonil-CoA , az első olyan lépésnek a zsírsavak szintézisében.
A zsírsav -szintézis szabályozása
Az acetil-CoA - t acetil-CoA-karboxiláz képezi malonil-CoA -ként , ekkor a malonil-CoA-t a zsírsav-szintézis útvonalába kell betáplálni. Acetil-CoA-karboxiláz az a pont a szabályozás, telített, egyenes láncú zsírsav szintézis, és ki van téve mind foszforiláció és allosztérikus szabályozás . A foszforilációval történő szabályozás többnyire emlősökben fordul elő, míg az alloszterikus szabályozás a legtöbb szervezetben fordul elő. Az alloszterikus kontroll a palmitoil-CoA által okozott visszacsatolás-gátlás és a citrát aktiválása révén történik. Ha magas a palmitoil-CoA szintje, a telített zsírsavak szintézisének végterméke, alloszterikusan inaktiválja az acetil-CoA karboxilázt, hogy megakadályozza a zsírsavak felhalmozódását a sejtekben. A citrát nagy mennyiségben aktiválja az acetil-CoA-karboxilázt, mivel a magas szint azt jelzi, hogy elegendő acetil-CoA van ahhoz, hogy a Krebs-ciklusba betápláljon és energiát termeljen.
A magas plazma inzulinszint a vérplazmában (pl. Étkezés után) az acetil-CoA-karboxiláz defoszforilációját és aktiválódását okozza, ezáltal elősegíti a acetil-CoA-ból a malonyl-CoA képződését, következésképpen a szénhidrátok zsírsavvá alakulását, míg az epinefrin és a glukagon (az éhezés és a testmozgás során a vérbe kerül) ennek az enzimnek a foszforilációját okozza, gátolja a lipogenezist a béta-oxidáció révén a zsírsav oxidáció javára .
Rendellenességek
A zsírsav -anyagcsere zavarai leírhatók például hipertrigliceridémiával (túl magas trigliceridszint ) vagy más típusú hiperlipidémiával . Ezek lehetnek családi vagy szerzett.
A zsírsav -anyagcsere családi rendellenességeit általában a lipid -anyagcsere veleszületett hibái közé sorolják . Ezek a rendellenességek lehetnek leírni, mint zsírsav-oxidáció rendellenességek vagy egy lipid-raktározási rendellenességek , és bármely egyike a számos veleszületett anyagcsere ezen eredmény Enzyme hibákra képessége a test oxidálja a zsírsavak annak érdekében, hogy energiát belül izmok, máj és más sejttípusok .
Ezenkívül a rákos sejtek szabálytalan zsírsav -anyagcserét mutathatnak mind a zsírsavszintézis , mind a mitokondriális zsírsav -oxidáció (FAO) tekintetében, amelyek részt vesznek a daganatképződés és a sejtnövekedés különböző aspektusaiban.