Szinaptikus hólyag - Synaptic vesicle
| Szinaptikus hólyag | |
|---|---|
 Neuron A (átvitel) a B neuronhoz (fogadó).
1 . Mitokondriumok ; 2 . Szinaptikus hólyag neurotranszmitterekkel ; 3 . Autoreceptor 4 . Szinapszis felszabaduló neurotranszmitterrel ( szerotonin ); 5 . Neurotranszmitter által aktivált posztszinaptikus receptorok ( posztszinaptikus potenciál indukciója ); 6 . Kalcium csatorna ; 7 . Hólyag exocitózisa ; 8 . Visszafogott neurotranszmitter. | |
| Részletek | |
| Rendszer | Idegrendszer |
| Azonosítók | |
| latin | vesicula synaptica |
| Háló | D013572 |
| TH | H2.00.06.2.00004 |
|
A mikroanatómia anatómiai feltételei | |
A neuron , szinaptikus vezikulák (vagy neurotranszmitter hólyagocskák ) tárolja a különböző neurotranszmitterek , amelyek megjelent a szinapszis . A felszabadulást feszültségfüggő kalciumcsatorna szabályozza . A hólyagok elengedhetetlenek az idegimpulzusok terjedéséhez a neuronok között, és a sejt folyamatosan újrateremti őket . Az axonban a hólyagcsoportokat tartó terület egy axonterminál vagy "terminális bouton". Egy boutononként legfeljebb 130 vezikulum szabadulhat fel tíz perces stimulációs periódus alatt 0,2 Hz-en. Az emberi agy látókéregében a szinaptikus vezikulák átlagos átmérője 39,5 nanométer (nm), szórása 5,1 nm.
Szerkezet
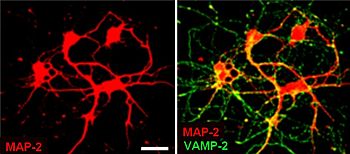
A szinaptikus vezikulumok viszonylag egyszerűek, mivel csak korlátozott számú fehérje fér el egy 40 nm átmérőjű gömbben. A tisztított hólyagok fehérje : foszfolipid aránya 1: 3, lipidösszetételük 40% foszfatidilkolin , 32% foszfatidil -etanol -amin , 12% foszfatidil -szerin , 5% foszfatidil -inozit és 10% koleszterin .
A szinaptikus vezikulák a kötelező komponensek két osztályát tartalmazzák: a neurotranszmitter felvételében részt vevő transzportfehérjéket és a szinaptikus vezikulák exocitózisában , endocitózisában és újrafeldolgozásában részt vevő transzportfehérjéket .
- A transzportfehérjék protonpumpákból állnak , amelyek elektrokémiai gradienseket hoznak létre , amelyek lehetővé teszik a neurotranszmitter felvételét, és neurotranszmitter transzporterekből, amelyek szabályozzák a neurotranszmitterek tényleges felvételét. A szükséges protongradienst a V-ATPáz hozza létre , amely lebontja az ATP- t energiaként. A vezikuláris transzporterek a neurotranszmittereket a sejtek citoplazmájából a szinaptikus hólyagokba mozgatják. A hólyagos glutamát transzporterek például a glutamátot vezikulumokká kötik ezzel az eljárással.
- A fehérjék kereskedelme összetettebb. Ide tartoznak a belső membránfehérjék , a perifériás kötődésű fehérjék és a fehérjék, például a SNARE -k . Ezek a fehérjék nem rendelkeznek olyan tulajdonságokkal, amelyek alapján szinaptikus hólyagfehérjékként azonosíthatók lennének, és keveset tudunk arról, hogy ezek a fehérjék hogyan rakódnak le specifikusan a szinaptikus vezikulákba. Sok, de nem minden ismert szinaptikus vezikuláris fehérje kölcsönhatásba lép a nem vezikuláris fehérjékkel, és specifikus funkciókhoz kapcsolódik.
A különböző neurotranszmitterek hólyagba való mozgásának sztöchiometriáját az alábbi táblázat tartalmazza.
| Neurotranszmitter típus (ok) | Befelé irányuló mozgás | Kifelé irányuló mozgás |
|---|---|---|
| noradrenalin , dopamin , hisztamin , szerotonin és acetilkolin | neurotranszmitter + | 2H + |
| GABA és glicin | neurotranszmitter | 1H + |
| glutamát | neurotranszmitter - + Cl - | 1H + |
A közelmúltban felfedezték, hogy a szinaptikus vezikulumok kis RNS -molekulákat is tartalmaznak, beleértve a transzfer RNS -fragmenseket, az Y RNS -fragmenseket és a mirRNS -eket . Ez a felfedezés vélhetően széles körű hatással van a kémiai szinapszisok tanulmányozására.
A neurotoxinok hatásai
Egyes neurotoxinok , például a batrachotoxin , ismerten elpusztítják a szinaptikus vezikulákat. A tetanusz toxin károsítja a vezikulákkal kapcsolatos membránfehérjéket (VAMP), a v-SNARE egyik típusát, míg a botulinum toxinok károsítják a t-SNARES-t és a v-SNARES-t, és ezáltal gátolják a szinaptikus átvitelt. Egy pók toxin úgynevezett alfa-Latrotoxin kötődik neurexins , károsítva vezikulumok és ami hatalmas neurotranszmitterek felszabadulását.
Vezikuláris medencék
Az idegvégződésben lévő hólyagok három medencébe vannak csoportosítva: a könnyen kivehető medence, az újrahasznosító medence és a tartalék medence. Ezeket a medencéket funkciójuk és idegterminális helyzetük jellemzi. A könnyen kiengedhető medence a sejtmembránhoz van rögzítve , így ez az első vezikulumcsoport, amely stimuláció hatására felszabadul. A könnyen kivehető medence kicsi és gyorsan kimerül. Az újrahasznosító medence közel van a sejtmembránhoz, és általában mérsékelt stimuláció mellett ciklusos, így a hólyagok felszabadulásának sebessége megegyezik a hólyagképződés sebességével vagy alacsonyabb. Ez a medence nagyobb, mint a könnyen kivehető medence, de hosszabb ideig tart a mozgósítás. A tartalék medence olyan hólyagokat tartalmaz, amelyek normál körülmények között nem szabadulnak fel. Ez a tartalékkészlet meglehetősen nagy (~ 50%) lehet üvegszubsztráton nevelt neuronokban, de nagyon kicsi vagy hiányzik az ép agyszövet érett szinapszisaiban.
Fiziológia
A szinaptikus hólyagciklus
A szinaptikus hólyagciklus eseményei néhány kulcslépésre oszthatók:
- 1. Kereskedelem a szinapszisba
A szinaptikus hólyagkomponenseket kezdetben a szinapszisba szállítják a kinesin motorcsalád tagjainak segítségével . A C. elegans-ban a szinaptikus vezikulumok fő motorja az UNC-104. Bizonyíték van arra is, hogy más fehérjék, például az UNC-16/Sunday Driver szabályozzák a motorok használatát a szinaptikus vezikulumok szállítására.
- 2. Az adó betöltése
A szinapszisba kerülve a szinaptikus hólyagok neurotranszmitterrel vannak feltöltve. Az adó betöltése aktív folyamat, amely neurotranszmitter transzportert és protonpumpa ATPáz -ot igényel, amely elektrokémiai gradienst biztosít. Ezek a transzporterek szelektívek a különböző típusú adók számára. A hólyagos acetilkolin transzportert és a vezikuláris GABA transzportert kódoló unc-17 és unc-47 jellemzését eddig leírták.
- 3. Dokkolás
A betöltött szinaptikus vezikuláknak a felszabadulási helyek közelében kell dokkolniuk, azonban a dokkolás a ciklus egy olyan lépése, amelyről keveset tudunk. Számos fehérjét azonosítottak a szinaptikus vezikulákon és a felszabadulási helyeken, azonban a vezikuláris fehérjék és a felszabadulási hely fehérjéi között azonosított fehérje kölcsönhatások egyike sem képes figyelembe venni a ciklus dokkoló szakaszát. A rab-3 és munc-18 mutánsok megváltoztatják a hólyagok dokkolását vagy a vezikulák szervezetét a felszabadulási helyeken, de nem zavarják teljesen a dokkolást. Úgy tűnik, hogy a SNARE fehérjék szintén részt vesznek a ciklus dokkolási lépésében.
- 4. Alapozás
Miután a szinaptikus vezikulumok kezdetben kiköttek, a fúzió megkezdése előtt alapozni kell őket. Az alapozás előkészíti a szinaptikus hólyagot, hogy gyorsan képesek legyenek összeolvadni a kalcium beáramlás hatására. Úgy gondolják, hogy ez az alapozási szakasz részben összeállított SNARE -komplexek kialakulását foglalja magában. A Munc13 , RIM és RIM-BP fehérjék részt vesznek ezen az eseményen. Úgy gondolják, hogy a Munc13 serkenti a t-SNARE szintaxis zárt konformációból nyílt konformációvá változását, ami stimulálja a v-SNARE /t-SNARE komplexek összeállítását. Úgy tűnik, a RIM is szabályozza az alapozást, de nem nélkülözhetetlen a lépéshez.
- 5. Fúzió
Az alapozott hólyagok nagyon gyorsan összeolvadnak, reagálva a citoplazma kalciumszintjének emelkedésére. Úgy gondolják, hogy ezt a fúziós eseményt közvetlenül a SNARE -k közvetítik, és a SNARE összeállításból származó energia hajtja. Ennek az eseménynek a kalcium-érzékelő kiváltója a kalcium-kötő szinaptikus vezikuláris fehérje, a szinaptotagmin. A SNARE-k azon képességét, hogy kalciumfüggő módon közvetítsék a fúziót, a közelmúltban in vitro helyreállították. A fúziós folyamathoz nélkülözhetetlen SNARE-kkel összhangban a C. elegans v-SNARE és t-SNARE mutánsai halálosak. Hasonlóképpen, a Drosophila mutánsai és az egerek kiütései azt jelzik, hogy ezek a SNARES -ek kritikus szerepet játszanak a szinaptikus exocitózisban.
- 6. Endocitózis
Ez a szinaptikus vezikulumok újrafelvételét jelenti a teljes kontaktfúziós modellben. Más tanulmányok azonban bizonyítékokat gyűjtöttek össze, amelyek arra utalnak, hogy az ilyen típusú fúzió és endocitózis nem mindig van így.
Vezikula újrahasznosítás
Úgy gondolják, hogy két vezető hatásmechanizmus felelős a szinaptikus hólyagok újrahasznosításáért: a teljes összeomlás fúziója és a "csók-fuss" módszer. Mindkét mechanizmus a szinaptikus pórus kialakulásával kezdődik, amely felszabadítja a jeladót az extracelluláris térbe. A neurotranszmitter felszabadulása után a pórusok vagy teljesen kitágulhatnak úgy, hogy a vezikulum teljesen összeomlik a szinaptikus membránban, vagy gyorsan bezáródhat, és lecsípheti a membránt, hogy fúziós csókot fusson.
Teljes összeomlás fúzió
Kimutatták, hogy az idegi szinapszisok intenzív ingerlési periódusai kimerítik a hólyagok számát, valamint növelik a sejtek kapacitását és felszínét. Ez azt jelzi, hogy miután a szinaptikus vezikulák felszabadítják neurotranszmitterük hasznos terhét, egyesülnek a sejtmembránnal, és annak részévé válnak. Miután a szinaptikus vezikulákat HRP -vel ( tormaperoxidáz ) megjelölték, Heuser és Reese megállapították, hogy a béka neuromuszkuláris csomópontjában lévő sejtmembrán egyes részeit a sejt felvette, és újra szinaptikus vezikulumokká alakította át. A vizsgálatok azt sugallják, hogy a szinaptikus hólyagok exocitózisának, visszanyerésének és reformálásának teljes ciklusa kevesebb, mint 1 percet vesz igénybe.
A teljes összeomlásos fúzió során a szinaptikus vezikula egyesül és beépül a sejtmembránba. Az új membrán kialakulása fehérje által közvetített folyamat, és csak bizonyos körülmények között fordulhat elő. Az akciós potenciál után a Ca 2+ árad a preszinaptikus membránra. A Ca 2+ a citoplazmában specifikus fehérjékhez kötődik, amelyek közül az egyik a szinaptotagmin , ami viszont kiváltja a szinaptikus vezikula és a sejtmembrán teljes fúzióját. A pórusok teljes összeolvadását SNARE fehérjék segítik . Ez a nagy fehérjecsalád ATP-függő módon közvetíti a szinaptikus vezikulák dokkolását. A szinaptikus vezikulán lévő szinaptobrevin segítségével a membránon található t-SNARE komplex, amely szintaxinból és SNAP-25-ből áll , dokkolhatja, feltöltheti és összeolvaszthatja a szinaptikus hólyagot a membránban.
Kimutatták, hogy a teljes összeomlás fúziójának mechanizmusa a botulinum és a tetanusz toxinok célpontja . A botulinum toxin proteáz aktivitással rendelkezik, amely lebontja az SNAP-25 fehérjét. Az SNAP-25 fehérje szükséges a vezikulák fúziójához, amely neurotranszmittereket, különösen acetilkolint szabadít fel. A botulinum toxin lényegében lehasítja ezeket a SNARE fehérjéket, és ezáltal megakadályozza a szinaptikus vezikulák összeolvadását a sejtes szinaptikus membránnal, és felszabadítja neurotranszmittereiket. A tetanusz toxin hasonló utat követ, de ehelyett megtámadja a szinaptobrevin fehérjét a szinaptikus hólyagon . Ezek a neurotoxinok viszont megakadályozzák a szinaptikus vezikulák teljes összeomlásának befejezését. Ennek a mechanizmusnak a hiányában izomgörcsök, bénulás és halál léphet fel.
"Csókolj és fuss"
A szinaptikus vezikulumok újrafeldolgozására szolgáló második mechanizmust csók-fuss fúziónak nevezik . Ebben az esetben a szinaptikus vezikulum "megcsókolja" a sejtmembránt, megnyitva egy kis pórusot a neurotranszmitter hasznos terhelésének átengedéséhez, majd bezárja a pórusokat, és visszavezeti a sejtbe. A csók-fuss mechanizmus hevesen vitatott téma. Hatásait megfigyelték és rögzítették; azonban a teljes összeomlású fúzióval szembeni használatának oka még mindig vizsgálódik. Feltételezések szerint a csókos futást gyakran használják a szűkös hólyagos erőforrások megőrzésére, valamint a magas frekvenciájú bemenetek kezelésére. A kísérletek azt mutatták, hogy csók-fuss események előfordulnak. Először Katz és del Castillo figyelték meg, később azt figyelték meg, hogy a csók-futtatás mechanizmus különbözik a teljes összeomlás fúziójától, mivel a sejt kapacitása nem nőtt a csók-fuss eseményekben. Ez megerősíti a csók-fuss divat ötletét, a szinaptikus vezikula felszabadítja hasznos terhét, majd elválik a membrántól.
Moduláció
Úgy tűnik tehát, hogy a sejteknek legalább két mechanizmusuk van a membrán újrahasznosításához. Bizonyos körülmények között a sejtek egyik mechanizmusról a másikra tudnak váltani. A lassú, hagyományos, teljes összeomlású fúzió uralja a szinaptikus membránt, ha a Ca 2+ szint alacsony, és a gyors csók-futás mechanizmust követik, ha a Ca 2+ szint magas.
Ales és mtsai. kimutatták, hogy az extracelluláris kalciumionok megnövekedett koncentrációja az újrahasznosítás és a szinaptikus vezikulák felszabadulásának előnyös módját váltja ki a csók-futtatás mechanizmusra kalcium-koncentrációfüggő módon. Javasolták, hogy a neurotranszmitterek szinapszisokban történő szekréciója során az exocitózis módját kalcium modulálja, hogy optimális feltételeket biztosítson a szinaptikus aktivitásnak megfelelően a kapcsolt exocitózishoz és endocitózishoz.
A kísérleti bizonyítékok azt sugallják, hogy a csók-futás a szinaptikus felszabadulás domináns módja az ingervonatok elején. Ebben az összefüggésben a csók-futás nagy hólyag-felszabadulási valószínűséget tükröz. A csók-futás gyakoriságát növeli a gyors tüzelés és az idegsejtek stimulálása is, ami arra utal, hogy az ilyen típusú felszabadulás kinetikája gyorsabb, mint a vezikulák felszabadulásának más formái.
Történelem
Az elektronmikroszkóp megjelenésével az 1950-es évek elején kiderült, hogy az idegvégződések nagy számban tartalmaznak elektron-lucens (elektronok számára átlátszó) hólyagokat. A szinaptikus vezikulum kifejezést először De Robertis és Bennett vezették be 1954-ben. Röviddel azután, hogy az adó felszabadulása a béka neuromuszkuláris csomópontjában megállapította, hogy posztszinaptikus miniatűr véglemez potenciált vált ki , amelyet a neurotranszmitter (kvantum) különálló csomagjainak felszabadításának tulajdonítottak a preszinaptikus idegvégződéstől. Így ésszerű volt feltételezni, hogy a transzmitter anyag ( acetilkolin ) olyan vezikulákban volt, amelyek szekréciós mechanizmus révén tartalmukat a szinaptikus hasadékba bocsátották (vezikulum hipotézis).
A hiányzó láncszem annak a bizonyítása volt, hogy az acetilkolin neurotranszmitter valóban szinaptikus vezikulákban található. Körülbelül tíz évvel később a szubcelluláris frakcionálási technikák agyszövetre történő alkalmazása lehetővé tette az idegvégződések ( szinaptoszómák ), majd a szinaptikus vezikulák elkülönítését az emlős agyból. Két egymással versengő laboratórium vett részt ebben a munkában, Victor P. Whittaker , a Mezőgazdasági Kutatási Tanács Állat -élettani Intézete, Babraham , Cambridge, Egyesült Királyság és Eduardo de Robertis , az Instituto de Anatomía General y Embriología, Facultad de Medicina, Buenos Aires -i Egyetem, Argentína. Whittaker munkáját, amely az acetilkolint mutatja be tengerimalac agyból származó vezikulumfrakcióban, először 1960-ban, majd részletesebben 1963-ban és 1964 - ben tették közzé, a de Robertis csoport dolgozata pedig a kötött acetil-kolin dúsítását mutatja be patkányok szinaptikus vezikulum-frakcióiban. Mindkét csoport ozmotikus sokk hatására felszabadította a szinaptikus vezikulákat az izolált szinaptoszómákból . Az acetilkolin tartalmát egy hólyagban eredetileg 1000–2000 molekula becsülték. A későbbi munka azonosította más neurotranszmitterek, például aminosavak , katecholaminok , szerotonin és ATP hólyagos lokalizációját . Később szinaptikus hólyagokat is el lehetett különíteni más szövetekből, például a felső nyaki ganglionból vagy a polip agyából. A kolinerg szinaptikus vezikulák nagymértékben tisztított frakcióinak izolálása a Torpedo elektromos szervből fontos előrelépés volt a hólyagok biokémiájának és működésének tanulmányozásában.

