Toxoplazmózis -Toxoplasmosis
| Toxoplazmózis | |
|---|---|
 | |
| T. gondii tachyzoites | |
| Különlegesség | Fertőző betegség |
| Tünetek | Gyakran semmi, terhesség alatt (születési rendellenességek) |
| Okoz | Toxoplasma gondii |
| Kockázati tényezők | Rosszul főzött ételek fogyasztása, fertőzött macska ürülékének való kitettség |
| Diagnosztikai módszer | Vérvétel, magzatvíz vizsgálat |
| Kezelés | Terhesség alatt spiramicin vagy pirimetamin / szulfadiazin és folinsav |
| Frekvencia | Az emberek akár 50%-a, évente 200 000 veleszületett toxoplazmózis |
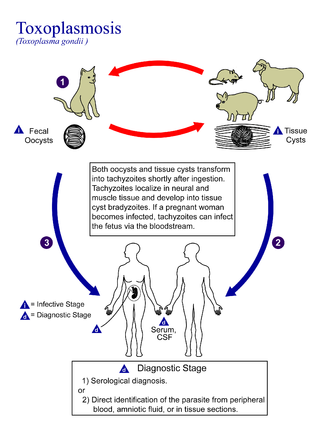
A toxoplazmózis egy parazita betegség, amelyet a Toxoplasma gondii , egy apicomplexan okoz . A toxoplazmózissal járó fertőzések számos neuropszichiátriai és viselkedési állapothoz kapcsolódnak. Alkalmanként az emberek néhány hetes vagy hónapos enyhe, influenzaszerű betegségben szenvedhetnek , mint például izomfájdalmak és érzékeny nyirokcsomók . Kis számú embernél szemproblémák alakulhatnak ki. Gyenge immunrendszerű betegeknél súlyos tünetek, például görcsrohamok és rossz koordináció léphet fel. Ha egy személy a terhesség alatt megfertőződik , a veleszületett toxoplazmózis néven ismert állapot hatással lehet a gyermekre.
A toxoplazmózis általában rosszul főzött, cisztákat tartalmazó étel elfogyasztásával , fertőzött macskaürüléknek való kitettséggel, valamint fertőzött nőtől a terhesség alatti babájáig terjed. Ritkán a betegség vérátömlesztéssel terjedhet . Másképp nem terjed el az emberek között. A parazita köztudottan csak a macskacsaládban szaporodik ivarosan . Azonban a legtöbb melegvérű állatot megfertőzheti , beleértve az embereket is. A diagnózis általában az antitestek vérének vizsgálata, vagy a magzatvíz vizsgálata terhes betegeknél a parazita DNS- ére .
A megelőzés az ételek megfelelő elkészítése és főzése. A terhes nőknek azt is javasoljuk, hogy ne takarítsák ki a macskaalomdobozokat, vagy ha muszáj, viseljenek kesztyűt és mossanak kezet utána. Az egyébként egészséges emberek kezelésére általában nincs szükség. Terhesség alatt a kezelésre spiramicin vagy pirimetamin / szulfadiazin és folinsav alkalmazható.
A világ lakosságának akár fele is fertőzött T. gondii- vel , de nincsenek tünetei. Az Egyesült Államokban az emberek hozzávetőleg 11%-a fertőződött meg, míg a világ egyes részein ez több mint 60%. Évente körülbelül 200 000 veleszületett toxoplazmózis fordul elő. Charles Nicolle és Louis Manceaux 1908-ban írta le először a szervezetet. 1941-ben megerősítették, hogy a terhesség alatt a terhes szülőről a babára terjed. Bizonyítékok vannak arra vonatkozóan, hogy a fertőzés hatással lehet az emberek viselkedésére.
jelek és tünetek
A fertőzésnek három szakasza van:
Akut
Az akut toxoplazmózis egészséges felnőtteknél gyakran tünetmentes. A tünetek azonban megnyilvánulhatnak, és gyakran influenzaszerűek : duzzadt nyirokcsomók , fejfájás, láz és fáradtság, vagy egy hónapig vagy tovább tartó izomfájdalmak . Ritka, hogy egy teljesen működő immunrendszerrel rendelkező embernél súlyos tünetek jelentkezzenek a fertőzést követően. A legyengült immunrendszerű embereknél valószínűleg fejfájás, zavartság, rossz koordináció, görcsrohamok, tüdőproblémák fordulnak elő, amelyek a tuberkulózisra vagy a Pneumocystis jiroveci tüdőgyulladásra (AIDS-ben szenvedőknél előforduló gyakori opportunista fertőzés) vagy a retina súlyos gyulladása által okozott chorioretinitisre emlékeztetnek. (szemészeti toxoplazmózis). Súlyos toxoplazmózis alakulhat ki a kisgyermekeknél és az immunhiányos betegeknél, mint például a HIV/AIDS-ben szenvedők, bizonyos típusú kemoterápiában részesülők , vagy akik nemrégiben szervátültetésen estek át . Ez károsíthatja az agyat ( encephalitis ) vagy a szemet ( nekrotizáló retinochoroiditis ). A placentán keresztül fertőzött csecsemők e problémák bármelyikével vagy orrfejlődési rendellenességekkel születhetnek, bár ezek a szövődmények ritkák az újszülötteknél. Az akut toxoplazmózist okozó toxoplazmatikus trofozoitokat tachyzoitáknak nevezik , és jellemzően különféle szövetekben és testnedvekben találhatók meg, de ritkán a vérben vagy a cerebrospinális folyadékban.
A duzzadt nyirokcsomók általában a nyakban vagy az áll alatt találhatók, majd a hónalj és az ágyék. A duzzanat a kezdeti fertőzés után különböző időpontokban jelentkezhet, fennmaradhat, és különböző ideig ismétlődik, függetlenül az antiparazita kezeléstől. Felnőtteknél általában egyetlen helyen található, de gyermekeknél több hely is gyakoribb lehet. A megnagyobbodott nyirokcsomók az esetek 60%-ában 1-2 hónapon belül megszűnnek. Az érintettek negyedének azonban 2-4 hónap, míg 8%-uk 4-6 hónapig tart. Jelentős részük (6%) csak sokkal később tér vissza a normális kerékvágásba.
Rejtett
A nyilvánvaló tünetek hiánya miatt a gazdaszervezetek könnyen megfertőződnek T. gondii- vel , és anélkül, hogy tudnák, toxoplazmózis alakul ki. Bár enyhe, influenzaszerű tünetek időnként előfordulnak az expozíciót követő első hetekben, a T. gondii fertőzés nem okoz könnyen megfigyelhető tüneteket egészséges felnőtteknél. A legtöbb immunkompetens emberben a fertőzés látens fázisba lép, amely során csak bradyzoiták ( szöveti cisztákban ) vannak jelen; ezek a szöveti ciszták, sőt elváltozások is előfordulhatnak a retinában , a tüdő alveoláris bélésében (ahol az akut fertőzés a Pneumocystis jirovecii fertőzést utánozhatja ), a szívben, a vázizomzatban és a központi idegrendszerben (CNS), beleértve az agyat is. A CNS-ben ( agyszövetben ) ciszták képződnek a T. gondii- vel való fertőzés után , és a gazdaszervezet élete végéig fennmaradnak. A legtöbb anyaméhben fertőzött csecsemőnek születéskor nincsenek tünetei, de élete későbbi szakaszában jelentkezhetnek tünetek.
A szerológiai vizsgálatok áttekintése szerint a világ lakosságának 30–50%-a volt kitéve látens toxoplazmózisnak, és krónikusan fertőzött is lehet vele, bár a fertőzések aránya országonként jelentősen eltér. Ezt a látens fertőzési állapotot a közelmúltban számos betegségteherrel , idegi elváltozásokkal és finom, nemtől függő viselkedési változásokkal, valamint a gépjármű-ütközések fokozott kockázatával hozták összefüggésbe immunkompetens emberekben.
Bőr
Bár ritka, előfordulhatnak bőrelváltozások a betegség szerzett formájában, beleértve a roseola és az erythema multiforme-szerű kitöréseket, a prurigo -szerű csomókat, a csalánkiütést és a makulopapuláris elváltozásokat . Az újszülötteknél pontszerű foltok , ecchymosisok vagy „áfonyás muffin” elváltozások lehetnek . A bőr toxoplazmózisának diagnózisa a T. gondii tachyzoit formáján alapul, amely az epidermiszben található . Az epidermisz minden szintjén megtalálható, körülbelül 6 x 2 μm, ív alakú, a mag mérete a méretének egyharmada. Elektronmikroszkóppal vagy Giemsa-festéssel lehet azonosítani , ahol a citoplazma kék, a mag vörös színű.
Ok
Parazitológia
Életciklusa során a T. gondii többféle formát vesz fel. A tachyzoiták felelősek az akut fertőzésért; gyorsan osztódnak és szétterjednek a test szöveteiben. A tachyzoiták "tachyzoic merozoiták" néven is ismertek, egy leíró kifejezés, amely pontosabban közvetíti ennek a szakasznak a parazitológiai természetét. A szaporodás után a tachyzoiták bradyzoitokká alakulnak , amelyek a látens intracelluláris szöveti cisztákban találhatók , amelyek főleg az izmokban és az agyban képződnek. A ciszták képződését részben a gazdaszervezet immunrendszerének nyomása váltja ki. A bradyzoiták (más néven bradizoiták merozoiták) nem reagálnak az antibiotikumokra. A bradyzoiták, miután kialakultak, a gazdaszervezet élettartama alatt a szövetekben maradhatnak. Egészséges gazdaszervezetben, ha egyes bradyzoiták újra aktív tachyzoitokká alakulnak, az immunrendszer gyorsan elpusztítja őket. Legyengült immunrendszerű egyénekben vagy magzatokban azonban, amelyeknek nincs fejlett immunrendszere, a tachyzoiták elszaporodhatnak, és jelentős neurológiai károsodást okozhatnak.
A parazita túlélése a gazdaszervezet túlélése és a parazita proliferációja közötti egyensúlytól függ. A T. gondii úgy éri el ezt az egyensúlyt, hogy manipulálja a gazdaszervezet immunválaszát, csökkenti a gazdaszervezet immunválaszát, és fokozza a parazita szaporodási előnyét. Miután megfertőz egy normális gazdasejtet, ellenáll a gazdaszervezet immunrendszere által okozott károsodásoknak, és megváltoztatja a gazdaszervezet immunfolyamatait. Ahogy behatol a gazdasejtbe, a parazita parazitoforikus vakuólum (PV) membránt képez a gazdasejt membránjából. A PV bekapszulázza a parazitát, és ellenáll az endolizoszomális rendszer aktivitásának, és átveheti az irányítást a gazda mitokondriumai és endoplazmatikus retikuluma felett .
Amikor először behatol a sejtbe, a parazita ROP fehérjéket szabadít fel a rhoptry organellum hagymájából . Ezek a fehérjék a sejtmagba és a PV membrán felszínére transzlokálódnak, ahol aktiválhatják a STAT útvonalakat, hogy módosítsák a citokinek expresszióját transzkripciós szinten, megkötik és inaktiválják a PV membránt, elpusztítva az IRG fehérjéket, egyéb lehetséges hatások mellett. Ezenkívül a T. gondii bizonyos törzsei egy GRA15 néven ismert fehérjét is kiválaszthatnak, aktiválva az NF-κB útvonalat, amely a korai immunválaszban felszabályozza az IL-12 gyulladást elősegítő citokint , ami valószínűleg a parazita látens fázisához vezet. A parazita azon képessége, hogy kiválasztja ezeket a fehérjéket, genotípusától függ, és befolyásolja virulenciáját.
A parazita egy anti-apoptotikus mechanizmust is befolyásol, lehetővé téve a fertőzött gazdasejtek fennmaradását és replikációját. Az apoptózis- rezisztencia egyik módszere az apoptózist elősegítő effektor fehérjék, például a BAX és a BAK megbontása . E fehérjék megzavarására a T. gondii konformációs változásokat okoz a fehérjékben, ami megakadályozza, hogy a fehérjék különböző sejtkompartmentekbe kerüljenek, ahol apoptózist indítanak el. A T. gondii azonban nem okozza az apoptózist elősegítő effektor fehérjék leszabályozását.
A T. gondii képes beindítani a gazdasejtek autofágiáját is . Ez az egészséges, nem fertőzött sejtek számának csökkenéséhez vezet, és ennek következtében kevesebb gazdasejt támadja meg a fertőzött sejteket. Wang és munkatársai kutatása azt találja, hogy a fertőzött sejtek magasabb autofagoszómához vezetnek a normál és a fertőzött sejtekben. Kutatásuk feltárja, hogy a T. gondii kalciumfüggő útvonalon keresztül gazdasejt autofágiát okoz. Egy másik tanulmány szerint a parazita közvetlenül befolyásolhatja a kalciumraktárakból felszabaduló kalciumot, amely fontos a sejtek jelátviteli folyamataihoz.
A fenti mechanizmusok lehetővé teszik, hogy a T. gondii megmaradjon egy gazdaszervezetben. Néhány korlátozó tényező a toxoplazma esetében, hogy a gazdasejtekre gyakorolt hatása gyenge immunrendszerben erősebb és mennyiségfüggő, így a gazdasejtenkénti nagyszámú T. gondii súlyosabb hatást vált ki. A gazdaszervezetre gyakorolt hatás a gazdaszervezet immunrendszerének erősségétől is függ. Az immunkompetens egyének általában nem mutatnak súlyos tüneteket, vagy egyáltalán nem mutatnak súlyos tüneteket, míg a halálos kimenetelű vagy súlyos szövődmények immunhiányos egyénekhez vezethetnek.
Kimutatták, hogy a T. gondii a MYR1 szekréciós útvonalon felszabaduló GRA28 nevű fehérjét termel, amely megzavarja a fertőzött sejtekben a génexpressziót, és olyan sejteket eredményez, amelyek dendrites sejtekként viselkednek, és nagymértékben mobilissá válnak a szervezetben .
Mivel a parazita megváltoztathatja a gazdaszervezet immunválaszát, pozitív vagy negatív hatással lehet más patogén fenyegetésekkel szembeni immunválaszra is. Ez magában foglalja, de nem kizárólagosan, a Helicobacter felis , Leishmania major vagy más paraziták, például a Nippostrongylus brasiliensis által okozott fertőzésekre adott válaszokat .
Terjedés
A toxoplazmózis általában a szájon keresztül terjed, amikor a Toxoplasma gondii oocisztákat vagy szöveti cisztákat véletlenül elfogyasztják. Veleszületett átvitel is előfordulhat anyáról magzatra. A fertőzés szilárd szervátültetési folyamat vagy hematogén őssejt-transzplantáció során is előfordulhat.
Orális átvitel történhet:
- Nyers vagy részben főtt hús, különösen sertés-, bárány- vagy vadhús lenyelése, amely Toxoplasma cisztákat tartalmaz: A fertőzések előfordulása azokban az országokban, ahol hagyományosan rosszul sült húst fogyasztanak, ezzel a átviteli móddal függ össze. A szöveti ciszták az alulsült hús kezelése utáni kéz-száj érintkezéskor is lenyelhetők, vagy a nyers hússal szennyezett kések, edények vagy vágódeszkák használatakor.
- Mosatlan gyümölcs vagy zöldség lenyelése, amely fertőzött macskaürüléket tartalmazó szennyezett talajjal érintkezett.
- Ocisztákat tartalmazó macskaürülék lenyelése : Ez történhet kéz-szájjal való érintkezéskor a kertészkedés, a macska alomdobozának tisztítása vagy a gyermekek homokozójával való érintkezés során; a parazita hónapokig képes életben maradni a környezetben.
- Kezeletlen, szűretlen víz lenyelése a víz közvetlen fogyasztása vagy ételkészítéshez való felhasználása révén.
- Nem pasztőrözött tej és tejtermékek, különösen kecsketej lenyelése.
- Nyers tenger gyümölcsei lenyelése.
A macskák a kórokozót a bélsárral választják ki a betegség elkapása után néhány hétig, általában úgy, hogy egy fertőzött köztes gazdaszervezetet esznek meg, amelybe emlősök (például rágcsálók) vagy madarak is beletartoznak. A petesejt-ürítés általában a fertőzött köztes gazdaszervezetek lenyelése utáni harmadik napon kezdődik, és hetekig tarthat. Az oociszták nem fertőzőek, amikor kiválasztódnak. Körülbelül egy nap múlva az oociszta sporulációnak nevezett folyamaton megy keresztül, és potenciálisan patogénné válik. A macskák mellett a madarak és az emlősök, köztük az emberek is a parazita köztes gazdái, és részt vesznek az átviteli folyamatban. A patogenitás azonban a T. gondii életkorától és fajától, valamint a T. gondii átviteli módjától függően változik .
A toxoplazmózis szilárd szervátültetésen keresztül is átadható. Veszélyben vannak azok a toxoplazma szeronegatív recipiensek, akik nemrégiben fertőzött Toxoplasma szeropozitív donoroktól kapnak szerveket. A látens toxoplazmózisban szenvedő szervrecipienseknél fennáll annak a veszélye, hogy a betegség újraaktiválódik a rendszerükben a szilárd szervátültetés során fellépő immunszuppresszió miatt. A hematogén őssejt-transzplantációban részesülőknél nagyobb lehet a fertőzés kockázata a hosszabb immunszuppresszió miatt.
A szív- és tüdőátültetések jelentik a legnagyobb kockázatot a toxoplazmózis fertőzésre a szívet alkotó harántcsíkolt izomzat miatt, amely cisztákat tartalmazhat, más szervek és szövetek kockázata pedig igen eltérő. Az átvitel kockázata csökkenthető a donorok és recipiensek átültetés előtti szűrésével és kezeléssel.
Terhességi óvintézkedések
A veleszületett toxoplazmózis a toxoplazmózis egy specifikus formája, amelyben a meg nem született magzat a méhlepényen keresztül fertőződik meg . A veleszületett toxoplazmózis magzati halálhoz és vetéléshez, csecsemőknél pedig hydrocephalushoz, agyi meszesedéshez és chorioretinitishez kapcsolódik , ami encephalopathiához és esetleg vaksághoz vezet. Ha egy nő először kap T. gondii fertőzést terhesség alatt, a magzat különösen veszélyeztetett. Egy egyszerű vérvétel az első szülés előtti orvosi látogatás alkalmával megállapíthatja, hogy egy nő volt-e már expozícióban, és ezért veszélyben van-e vagy sem. A pozitív antitesttiter korábbi expozíciót és immunitást jelez, és nagymértékben biztosítja a születendő magzat biztonságát.
Nem sok bizonyíték áll rendelkezésre a terhesség előtti oktatásnak a veleszületett toxoplazmózis megelőzésére gyakorolt hatására vonatkozóan. A szülők oktatása a baba születése előtt azonban hatékonynak bizonyult, mivel javíthatja az élelmiszer-, a személyi és a háziállatok higiéniáját. További kutatásokra van szükség annak megállapítására, hogy a születés előtti oktatás csökkentheti-e a veleszületett toxoplazmózist.
Azoknál a terhes nőknél, akiknek negatív antitesttiterük van, ami azt jelzi, hogy korábban nem volt kitéve T. gondii-nek , havonta javasolt szerológiai vizsgálatot végezni, mivel a terhesség alatti kezelés azoknál a nőknél, akik először voltak kitéve T. gondii-nek , drámaian csökkenti a parazita átjutásának kockázatát. a magzat. Mivel a csecsemők immunrendszere nem fejlődik ki teljesen az első életévben, és a testben kialakuló rugalmas cisztákat nagyon nehéz felszámolni protozoonellenes szerekkel, a fertőzés nagyon súlyos lehet a fiataloknál.
E kockázatok ellenére a terhes nőket a legtöbb országban nem szűrik rutinszerűen toxoplazmózisra, költséghatékonysági okokból és a generált álpozitívek nagy száma miatt; Portugália , Franciaország , Ausztria , Uruguay és Olaszország figyelemre méltó kivételt képez, és néhány regionális szűrőprogram működik Németországban , Svájcban és Belgiumban . Mivel az invazív prenatális szűrés bizonyos kockázatot jelent a magzatra nézve ( 18,5 terhességi veszteség toxoplazmózisos esetenként megelőzve), a posztnatális vagy újszülöttkori szűrést részesítik előnyben. Kivételt képeznek azok az esetek, amikor magzati rendellenességeket észlelnek, és így a szűrés célzott.
A terhes nőknek kerülniük kell a nyers hús kezelését , a nyers tej (különösen a kecsketej) fogyasztását , és azt tanácsolják nekik, hogy fajtától függetlenül ne egyenek nyers vagy rosszul főtt húst. A Toxoplasma és a macskák közötti nyilvánvaló kapcsolat miatt gyakran azt is tanácsolják, hogy kerüljék a macskaürülékkel való érintkezést, és tartózkodjanak a kertészkedéstől (a macskaürülék gyakori a kerti talajban), vagy legalább viseljen kesztyűt, ha így van. A legtöbb macska nem üríti ki aktívan az oocisztákat , mivel életük első hat hónapjában fertőződik meg, amikor is rövid ideig (1-2 hétig) ürítik az oocisztákat. Ezek az oociszták azonban a talajba temetkeznek, spórálódnak és több hónaptól több mint egy évig terjedő időszakon keresztül fertőzőképes marad. Számos tanulmány kimutatta, hogy a macskával egy háztartásban élés nem jelent jelentős kockázati tényezőt a T. gondii fertőzés szempontjából, bár a több cicával való együttélésnek van némi jelentősége.
2006-ban egy cseh kutatócsoport felfedezte, hogy a magas toxoplazmózis antitestekkel rendelkező nőknél lényegesen nagyobb valószínűséggel születnek fiúgyermekek, mint kislányoknál. A legtöbb populációban a születési arány a fiúk 51%-a körül mozog, de a T. gondii- vel fertőzötteknél akár 72% az esélye a fiúgyermeknek.
Diagnózis
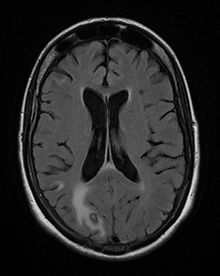
A toxoplazmózis diagnózisa emberben biológiai, szerológiai, szövettani vagy molekuláris módszerekkel, illetve a fentiek valamilyen kombinációjával történik. A toxoplazmózist nehéz megkülönböztetni az elsődleges központi idegrendszeri limfómától . Számos más fertőző betegséget utánoz, így a klinikai tünetek nem specifikusak, és nem eléggé jellemzőek a biztos diagnózishoz. Ennek eredményeként az alternatív diagnózis lehetőségét alátámasztja az antimikrobiális terápia ( pirimetamin , szulfadiazin és folinsav ( USAN : leucovorin)) sikertelen kísérlete , azaz ha a gyógyszerek nem fejtenek ki klinikai hatást, és nem javítanak az ismételt képalkotáson.
A T. gondii a vérben , a magzatvízben vagy a cerebrospinális folyadékban is kimutatható polimeráz láncreakció segítségével . A T. gondii inaktív cisztaként létezhet a gazdaszervezetben, amely valószínűleg elkerülné a felismerést.
A szerológiai vizsgálattal kimutatható a T. gondii antitestek a vérszérumban, olyan módszerekkel, mint a Sabin–Feldman festékteszt (DT), az indirekt hemagglutinációs vizsgálat , az indirekt fluoreszcens antitest vizsgálat (IFA) , a direkt agglutinációs teszt , a latex agglutinációs teszt (LAT). ), az enzimhez kötött immunszorbens teszt (ELISA) és az immunszorbens agglutinációs teszt (IAAT).
Az IgG antitest mérésére leggyakrabban használt tesztek a DT, az ELISA, az IFA és a módosított közvetlen agglutinációs teszt. Az IgG antitestek általában a fertőzést követő egy-két héten belül jelennek meg, egy-két hónapon belül tetőznek, majd különböző ütemben csökkennek. A toxoplazma IgG antitestek általában egész életen át fennmaradnak, ezért jelen lehetnek a véráramban akár a jelenlegi, akár korábbi fertőzés eredményeként.
Bizonyos mértékig az akut toxoplazmózis fertőzések megkülönböztethetők a krónikus fertőzésektől IgG aviditásteszt segítségével , amely az ELISA egy változata. A fertőzésre adott első válaszként a toxoplazma-specifikus IgG alacsony affinitást mutat a toxoplazma antigénhez; a következő hetekben és hónapokban megnő az IgG affinitása az antigénhez. Az IgG aviditási teszt alapján, ha a fertőzött egyén IgG-jének nagy affinitása van, az azt jelenti, hogy a fertőzés három-öt hónappal a vizsgálat előtt kezdődött. Ez különösen hasznos veleszületett fertőzés esetén, ahol a terhesség állapota és a terhességi kor a fertőzés időpontjában határozza meg a kezelést.
Az IgG-vel ellentétben az IgM antitestek felhasználhatók akut fertőzés kimutatására, de általában nem krónikus fertőzések kimutatására. Az IgM antitestek hamarabb megjelennek a fertőzés után, mint az IgG antitestek, és gyorsabban tűnnek el, mint az IgG antitestek a gyógyulás után. A legtöbb esetben a T. gondii -specifikus IgM antitestek először körülbelül egy héttel az elsődleges fertőzés megszerzése után mutathatók ki, és 1-6 hónapon belül csökkennek; A fertőzöttek 25%-a negatív a T. gondii -specifikus IgM-re hét hónapon belül. Az IgM azonban hónapokkal vagy évekkel a fertőzés után, a krónikus fázisban kimutatható, és az akut fertőzés álpozitívumai lehetségesek. Az IgM antitest mérésére leggyakrabban használt tesztek a kettős szendvics IgM-ELISA , az IFA teszt és az immunszorbens agglutinációs vizsgálat (IgM-ISAGA). A kereskedelmi tesztkészletek gyakran alacsony specifitásúak, és a jelentett eredményeket gyakran félreértelmezik.
2021-ben húsz kereskedelmi forgalomban kapható toxoplazma elleni IgG-tesztet értékeltek ki szisztematikus áttekintésben , összehasonlítva egy elfogadott referenciamódszerrel. Legtöbbjük enzim-immunoassay volt, amit agglutinációs tesztek, immunkromatográfiás tesztek és Western-Blot vizsgálat követett. Az IgG vizsgálatok átlagos érzékenysége 89,7% és 100% között volt a standard titereknél és 13,4% és 99,2% között volt az alacsony IgG titereknél. Néhány tanulmány rámutatott arra, hogy egyes módszerek, különösen a WB képesek az IgG korai kimutatására az elsődleges fertőzés után. Az IgG vizsgálatok specificitása általában magas volt, 91,3% és 100% között változott; és 99%-nál magasabb a legtöbb EIA vizsgálatnál. A pozitív prediktív érték (PPV) nem volt megkülönböztető mutató a módszerek között, míg a negatív prediktív értékek (NPV) között jelentős eltéréseket (87,5–100%) jelentettek, amely kulcsparaméter, amely a Toxoplasma fertőzés végleges kizárásának képességét értékeli . az opportunista fertőzések által veszélyeztetett betegek.
Veleszületett
A veleszületett toxoplazmózis diagnosztizálására vonatkozó ajánlások a következők: a magzatvíz vizsgálatán és ultrahangos vizsgálatokon alapuló prenatális diagnózis ; újszülöttkori diagnózis a méhlepény és a köldökzsinórvér molekuláris vizsgálatán , valamint az anya-gyermek összehasonlító szerológiai teszteken és a születéskor végzett klinikai vizsgálaton alapuló diagnózis; valamint a koragyermekkori diagnózis neurológiai és szemészeti vizsgálatokon, valamint az első életévben végzett szerológiai felmérésen alapul. Terhesség alatt háromhetes időközönként szerológiai vizsgálat javasolt.
Annak ellenére, hogy a toxoplazmózis diagnózisa nagymértékben támaszkodik a specifikus anti- toxoplazma immunglobulin szerológiai kimutatására, a szerológiai vizsgálatnak vannak korlátai. Például előfordulhat, hogy nem képes kimutatni a T. gondii fertőzés aktív fázisát, mert előfordulhat, hogy a specifikus anti- Toxoplasma IgG vagy IgM csak néhány hét fertőzés után termelődik. Ennek eredményeként egy terhes nő tesztje negatív lehet a T. gondii fertőzés aktív fázisában, ami fel nem ismert, és ezért kezeletlen veleszületett toxoplazmózishoz vezethet. Ezenkívül előfordulhat, hogy a teszt nem mutat ki T. gondii fertőzést immunhiányos betegeknél, mivel a specifikus anti- Toxoplasma IgG vagy IgM titere nem emelkedik az ilyen típusú betegekben.
Számos PCR-alapú technikát fejlesztettek ki a toxoplazmózis diagnosztizálására olyan klinikai minták felhasználásával, amelyek magukban foglalják a magzatvíz, a vér , a cerebrospinális folyadék és a szövetbiopsziát . A legérzékenyebb PCR-alapú technika a beágyazott PCR , amelyet a PCR-termékek hibridizációja követ. Ezeknek a technikáknak a fő hátránya, hogy időigényesek, és nem szolgáltatnak mennyiségi adatokat.
A valós idejű PCR hasznos a kórokozók kimutatásában, a génexpresszióban és -szabályozásban, valamint az allél diszkriminációban. Ez a PCR-technika a Taq DNS polimeráz 5' nukleáz aktivitását használja fel egy nem kiterjeszthető, fluoreszcenciával jelölt hibridizációs próba hasítására a PCR kiterjesztési fázisa során. Egy második fluoreszcens festék, például a 6-karboxi-tetrametil-rodamin, kioltja az érintetlen próba fluoreszcenciáját. A hibridizációs próba nukleázos hasítása a PCR során felszabadítja a kioltás hatását, ami a PCR termék mennyiségével arányos fluoreszcencia növekedést eredményez, amit szekvenciadetektorral lehet nyomon követni.
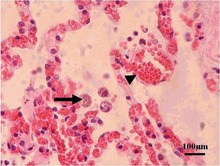
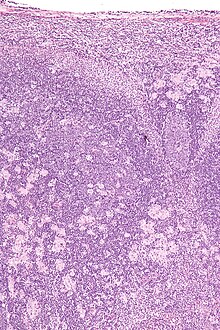
A Toxoplasma által érintett nyirokcsomók jellegzetes elváltozásokkal rendelkeznek, beleértve a rosszul körülhatárolt reaktív csíraközpontokat , a monocitoid B-sejtek klasztereit és a szétszórt epithelioid hisztiocitákat .
A veleszületett toxoplazmózis klasszikus triásza a következőket tartalmazza: chorioretinitis , hydrocephalus és intracranialis arteriosclerosis . Egyéb következmények közé tartozik a szenzorineurális süketség, görcsrohamok és értelmi fogyatékosság.
A veleszületett toxoplazmózis is befolyásolhatja a gyermek hallását. Az újszülöttek 30%-ának van valamilyen fokú szenzorineurális halláskárosodása. A gyermek kommunikációs készségei is érintettek lehetnek. Egy 2010-ben közzétett tanulmányban 106 beteget vizsgáltak, akik mindegyike részesült toxoplazmózis kezelésében 2,5 hónap előtt. Ennek a csoportnak 26,4%-a jelentkezett nyelvi zavarokkal.
Kezelés
A kezelés súlyos egészségügyi problémákkal küzdők számára javasolt, például olyan HIV- fertőzöttek számára , akiknek CD4 -száma 200 sejt/mm 3 alatt van . A trimetoprim/szulfametoxazol a választott gyógyszer a toxoplazmózis megelőzésére, de nem az aktív betegségek kezelésére. Egy 2012-es tanulmány ígéretes új módszert mutat be a betegség aktív és látens formájának kezelésére két endochin-szerű kinolon alkalmazásával .
Akut
Az akut toxoplazmózis kezelésére felírt gyógyszerek a következők:
- Pirimetamin – malária elleni gyógyszer
-
Szulfadiazin – egy antibiotikum , amelyet pirimetaminnal kombinálva alkalmaznak a toxoplazmózis kezelésére
- A kombinált terápiát általában folsav-kiegészítőkkel adják a thrombocytopenia előfordulásának csökkentése érdekében .
- A kombinált terápia a HIV-fertőzés hátterében a leghasznosabb.
- Klindamicin
- Spiramycin – egy antibiotikum, amelyet leggyakrabban terhes nőknél alkalmaznak gyermekeik fertőzésének megelőzésére.
(más antibiotikumokat, mint például a minociklint , mentőterápiaként használták ).
Terhesség alatti fertőzés esetén a spiramicin az első és a második trimeszter elején, míg a pirimetamin/szulfadiazin és a leukovorin a második és harmadik trimeszter végén javasolt.
Rejtett
A látens toxoplazmózisban szenvedőknél a ciszták immunisak ezekre a kezelésekre, mivel az antibiotikumok nem jutnak el kellő koncentrációban a bradyzoitákhoz .
A látens toxoplazmózis kezelésére felírt gyógyszerek a következők:
- Atovaquone – egy antibiotikum, amelyet AIDS- betegek Toxoplasma cisztáinak elpusztítására használnak
- Klindamicin – egy antibiotikum, amely atovakvonnal kombinálva optimálisan elpusztította a cisztákat egerekben
Veleszületett
Ha egy terhes nőnél akut toxoplazmózist diagnosztizálnak, amniocentézissel megállapítható, hogy a magzat fertőzött-e vagy sem. Amikor egy terhes nőnél akut toxoplazmózis alakul ki, a tachyzoiták körülbelül 30%-os eséllyel bejutnak a placenta szövetébe, és onnan bejutnak és megfertőzik a magzatot. A fertőzés idején a terhességi kor növekedésével a magzati fertőzés esélye is nő.
Ha a parazita még nem érte el a magzatot, a spiramicin segíthet megelőzni a placentán történő átvitelt. Ha a magzat fertőzött, a terhes nő az első trimesztert követően pirimetaminnal és szulfadiazinnal , folinsavval kezelhető . Az első trimeszter után kezelik őket, mivel a pirimetamin antifolát hatású, a folsav hiánya pedig megzavarhatja a magzati agy kialakulását és thrombocytopeniát okozhat . A terhesség korábbi szakaszaiban bekövetkezett fertőzés a magzati és újszülöttkori rosszabb kimenetelekkel korrelál, különösen akkor, ha a fertőzést nem kezelik.
Azoknál az újszülötteknél, akik 12 hónapos posztnatális toxoplazmózis elleni kezelésen esnek át, kicsi az esélye a szenzorineurális halláskárosodásnak. A veleszületett toxoplazmózisban szenvedő gyermekek kezelésének mérföldköveire vonatkozó információkat készítettek ehhez a csoporthoz.
Járványtan
A T. gondii fertőzések világszerte előfordulnak, bár a fertőzések aránya országonként jelentősen eltér. A fogamzóképes korú nők esetében egy 44 országban végzett 99 tanulmányból álló felmérés szerint a legmagasabb előfordulási területek Latin-Amerikában (körülbelül 50–80%), Kelet- és Közép-Európa egyes részein (körülbelül 20–60%), valamint a Közel-Keleten találhatók . körülbelül 30-50%), Délkelet-Ázsia egyes részei (kb. 20-60%) és Afrika egyes részei (kb. 20-55%).
Az Egyesült Államokban a National Health and Nutrition Examination Survey (NHANES ) 1999 és 2004 közötti adatai szerint az Egyesült Államokban született 12–49 évesek 9,0%-a volt szeropozitív a T. gondii elleni IgG antitestekre , szemben a 14,1%-kal. mérve az NHANES 1988–1994. Az 1999–2004-es felmérésben az Egyesült Államokban született 15–44 éves nők 7,7%-a és a külföldön született nők 28,1%-a volt szeropozitív T. gondii- re. A szeroprevalencia csökkenésének tendenciáját számos tanulmány figyelte meg az Egyesült Államokban és számos európai országban. A Toxoplasma gondii-t az élelmiszer -eredetű halálozások második vezető okának, az élelmiszerekkel összefüggő kórházi kezelések negyedik vezető okának tekintik az Egyesült Államokban.
A toxoplazmózisért felelős protiszta a T. gondii . A T. gondii három fő típusa felelős a toxoplazmózis mintázataiért világszerte. Vannak I, II és III típusok. A T. gondii e három típusa eltérő hatást fejt ki bizonyos gazdaszervezetekre, főként egerekre és emberekre a genotípusbeli eltéréseik miatt.
- I. típus: virulens egerekben és emberekben, AIDS-ben szenvedőknél észlelhető .
- II. típus: nem virulens egerekben, virulens emberekben (főleg Európában és Észak-Amerikában), AIDS-ben szenvedőknél észlelhető.
- III. típus: nem virulens egerekben, virulens főleg állatokban, de kisebb mértékben emberben is.
A jelenlegi szerotipizálási technikák csak az I. vagy III. típusú parazitákat tudják elkülöníteni a II. típusú parazitáktól.
Mivel a parazita különös veszélyt jelent a magzatra, ha terhesség alatt megfertőződik, a T. gondii-vel kapcsolatos globális epidemiológiai adatok nagy része fogamzóképes korú nőkön végzett szeropozitivitási tesztekből származik. A szeropozitivitási tesztek a T. gondii elleni antitestek jelenlétét keresik a vérben, így bár a szeropozitivitás garantálja, hogy valaki ki volt téve a parazitának, nem feltétlenül garantálja, hogy krónikusan fertőzött.
Történelem
A Toxoplasma gondii-t először Nicolle és Manceaux írta le 1908-ban Tunéziában, és egymástól függetlenül a brazil Splendore. Splendore egy nyúlon, míg Nicolle és Manceaux egy észak-afrikai rágcsálónál, a gundinál ( Ctenodactylus gundi )számolt be a protozoonról . 1909-ben Nicolle és Manceaux megkülönböztette a protozoont a Leishmania- tól . Nicolle és Manceaux ezután Toxoplasma gondii- nek nevezték elfertőző stádiumának ívelt alakja után (görög gyökér " toxon " = íj).
Az első feljegyzett veleszületett toxoplazmózis eset 1923-ban volt, de nem azonosították, hogy T. gondii okozta volna . Janků (1923) részletesen leírta egy 11 hónapos kisfiú boncolási eredményeit, aki hidrocephalusszal került kórházba . A fiúnál a toxoplazmózis klasszikus jelei voltak, beleértve a chorioretinitist (a szem érhártyájának és retinájának gyulladása). A szövettan számos „sporocitát” tárt fel, bár Janků nem azonosította ezeket T. gondiiként .
Csak 1937-ben került sor a T. gondii első részletes tudományos elemzésére a vírusok elemzésére korábban kifejlesztett technikák felhasználásával. 1937-ben Sabin és Olitsky laboratóriumi majmokon és egereken elemezték a T. gondii-t . Sabin és Olitsky kimutatta, hogy a T. gondii obligát intracelluláris parazita, és a T. gondii-vel szennyezett szövettel táplált egerek is elkapták a fertőzést. Így Sabin és Olitsky kimutatta, hogy a T. gondii állatok között átvihető kórokozó .
A T. gondii-t először 1939-ben írták le emberi kórokozóként a New York -i Babies Hospitalban . Wolf, Cowen és Paige T. gondii fertőzést azonosított egy császármetszéssel teljes időre világra hozott csecsemőnél . A csecsemőnél három napon belül görcsrohamok jelentkeztek, és mindkét szemében chorioretinitis alakult ki. A csecsemő ezután agyvelőgyulladást kapott, és egy hónapos korában meghalt. Wolf, Cowen és Paige agyszöveti elváltozásokból izolálták a T. gondii-t . Az agy- és gerincvelőminták koponyán belüli injekciója egerekbe, nyulakhoz és patkányokba agyvelőgyulladást okozott az állatokban. Wolf, Cowen és Page további eseteket is áttekintettek, és arra a következtetésre jutottak, hogy a T. gondii felismerhető tüneteket produkált, és átadható anyáról gyermekre.
Az első felnőttkori toxoplazmózis esetet 1940-ben jelentették, neurológiai tünetek nélkül. Pinkerton és Weinman Toxoplasma jelenlétéről számoltak be egy 22 éves perui férfinál, aki egy későbbi bakteriális fertőzésben és lázban halt meg.
1948-ban Sabin és Feldman szerológiai festéktesztet készítettek, amely a páciens antitesteinek a Toxoplasma festődését megváltoztató képességén alapult . A Sabin Feldman festékteszt ma már az arany standard a Toxoplasma fertőzés azonosítására.
A toxoplazma átvitelét nyers vagy rosszul főtt hús fogyasztásával Desmonts et al. 1965-ben Párizsban. Desmonts megfigyelte, hogy a nyers marha- vagy lóhús terápiás fogyasztása egy tuberkulóziskórházban a Toxoplasma antitestek évi 50%-os növekedésével járt együtt . Ez azt jelenti, hogy több T. gondii terjedt át a nyers húson keresztül.
1974-ben Desmonts és Couvreur kimutatta, hogy a fertőzés az első két trimeszterben okozza a legtöbb kárt a magzatban, hogy a fertőzés attól függ, hogy az anyák mikor fertőződtek meg a terhesség alatt, hogy a terhesség előtt antitestekkel rendelkező anyák nem továbbították a fertőzést a magzatra, és hogy a spiramicin csökkentette az átvitelt a magzatra.
A toxoplazma az 1970-es években kapott nagyobb figyelmet a szerv- vagy csontvelő-átültetések után alkalmazott immunszuppresszáns kezelések térnyerésével és az 1980-as évek AIDS- járványával. A csökkent immunrendszerű betegek sokkal fogékonyabbak a betegségekre.
Társadalom és kultúra
"Őrült macska hölgy"
Az "őrült macska-hölgy szindróma" kifejezést a hírszervezetek alkották meg, hogy leírják azokat a tudományos eredményeket, amelyek a Toxoplasma gondii parazitát számos mentális zavarhoz és viselkedési problémához kötik. A gyermekkori macskatartás és a skizofrénia későbbi kialakulása közötti feltételezett összefüggés arra utalt, hogy további vizsgálatokra van szükség a gyermekek kockázati tényezőjének meghatározásához; a későbbi vizsgálatok azonban kimutatták, hogy a T. gondii nem volt okozó tényező a későbbi pszichózisokban. A kutatók azt is megállapították, hogy a macskatartás nem növeli jelentősen a T. gondii fertőzés kockázatát terhes nőknél.
Az őrült macska-hölgy szindróma kifejezés sztereotípiákra és népszerű kulturális utalásokra is támaszkodik. Úgy keletkezett, hogy a fent említett csapások előfordulását a lakosság körében észlelték. A macskahölgy egy olyan nő kulturális sztereotípiája, aki kényszeresen gyűjti és gyűlöli a macskákat. Jaroslav Flegr biológus annak az elméletnek a híve, hogy a toxoplazmózis befolyásolja az emberi viselkedést.
Nevezetes esetek
- A teniszező Arthur Ashe toxoplazmózis miatt neurológiai problémákat okozott (és később kiderült, hogy HIV -pozitív).
- Merritt Butrick színész HIV-pozitív volt, és toxoplazmózisban halt meg az amúgy is legyengült immunrendszere következtében.
- Pedro Zamorát , a reality televíziós személyiséget és HIV/AIDS aktivistát toxoplazmózissal diagnosztizálták, mivel immunrendszerét a HIV legyengítette.
- François herceg, Clermont grófja , Franciaország trónjának esélyesének veleszületett toxoplazmózisa volt; fogyatékossága miatt figyelmen kívül hagyták az utódlási sorban.
- Leslie Ash színésznő toxoplazmózist kapott a terhesség második hónapjában.
- Sebastian Coe brit középtávfutó 1983-ban toxoplazmózist kapott, amelyet valószínűleg egy macska terjesztett, miközben Olaszországban edzett.
- Martina Navratilova teniszező toxoplazmózist tapasztalt az 1982-es US Openen .
Más állatok
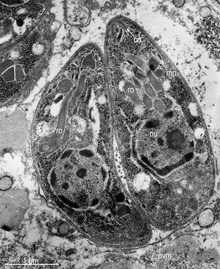
Bár a T. gondii képes gyakorlatilag az összes melegvérű állatot megfertőzni, a fertőzés fogékonysága és aránya igen eltérő a különböző nemzetségek és fajok között . Ugyanazon faj populációiban a fertőzések aránya is nagymértékben változhat a hely, az étrend és más tényezők különbségei miatt.
Bár a T. gondii fertőzést több ázsiai főemlősfajnál is megfigyelték, a T. gondii antitestek szeroprevalenciáját először Srí Lanka szigetén endemikus makákókban ( Macaca sinica ) találták.
Az ausztrál erszényes állatok különösen érzékenyek a toxoplazmózisra. Wallabies , koalák , wombats , pademelons és kis dasyuridák elpusztulhatnak tőle, a keleti sávos bandicoots általában a fertőzést követő 3 héten belül elpusztul.
Becslések szerint világszerte a vaddisznók 23%-a szeropozitív T. gondii- ra . A szeroprevalencia az egész világon változó, a legmagasabb szeroprevalencia Észak-Amerikában (32%) és Európában (26%), a legalacsonyabb Ázsiában (13%) és Dél-Amerikában (5%). A magasabb szélességi fokon elhelyezkedő földrajzi régiók és a melegebb, nedves éghajlatú régiók a T. gondii fokozott szeroprevalenciájával járnak együtt a vaddisznók körében. A T. gondii- vel fertőzött vaddisznó potenciális egészségügyi kockázatot jelent a húsukat fogyasztó emberek számára.
Állatállomány
Az állatállomány közül a sertéseknél, a juhoknál és a kecskéknél a legmagasabb a krónikus T. gondii fertőzés aránya . A T. gondii elterjedtsége a hústermelő állatokban nagyon változó mind az országokon belül, mind az országok között, és kimutatták, hogy a fertőzések arányát drámai módon befolyásolják az eltérő gazdálkodási és gazdálkodási gyakorlatok. Például a szabadban vagy szabadon tartott állatokat nagyobb a fertőzésveszély, mint a zárt térben vagy kereskedelmi elzárásban tartott állatokat .
Disznók
Világszerte 3–71,43% között van az életképes parazitákat hordozó sertések aránya, az Egyesült Államokban pedig ( egereken vagy macskákon végzett biológiai vizsgálattal ) 92,7% és 0% között van, a gazdaságtól vagy a gazdaságtól függően. csorda. A szeroprevalencia felmérései ( T. gondii antitestek a vérben) gyakoribbak, és az ilyen mérések a sertéseknél világszerte tapasztalható magas relatív szeroprevalenciára utalnak. Megállapították, hogy az újszülött malacok a súlyosság teljes tartományát átélik, beleértve a halvaszületésig történő progressziót is . Ezt különösen az alapozó Thiptara et al. 2006-ban három halvaszületett alomról számoltak be, és hat Thaiföldön él. Ez a megfigyelés nemcsak ebben az országban, hanem a sertéstenyésztésben a toxoplazmózis elleni küzdelemben is releváns volt világszerte.
Juh
A sertések mellett a juhok és a kecskefélék a leggyakrabban fertőzött, járványügyi jelentőségű állatállományok közé tartoznak az emberi fertőzések szempontjából. Az életképes T. gondii prevalenciáját a juhszövetben (biológiai vizsgálattal) 78%-ra mérték az Egyesült Államokban, és egy 2011-es, az Egyesült Államokban fogyasztásra szánt kecskék körében végzett felmérés 53,4%-os szeroprevalenciát mutatott ki.
Csirkék
A szabadban való kitettség hiánya miatt a nagyszabású beltéri elzárásban nevelt csirkék általában nem fertőződnek meg T. gondii- vel . A szabadon tartott vagy háztáji csirkék sokkal gyakrabban fertőződnek meg. Az Egyesült Államokban szabadon tartott csirkéken végzett felmérés szerint előfordulási gyakorisága 17–100% a gazdaságtól függően. Mivel a csirkehúst fogyasztás előtt általában alaposan megfőzik, a baromfit általában nem tekintik az emberi T. gondii fertőzés jelentős kockázati tényezőjének.
Marha
Bár a szarvasmarhák és a bivalyok megfertőződhetnek T. gondii -vel , a parazita általában eltűnik vagy kimutathatatlan szintre csökken az expozíciót követő néhány héten belül. A szöveti ciszták ritkán fordulnak elő a bivalyhúsban vagy a marhahúsban, és ezeknek az állatoknak a húsa alacsony kockázatúnak tekinthető az életképes paraziták számára.
Lovak
A lovakat rezisztensnek tekintik a krónikus T. gondii fertőzéssel szemben. Az export céljából levágott amerikai lovakból azonban életképes sejteket izoláltak, és Franciaországban a súlyos emberi toxoplazmózist epidemiológiailag összefüggésbe hozták a lóhús fogyasztásával .
Házi macskák
1942-ben a New York állambeli Middletownban diagnosztizálták és jelentették az első macska toxoplazmózist egy házimacskában. A kutatók oocisztákat izoláltak a macska ürülékéből, és megállapították, hogy az oociszták akár 12 hónapig is fertőzőek lehetnek a környezetben.
A T. gondii szeroprevalenciáját házimacskákban világszerte 30-40%-ra becsülik, és jelentős földrajzi eltéréseket mutat . Az Egyesült Államokban nem készült hivatalos nemzeti becslés, de a helyi felmérések 16% és 80% között változnak. Egy 2012-es felmérés 445 fajtatiszta kedvtelésből tartott macskával és 45 menhelyi macskával Finnországban 48,4 %-os általános szeroprevalenciát mutatott ki, míg egy 2010-es felmérés az egyiptomi gízai elvadult macskák körében 97,4%-os szeroprevalencia arányt mutatott ki. Egy másik kolumbiai felmérés 89,3%-os szeroprevalenciát mutatott ki, míg egy kínai ( Guangdong ) tanulmány mindössze 2,1%-os prevalenciát talált.
A házimacskák T. gondii fertőzésének aránya nagymértékben változik a macskák étrendjétől és életmódjától függően. A táplálékra vadászó elvadult macskák nagyobb valószínűséggel fertőződnek meg, mint a házimacskák, és természetesen a T. gondii -vel fertőzött zsákmány, például madarak és kisemlősök előfordulási gyakoriságától is függ .
A legtöbb fertőzött macska életében csak egyszer, körülbelül egy-két hétig ürít ki oocisztákat. Ez a leválás több millió oocisztát szabadíthat fel, amelyek mindegyike képes terjedni és hónapokig túlélni. Becslések szerint a macskák 1%-a bármikor aktívan irtja az oocisztákat.
A macskapopulációt nehéz ellenőrizni a fertőzött oocisztákkal a hatékony vakcina hiánya miatt. Ez a legtöbb esetben továbbra is kihívást jelent, és a könnyen elérhető programok hatékonysága megkérdőjelezhető.
Rágcsálók
A T. gondii fertőzésről kimutatták, hogy megváltoztatja az egerek és patkányok viselkedését oly módon, hogy úgy gondolják, hogy növeli a rágcsálók esélyét, hogy macskák áldozatává váljanak. A fertőzött rágcsálóknál csökken a macskaszagokkal szembeni veleszületett idegenkedés; Míg a nem fertőzött egerek és patkányok általában elkerülik a macska vizeletével vagy macska testszagával jelölt területeket, ez az elkerülés csökken vagy megszűnik a fertőzött állatoknál. Ezen túlmenően egyes bizonyítékok arra utalnak, hogy ez az idegenkedés elvesztése a macskaszagokra jellemző: ha két ragadozószag (macska vagy nerc ) közül választhatnak, a fertőzött rágcsálók lényegesen erősebben preferálják a macskaszagokat, mint a nem fertőzött kontrollok .
Rágcsálókban a T. gondii által kiváltott viselkedési változások a megfigyelt viselkedéssel összefüggő neuronok epigenetikai átépülésén keresztül következnek be; például módosítja az epigenetikus metilációt , hogy az arginin vazopresszinnel rokon gének hipometilációját indukálja a mediális amygdalában, hogy nagymértékben csökkentse a ragadozók ellen való averziót. Hasonló epigenetikailag indukált viselkedési változásokat figyeltek meg a függőség egérmodelljeiben is, ahol a hisztonmódosító enzimek expressziójában bekövetkezett változások a génkiütésen vagy az enzimgátláson keresztül specifikus neuronokban változásokat idéztek elő a kábítószerrel kapcsolatos viselkedésekben. Úgy tűnik, hogy a kérgi asztrocitákban széles körben elterjedt hiszton-lizin acetiláció egy másik epigenetikai mechanizmus, amelyet a T. gondii alkalmaz .
A T. gondii -vel fertőzött rágcsálók számos viselkedésbeli változást mutatnak a macskaszagokra adott megváltozott reakciókon túl. A parazitával fertőzött patkányok fokozott aktivitást és csökkent neofób viselkedést mutatnak. Hasonlóképpen, a fertőzött egerek a kísérleti tesztek során változásokat mutatnak a mozgás és a felfedező viselkedés mintáiban . Ezek a minták magukban foglalják a nagyobb távolságok megtételét, a nagyobb sebességgel való mozgást, a hosszabb ideig tartó gyorsítást és a csökkentett szünetidőt, amikor új arénában helyezkednek el. Kimutatták, hogy a fertőzött rágcsálóknál alacsonyabb a szorongás , olyan hagyományos modellek alkalmazásával, mint a magasított plusz labirintusok , nyílt terepen lévő arénák és a szociális interakciós tesztek.
tengeri emlősök
A Kaliforniai Egyetem, Davis tanulmánya holt tengeri vidrákon 1998 és 2004 között gyűjtött, és megállapította, hogy az állatok 13%-ánál toxoplazmózis okozta a halálozást. Az édesvíz óceánba való kiáramlásának közelsége jelentős kockázati tényező volt. A macskaürülékből származó oociszták lenyelése a legvalószínűbb végső forrás. A vadmacska-ürüléket és a WC-ből leöblített házimacskák alom felszíni elfolyása az oociszták lehetséges forrása. Ugyanezek a források vezethették be a toxoplazmózis fertőzést a veszélyeztetett hawaii szerzetesfókára is . A parazitával való fertőzés legalább négy hawaii szerzetesfóka halálához járult hozzá. Egy hawaii szerzetesfóka T. gondii- vel való fertőzését először 2004-ben észlelték. A parazita elterjedése fenyegeti ennek a rendkívül veszélyeztetett úszólábúnak a gyógyulását. A parazitákat delfinekben és bálnákban találták meg. Black és Massie kutatók úgy vélik, hogy a szardella, amely a torkolatokból a nyílt óceánba jut, elősegítheti a betegség terjedését.
Óriáspanda
Toxoplasma gondii-t jelentettek egy kínai állatkertben tartott óriáspanda halálának okaként , aki 2014-ben akut gyomor-bélhurutban és légúti betegségben halt meg . Bár látszólag anekdotikusnak tűnik, ez a jelentés hangsúlyozza, hogy minden melegvérű faj valószínűleg megfertőződött T. gondii- vel , beleértve a veszélyeztetett fajokat is, mint például az óriáspandát.
Kutatás
A T. gondii okozta krónikus fertőzést hagyományosan tünetmentesnek tekintik normál immunfunkciójú embereknél. Egyes bizonyítékok arra utalnak, hogy a látens fertőzés finoman befolyásolhatja az emberi viselkedések és hajlamok széles skáláját, és a fertőzés számos pszichiátriai vagy neurológiai rendellenességre való hajlamot vagy intenzitását megváltoztathatja.
A legtöbb jelenlegi tanulmányban, ahol pozitív korrelációt találtak a T. gondii antitesttiterek és bizonyos viselkedési tulajdonságok vagy neurológiai rendellenességek között, a T. gondii szeropozitivitási tesztjeit a vizsgált betegség vagy viselkedési jellemző megjelenése után végzik el; vagyis gyakran nem világos, hogy a parazitával való fertőzés növeli-e egy bizonyos tulajdonság vagy rendellenesség előfordulásának esélyét, vagy ha egy bizonyos tulajdonság vagy rendellenesség növeli a parazitával való fertőzés esélyét. Bizonyos viselkedési jellemzőkkel vagy neurológiai rendellenességekkel küzdő egyének csoportjai bizonyos viselkedési tendenciákat mutathatnak, amelyek növelik a T. gondii- vel való érintkezés és fertőzés valószínűségét ; ennek eredményeként nehéz megerősíteni az okozati összefüggést a T. gondii fertőzések és a kapcsolódó neurológiai rendellenességek vagy viselkedési jellemzők között.
Mentális egészség
Egyes bizonyítékok a T. gondii-t a skizofréniához kapcsolják . Két 2012-es metaanalízis megállapította, hogy a T. gondii elleni antitestek aránya skizofréniában 2,7-szer magasabb volt, mint a kontrollokban. A T. gondii antitest-pozitívitást ezért köztes kockázati tényezőnek tekintették más ismert kockázati tényezőkhöz képest. Figyelmeztetések közé tartozik, hogy az antitest-tesztek nem mutatják ki közvetlenül a toxoplazmózist, a legtöbb skizofréniában szenvedő ember nem rendelkezik toxoplazmózis elleni antitestekkel, és előfordulhat, hogy a publikáció torzítja . Míg e vizsgálatok többségében már skizofréniával diagnosztizált embereket teszteltek T. gondii antitestekre, a T. gondii és a skizofrénia közötti összefüggéseket már a skizofrénia tüneteinek megjelenése előtt találták. A nemi különbségek a skizofrénia kialakulásának korában részben azzal magyarázhatók, hogy a T. gondii fertőzés előfordulási gyakoriságának második csúcsa 25–30 éves korban nőtt. Bár a skizofrénia és a T. gondii fertőzés közötti összefüggést alátámasztó mechanizmus nem tisztázott, a vizsgálatok ennek a korrelációnak a molekuláris alapját vizsgálták. A skizofréniában használt antipszichotikus szerek gátolják a T. gondii tachyzoiták replikációját sejttenyészetben. Feltételezve, hogy ok-okozati összefüggés áll fenn a T. gondii és a skizofrénia között, a vizsgálatok még nem határozták meg, hogy miért csak néhány látens toxoplazmózisban szenvedő egyénben alakul ki skizofrénia; néhány elfogadható magyarázat közé tartozik az eltérő genetikai fogékonyság, a parazita törzsek különbségei és a szerzett T. gondii fertőzés útvonalának különbségei .
Szintén összefüggést találtak a T. gondii és az OCD elleni antitest- titerek között , valamint a hangulati zavarokban, köztük a bipoláris zavarban szenvedő emberek öngyilkossága között . Úgy tűnik, hogy a T. gondii elleni pozitív antitest-titerek nem állnak összefüggésben a major depresszióval vagy a dysthymiával . Bár van összefüggés a T. gondii és számos pszichológiai rendellenesség között, a mögöttes mechanizmus nem világos. Egy 2016-os, 236, magas toxoplazmózis elleni antitesttel rendelkező személy bevonásával végzett tanulmány megállapította, hogy "kevés bizonyíték volt arra, hogy a T. gondii összefüggésben állna a pszichiátriai rendellenességek, a rossz impulzuskontroll, a személyiségzavarok vagy a neurokognitív károsodás fokozott kockázatával".
Neurológiai rendellenességek
A látens fertőzést összefüggésbe hozták a Parkinson-kórral és az Alzheimer-kórral .
A sclerosis multiplexben szenvedő egyének fertőzési aránya körülbelül 15%-kal alacsonyabb, mint a lakosság körében.
Közúti balesetek
Az emberekben előforduló látens T. gondii fertőzést az autóbalesetek magasabb kockázatával hozták összefüggésbe , ami potenciálisan a pszichomotoros teljesítmény csökkenése vagy a fokozott kockázatvállaló személyiségprofilok miatt következett be .
Klímaváltozás
Beszámoltak arról, hogy az éghajlatváltozás befolyásolja a T. gondii előfordulását, túlélését, elterjedését és terjedését . A T. gondii-t a kanadai sarkvidéken azonosították, egy olyan helyen, amely egykor túl hideg volt a túléléshez. A magasabb hőmérséklet növeli a T. gondii túlélési idejét . A több hóolvadás és csapadék növelheti a T. gondii oociszták mennyiségét , amelyek a folyók áramlásán keresztül szállítódnak. A madár-, rágcsáló- és rovarpopulációk változásai, valamint a vándorlási minták befolyásolhatják a T. gondii elterjedését rezervoárként és vektorként betöltött szerepük miatt. A városiasodás és a természetes környezet leromlása szintén befolyásolja a T. gondii terjedését és növeli a fertőzés kockázatát.
Lásd még
Hivatkozások
- Ennek a cikknek egyes részei a CDC nyilvános adatlapjából származnak : Toxoplasmosis
Bibliográfia
- Weiss, LM; Kim, K. (2011. április 28.).Toxoplasma gondii : Az Apicomplexan modellje. Perspektívák és módszerek . Akadémiai Kiadó. ISBN 978-0-08-047501-1. Letöltve : 2013. március 12 .
- Dubey, JP (2016). Toxoplasmosis of Animals and Humans (2. kiadás). Boca Raton : CRC Press . xvii+313. ISBN 978-1-4200-9237-0. OCLC 423572366 . ISBN 1-4200-9236-7 ISBN 9781420092363
- Dubey JP, Lindsay DS, Speer CA (1998. április). " A Toxoplasma gondii tachyzoiták, bradyzoiták és sporozoiták szerkezete, valamint a szöveti ciszták biológiája és fejlődése" . Klinikai mikrobiológiai áttekintések . 11 (2): 267–299. doi : 10.1128/CMR.11.2.267 . PMC 106833 . PMID 9564564 .
- Jaroslav Flegr (2011). Pozor, Toxo! . Academia, Prága, Cseh Köztársaság. ISBN 978-80-200-2022-2.
Külső linkek
- Hogyan fertőzi meg a macska által terjesztett parazita az embert (National Geographic)
- Toxoplazmózis a Merck Manual of Diagnosis and Therapy Professional Edition-nál
- Toxoplazmózis az Egészségvédelmi Ügynökségnél (HPA), Egyesült Királyság
- Képek a Toxoplazmózisról Medical Image Database
- Videointerjú Robert Sapolsky professzorral a toxoplazmózisról és annak az emberi viselkedésre gyakorolt hatásáról (24:27 perc)
- "Toxoplazmózis" . MedlinePlus . Amerikai Nemzeti Orvosi Könyvtár.