Aminoglikozid - Aminoglycoside
Az aminoglikozid egy gyógyszer és bakteriológiai kategóriában a hagyományos Gram-negatív antibakteriális gyógyszerek , amelyek gátolják a fehérjeszintézist, és tartalmazhatnak egy része a molekula amino-módosított glikozid ( cukor ). A kifejezés általánosabban utalhat bármely szerves molekulára, amely aminocukor -alszerkezeteket tartalmaz . Az aminoglikozid antibiotikumok baktericid hatást fejtenek ki a Gram-negatív aerobok és néhány anaerob bacilus ellen, ahol még nem alakult ki rezisztencia, de általában nem a Gram-pozitív és anaerob Gram-negatív baktériumok ellen.
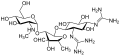
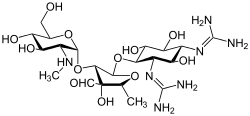
A streptomicin az első osztályú aminoglikozid antibiotikum . A Streptomyces griseus -ból származik, és a legkorábbi modern szer a tuberkulózis ellen . A sztreptomicinből hiányzik a közös 2-dezoxisztreptamin rész (kép jobbra, lent), amely az osztály többi tagjában megtalálható. Az aminoglikozidokra más példák a dezoxisztreptamin tartalmú szerek, a kanamicin , a tobramicin , a gentamicin és a neomicin (lásd alább).
Elnevezéstan
Aminoglikozidok, hogy baktériumokból származnak a Streptomyces nemzetség vannak elnevezve a utótag -mycin , míg azok, amelyek származnak Micromonospora vannak elnevezve a utótag -micin . Ez a nómenklatúra -rendszer azonban nem specifikus az aminoglikozidokra, és így az utótagok megjelenése nem utal közös hatásmechanizmusra. (Például a vankomicin , egy glikopeptid antibiotikum és az eritromicin , a Saccharopolyspora erythraea által termelt makrolid antibiotikum , valamint a szintetikus származékai, a klaritromicin és az azitromicin , mindegyike utótagokkal rendelkezik, de hatásmechanizmusuk jelentősen eltérő.)
A következő galériában a kanamicin A-tól a netilmicinig példák az aminoglikozidok 4,6-diszubsztituált dezoxisztreptamin alosztályára, a neomicinek a 4, 5 -szubsztituált alosztály példái , és a sztreptomicin egy példa a nem dezoxisztreptaminra aminoglikozid.
Hatásmechanizmusok
Az aminoglikozidok koncentrációfüggő baktericid aktivitást mutatnak a "legtöbb gram-negatív aerob és fakultatív anaerob bacilus ellen", de nem a gram-negatív anaerobok és a legtöbb gram-pozitív baktérium ellen. Csak rövid érintkezési időt igényelnek, és a leghatékonyabbak a gyorsan szaporodó fogékony baktériumpopulációk ellen. Ezeket a tevékenységeket a fehérjeszintézis -gátlók elsődleges hatásmechanizmusának tulajdonítják , bár bizonyos mechanizmusokhoz további mechanizmusok is kapcsolódnak, és/vagy az alapos mechanikus leírások még nem állnak rendelkezésre.
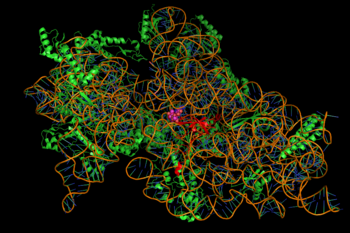
A fehérjeszintézis gátlását az aminoglikozidok energiafüggő, néha visszafordíthatatlan kötődése közvetíti a citoszolos , membránhoz kapcsolódó bakteriális riboszómához (kép a jobb oldalon). (Az aminoglikozidok először átjutnak a baktériumok sejtfalán- lipopoliszacharid a gram-negatív baktériumokban-és a sejtmembránokon, ahol aktívan szállítják őket .) Míg az érintett fehérjeszintézis egyes lépései bizonyos aminoglikozid-szerek között némileg eltérhetnek, akárcsak affinitásuk és kötődésük mértéke, az aminoglikozidok jelenléte a citoszolban általában megzavarja a peptidek megnyúlását a 30S riboszómális alegységnél, ami pontatlan mRNS -transzlációt eredményez, és ezáltal a csonka fehérjék bioszintézisét, vagy bizonyos helyeken megváltozott aminosav -összetételeket. Pontosabban, a kötés rontja a transzlációs lektorálást, ami az RNS -üzenet rossz olvasásához, idő előtti lezárásához vagy mindkettőhöz vezet, és így a lefordított fehérjetermék pontatlanságához vezet . A bakteriális sejtmembránba beépült aberráns fehérjék részhalmaza ezután megváltoztathatja permeabilitását, majd "tovább stimulálja az aminoglikozid transzportot". Ennek a molekulaosztálynak az aminocukor része (pl. A 2-dezoxisztreptamin kanamicinekben, gentamicinekben és tobramicinben, lásd fent) összefüggésben van a kis molekula és a riboszómális struktúrák társításával, amelyek a fordítás hűtlenségéhez vezetnek (uo.) . A riboszómális transzlokáció gátlását-például a peptidil-tRNS mozgását az A-tól a P-helyre-szintén javasolták. A legutóbbi egymolekulás követési kísérletek élő E. coliban folyamatos, de lassabb fehérjeszintézist mutattak különböző aminoglikozid gyógyszerekkel történő kezelés után. (A spektinomicin , egy rokon, de különálló kémiai szerkezetosztály, amelyet gyakran tárgyalnak aminoglikozidokkal, nem indukál rossz mRNS -olvasást, és általában nem baktericid.)
Végül további "sejtmembrán-hatás" is fellép aminoglikozidokkal; "A bakteriális sejtmembrán funkcionális integritása" elveszhet, később az aminoglikozid expozíció és szállítás során.
Farmakokinetika és farmakodinamika
A beadott dózis és a vér plazmaszintje közötti összefüggésben jelentős eltérések vannak. A terápiás gyógyszeres monitorozás (TDM) szükséges a megfelelő dózis eléréséhez. Ezek a szerek olyan antibiotikum utáni hatást mutatnak , amelyben a vérben nincs vagy csak nagyon kevés gyógyszer szintet lehet kimutatni, de úgy tűnik, hogy továbbra is gátolják a baktériumok szaporodását. Ennek oka a riboszómához való erős, visszafordíthatatlan kötődés, és a plazmaszint csökkenése után is intracelluláris marad, és lehetővé teszi a hosszabb adagolási intervallumot. Koncentrációjuktól függően bakteriosztatikus vagy baktericid szerek.
Javallatok
Az aminoglikozidok elsősorban aerob , Gram-negatív baktériumok, például Pseudomonas , Acinetobacter és Enterobacter fertőzések esetén hasznosak . Ezenkívül egyes mikobaktériumok , beleértve a tuberkulózist okozó baktériumokat , érzékenyek az aminoglikozidokra. A sztreptomicin volt az első hatékony gyógyszer a tuberkulózis kezelésében, bár az aminoglikozidok, például a sztreptomicin és az amikacin szerepe elhomályosult (a toxicitásuk és az alkalmazásuk kényelmetlen módja miatt), kivéve a többszörös gyógyszer-rezisztens törzseket. Az aminoglikozidok leggyakoribb alkalmazása súlyos fertőzések, például szepszis , komplikált hasüregi fertőzések, bonyolult húgyúti fertőzések és kórházi légúti fertőzések empirikus terápiája . Általában, miután az ok -okozati organizmus tenyészetét kinőttük és érzékenységüket teszteltük, az aminoglikozidok használatát leállítjuk a kevésbé mérgező antibiotikumok javára.
Mint említettük, az aminoglikozidok többnyire hatástalanok az anaerob baktériumokkal, gombákkal és vírusokkal szemben. A Gram-pozitív baktériumok által okozott fertőzések szintén kezelhetők aminoglikozidokkal, de más típusú antibiotikumok hatásosabbak és kevésbé károsak a gazdaszervezetre. A múltban az aminoglikozidokat béta-laktám antibiotikumokkal együtt alkalmazták streptococcus fertőzéseknél szinergikus hatásuk miatt, különösen endokarditiszben . Az egyik leggyakoribb kombináció az ampicillin ( béta-laktám vagy penicillinnel rokon antibiotikum) és a gentamicin. A kórházi személyzet gyakran ezt a kombinációt „erősítőnek” vagy újabban „pen and gent” -nek nevezi a penicillin és gentamicin esetében.
Hülyeség elfojtása
Az mRNS korrektúrába való beavatkozást a korai stop kodonokból eredő genetikai betegségek kezelésére használták fel (ami a fehérjeszintézis és a csonka fehérjék korai befejezéséhez vezet). Az aminoglikozidok hatására a sejt legyőzi a stop kodonokat, beiktat egy véletlenszerű aminosavat, és egy teljes hosszúságú fehérjét expresszál. Az aminoglikozid gentamicint a cisztás fibrózis (CF) sejtek kezelésére használták a laboratóriumban, hogy teljes hosszúságú fehérjéket termeljenek. A CF -t a cisztás fibrózis transzmembrán vezetőképesség -szabályozó ( CFTR ) fehérjét kódoló gén mutációja okozza . A CF esetek körülbelül 10% -ában a mutáció ebben a génben a transzláció során a korai befejeződést okozza , ami egy csonka és nem működő CFTR fehérje kialakulásához vezet. Úgy gondolják, hogy a gentamicin eltorzítja a riboszóma-RNS komplex szerkezetét, ami a terminációs kodon hibás leolvasásához vezet , ami miatt a riboszóma "átugorja" a stop szekvenciát, és folytatja a CFTR fehérje normális megnyúlását és termelését .
Az adminisztráció módjai
Mivel nem szívódnak fel a bélből, intravénásan és intramuszkulárisan adják be őket . Néhányat helyi sebészeti készítményekben használnak. Orális adagolás alkalmazható a bél fertőtlenítésére (pl. Hepatikus encephalopathia esetén). A tobramicin porlasztott formában adható be.
Klinikai felhasználás
A Gram-negatív baktériumtörzsek és az antimikrobiális rezisztencia fejlett mintázata miatt a közelmúltban megjelenő fertőzések arra késztették az orvosokat, hogy újraértékeljék ezen antibakteriális szerek alkalmazását. Az aminoglikozidok alkalmazása iránti újjáéledő érdeklődés napvilágra hozta a vitát az e vegyületekkel kapcsolatos két fő kérdésről, nevezetesen az antimikrobiális érzékenység és a toxicitás spektrumáról. A jelenlegi bizonyítékok azt mutatják, hogy az aminoglikozidok megtartják aktivitásukat a Gram-negatív klinikai bakteriális izolátumok többsége ellen a világ számos részén. Mégis, az aminoglikozid -kezelés során a nefrotoxicitás és ototoxicitás viszonylag gyakori előfordulása miatt az orvosok nem szívesen használják ezeket a vegyületeket a mindennapi gyakorlatban. A közelmúltban elért eredmények az aminoglikozidok különböző adagolási rendjeinek toxicitásra gyakorolt hatásának megértésében részleges megoldást jelentettek erre a problémára, bár további kutatásokra van szükség a probléma teljes leküzdése érdekében.
Az aminoglikozidok a D terhességi kategóriába tartoznak , vagyis a vizsgálati vagy marketing tapasztalatokból vagy embereken végzett vizsgálatokból származó mellékhatások adatai alapján pozitív bizonyítékok vannak az emberi magzat kockázatára, de a potenciális előnyök indokolhatják a gyógyszer terhes nőknél történő alkalmazását a lehetséges kockázatok ellenére.
Káros hatások
Az aminoglikozid belső fül toxicitást okozhat, ami szenzoros és halláskárosodáshoz vezethet . A belső fül toxicitásának előfordulási gyakorisága 7-90%között változik, az alkalmazott antibiotikumok típusától, a beteg érzékenységétől és az antibiotikum beadásának időtartamától függően.
Az aminoglikozidok használatának másik súlyos és akadályozó mellékhatása a vestibularis ototoxicitás. Ez oszcillopsziához (tekintet instabilitáshoz) és egyensúlyzavarokhoz vezet, amelyek hatással vannak az egyén antigravitációs funkciójának minden aspektusára. Ez a veszteség tartós, és bármilyen dózis esetén előfordulhat.
Az aminoglikozid egyik leginkább aggasztó mellékhatása a vesetoxicitás .
Ellenjavallatok bizonyos betegségek esetén
Az aminoglikozidok súlyosbíthatják a gyengeséget myasthenia gravisban szenvedő betegeknél , ezért ezeknél a betegeknél kerülni kell a használatát.
Az aminoglikozidok ellenjavalltak mitokondriális betegségekben szenvedő betegeknél, mivel károsodott mtDNS -transzlációt eredményezhetnek, ami visszafordíthatatlan halláscsökkenéshez, fülzúgáshoz, szívtoxicitáshoz és vesetoxicitáshoz vezethet. Mindazonáltal halláskárosodást és fülzúgást is megfigyeltek néhány, mitokondriális betegségben nem szenvedő betegnél.
Hivatkozások
Külső linkek
- MedlinePlus gyógyszerinformáció - Aminoglikozidok (szisztémás)
- Science Daily Bacterial "Battle for Survival" - Rodosztreptomicin