Toll -szerű receptor - Toll-like receptor
| Toll-szerű receptor | |
|---|---|
 Az útdíjas szerű receptorok ívelt leucinban gazdag ismétlődő régiója, amelyet itt a TLR3 képvisel
| |
| Azonosítók | |
| Szimbólum | Toll-szerű receptor |
| Membranóm | 7 |
| PIRSF037595 | |
A toll-szerű receptorok ( TLR-ek ) olyan fehérjék osztálya, amelyek kulcsszerepet játszanak a veleszületett immunrendszerben . Ezek egylépéses, membránon átívelő receptorok, amelyeket általában őrszem sejteken , például makrofágokon és dendritikus sejteken fejeznek ki, és amelyek felismerik a mikrobákból származó szerkezetileg konzervált molekulákat . Miután ezek a mikrobák áttörték a fizikai akadályokat, például a bőrt vagy a bélrendszer nyálkahártyáját , felismerik őket a TLR -ek, amelyek aktiválják az immunsejtek válaszát. A TLR-ek közé TLR1 , TLR2 , TLR3 , TLR4 , TLR5 , TLR6 , TLR7 , TLR8 , TLR9 , TLR10 , TLR11 , TLR12 és TLR13, bár az utolsó három nem az emberben, és nincs olyan funkcionális génnel TLR10 egerekben. A TLR1, TLR2, TLR4, TLR5, TLR6 és TLR10 a sejtmembránon helyezkednek el , míg a TLR3, TLR7, TLR8 és TLR9 sejten belüli vezikulumokban találhatók (mivel nukleinsav -érzékelők ).
A TLR-ek kapott nevüket való hasonlóságuk által kódolt protein az útdíj-gén azonosított Drosophila 1985 Christiane Nüsslein-Volhard és Eric Wieschaus .
Funkció
Az a képesség, az immunrendszer felismerni molekulák , amelyek széles körben osztják kórokozók van, részben, mivel a jelenléte immun receptorok úgynevezett Toll-like receptorok (TLR), amelyek expresszálódnak a membránok a leukociták beleértve dendritikus sejteket , makrofágokat , természetes gyilkos sejtek , az adaptív immunitás T-sejtjei és B-sejtjei , valamint nem immunsejtek ( hám- és endoteliális sejtek , valamint fibroblasztok ).
A ligandumok kötődése - akár adalékanyagként, akár vakcinázásban, vagy invazív egységek formájában a természetes fertőzés idején - a TLR -hez jelzi azokat a kulcsfontosságú molekuláris eseményeket, amelyek végül veleszületett immunválaszokhoz és antigénspecifikus szerzett betegségek kialakulásához vezetnek immunitás.
Az aktiválás után a TLR-ek adapterfehérjéket toboroznak (olyan fehérjék, amelyek más fehérje-fehérje kölcsönhatásokat közvetítenek) az immunsejt citoszoljában , hogy továbbítsák az antigén által indukált jelátviteli utat . Ezek a felvett fehérjék ezután felelősek a későbbi aktiválását más downstream fehérjék, beleértve a protein kinázok (IKKI, IRAK1 , IRAK4 , és TBK1 ), hogy tovább erősítik a jelet, és végső soron a serkentését vagy elnyomása gének , hogy hangszerel gyulladásos válaszokat és más transzkripciós események. Ezen események egy része citokin termeléshez, proliferációhoz és túléléshez vezet, míg mások nagyobb adaptív immunitáshoz. Ha a ligandum bakteriális faktor, akkor a kórokozót fagocitálhatjuk és megemészthetjük, és antigénjeit bemutathatjuk a CD4+ T -sejteknek . Vírusfaktor esetén a fertőzött sejt leállíthatja fehérjeszintézisét, és programozott sejthalált ( apoptózist ) szenvedhet . A vírust észlelő immunsejtek vírusellenes tényezőket, például interferonokat is felszabadíthatnak .
A toll-szerű receptorok szintén fontos kapcsolatnak bizonyultak a veleszületett és az adaptív immunitás között a dendritikus sejtekben való jelenlétük révén . A Flagellin , a TLR5 ligandum, citokin szekréciót indukál, amikor kölcsönhatásba lép a TLR5 -tel humán T -sejteken.
Szupercsalád
A TLR-k egyfajta mintázatfelismerő receptor (PRR), és felismerik azokat a molekulákat, amelyeket a kórokozók széles körben megosztanak, de megkülönböztethetők a gazdamolekuláktól, amelyeket együttesen kórokozókkal kapcsolatos molekuláris mintázatoknak (PAMP) neveznek . A TLR-k az Interleukin-1 receptorokkal együtt egy receptor szupercsaládot alkotnak , amelyet "interleukin-1 receptor / toll-szerű receptor szupercsaládnak" neveznek; ennek a családnak minden tagja közös az úgynevezett TIR (toll-IL-1 receptor) doménnel.
A TIR tartományok három alcsoportja létezik. Az 1. alcsoport TIR doménnel rendelkező fehérjék az interleukinek receptorai, amelyeket makrofágok , monociták és dendritikus sejtek termelnek, és mindegyikük extracelluláris immunglobulin (Ig) doménnel rendelkezik. A 2. alcsoport TIR doménnel rendelkező fehérjék klasszikus TLR -ek, és közvetlenül vagy közvetve kötődnek a mikrobiális eredetű molekulákhoz. A TIR doméneket tartalmazó fehérjék harmadik alcsoportja kizárólag citoszolikus adapterfehérjékből áll , amelyek az 1. és 2. alcsoport fehérjéiből közvetítik a jelátvitelt.
Kiterjesztett család
A TLR -ek gerincesekben és gerinctelenekben is jelen vannak . A TLR -ek molekuláris építőkövei a baktériumokban és a növényekben jelen vannak, és a növénymintázat -felismerő receptorokról köztudott, hogy szükségük van a gazdaszervezet fertőzés elleni védekezésére. A TLR -ek tehát az immunrendszer egyik legősibb, konzerváltabb összetevőjének tűnnek .
Az utóbbi években TLR -ket azonosítottak az emlősök idegrendszerében is. A TLR család tagjait glia, neuronok és idegi progenitor sejtek észlelték, amelyekben szabályozzák a sejt sorsát.
Becslések szerint a legtöbb emlősfaj tíz-tizenöt típusú vám-szerű receptorral rendelkezik. Tizenhárom TLR -t (egyszerűen TLR1 -TLR13 névvel) azonosítottak emberekben és egerekben együtt, és ezek közül sok másnak megfelelő formáját más emlősfajokban is megtalálták. Mindazonáltal bizonyos TLR emberekben található megfelelői nem minden emlősben vannak jelen. Például az emberekben a TLR10 -hez analóg fehérjét kódoló gén jelen van egerekben , de úgy tűnik, hogy a múltban valamikor megsérült egy retrovírus által . Másrészt az egerek 11, 12 és 13 TLR -t fejeznek ki, amelyek közül egyik sem képviselteti magát emberben. Más emlősök olyan TLR -eket fejezhetnek ki, amelyek nem fordulnak elő emberben. Más nem emlős fajok TLR- ei különbözhetnek az emlősöktől, amint azt a Takifugu pufferhalban található sejtfal elleni TLR14 is mutatja . Ez megnehezítheti a kísérleti állatok emberi veleszületett immunitás modelljeként való felhasználásának folyamatát.
A gerinces TLR -ket a hasonlóság a TLR 1/2/6/10/14/15, TLR 3, TLR 4, TLR 5, TLR 7/8/9 és TLR 11/12/13/16/21 családokra osztja /22/23.
TLR -ek a Drosophila immunitásban
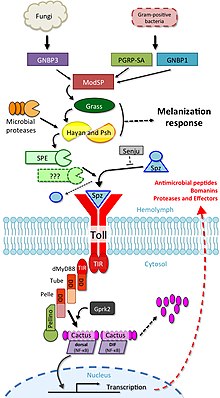
A Toll jelátvitelnek az immunitásba való bevonását először a gyümölcslégy, a Drosophila melanogaster bizonyította . A gyümölcslegyeknek csak veleszületett immunválaszaik vannak, amelyek lehetővé teszik a vizsgálatokat, hogy elkerüljék az adaptív immunmechanizmusok interferenciáját a jelátvitelben. A gombás vagy bakteriális fertőzésre adott légyválasz két különböző jelző kaszkádon keresztül történik, amelyek közül az egyik a Toll útvonal, a másik az immunhiányos (IMD) út . A Toll útvonal hasonló az emlős TLR jelzéshez, de az emlős TLR-ekkel ellentétben a Toll nem közvetlenül aktiválódik a kórokozókkal kapcsolatos molekuláris mintázatok ( PAMP ) segítségével. A receptor ektodoménje felismeri a Spätzle citokin hasított formáját, amely a hemolimfában inaktív dimer prekurzorként szekretálódik . A Toll receptor osztja a citoplazmatikus TIR domént az emlős TLR -ekkel, de az ektodomén és az intracitoplazmatikus farok eltérő. Ez a különbség tükrözheti ezeknek a receptoroknak a funkcióját, mint citokin receptorokat, nem pedig PRR -ket .
A Toll útvonalat különböző ingerek, például Gram -pozitív baktériumok , gombák és virulencia faktorok aktiválják . Először is, a Spätzle feldolgozó enzim (SPE) aktiválódik a fertőzés hatására, és lehasítja a Spätzle -t ( spz ). A hasított Spätzle ezután kötődik a Toll receptorhoz, és összekapcsolja ektodoménjeit. Ez konformációs változásokat idéz elő a receptorban, ami a Toll -on keresztül történő jelzést eredményez. Innentől kezdve a jelző kaszkád nagyon hasonlít a TLR -eken keresztül történő emlősjelzéshez. A Toll-indukált jelátviteli komplexum (TICS) a MyD88-ból , a Tube-ból és a Pelle-ből (az emlősök IRAK ortológjából) áll. A TICS jelét ezután Cactus-ba (emlősök IκB homológja ) transzdukálják , a foszforilezett kaktuszt polikvikvilitálják és lebontják, lehetővé téve a DIF (dorsalis-kapcsolódó immunitási faktor; emlősök NF-κB homológja) nukleáris transzlokációját és az antimikrobiális gének transzkripciójának indukálását peptidek (AMP -k ), például Drosomicin .
A droszofíliának összesen 9 fizetős családja és 6 spz család génje van, amelyek különböző mértékben kölcsönhatásba lépnek egymással.
TLR2
A TLR2 -t CD282 -nek (282 -es differenciálódási klaszter) is jelölték.
TLR3
A TLR3 nem használja a MyD88 függő útvonalat. Ligandusa a retrovirális kettős szálú RNS ( dsRNS ), amely aktiválja a TRIF- függő jelátviteli utat. Ennek az útvonalnak a retrovírus -újraprogramozásban betöltött szerepének feltárásához TLR3 vagy TRIF leütési technikákat készítettünk, és az eredmények azt mutatták, hogy csak a TLR3 útvonal szükséges a célgén expresszió teljes indukciójához a retrovírus expressziós vektor által. Ez a retrovirális expressziós négy transzkripciós faktorok ( Oct4 , Sox2 , Klf4 és c-Myc ; OSKM) indukálja pluripotencia szomatikus sejtekben. Ezt alátámasztja egy tanulmány, amely azt mutatja, hogy a retrovírus -vektorokat alkalmazó humán iPSC -generáció hatékonyságát és mennyiségét csökkenti az út leütése peptid inhibitorokkal vagy a TLR3 vagy annak TRIF adapterfehérje shRNS -leütése. Összességében elmondható, hogy a TLR3 stimulálása nagy változásokat okoz a kromatin átalakításában és a nukleáris újraprogramozásban, és ezekhez a változásokhoz, a pluripotencia gének indukciójához és az emberi indukált pluripotens őssejtek (iPSC) telepek létrehozásához gyulladásos utak aktiválása szükséges.
TLR11
Amint fentebb említettük, az emberi sejtek nem expresszálják a TLR11 -et , de az egerek sejtjei igen. Az egér-specifikus TLR11 felismeri az uropatogen E.coli-t és a Toxoplasma gondii apikomplexán parazitát . A Toxoplasma liganduma a fehérje profilin, és a ligandum az E. coli van flagellin . A Salmonella enteropatogén flagellint a TLR11 is felismeri.
Mivel a TLR11 egér képes hatékonyan felismerni a szalmonellát , a normál egerek nem fertőződnek meg az orális Salmonella Typhi-vel , ami emberekben étel- és vízben terjedő gasztroenteritist és tífuszt okoz . A TLR11 -hiányos kiütött egerek viszont hatékonyan fertőzöttek. Ennek eredményeként ez a kiütött egér az emberi tífuszos láz betegségmodelljeként működhet .
Az ismert emlős TLR -k összefoglalása
A toll-szerű receptorok különböző ligandumokkal kötődnek és aktiválódnak, amelyek viszont különböző típusú organizmusokon vagy szerkezeteken helyezkednek el. Különböző adapterekkel is rendelkeznek, amelyek reagálnak az aktiválásra, és néha a sejt felszínén, néha pedig a belső sejtrészeken találhatók . Ezenkívül különböző típusú leukociták vagy más sejttípusok fejezik ki őket :
| Receptor | Ligand (ok) | Ligand helyszín | Adapter (ek) | Elhelyezkedés | Sejt típusok |
|---|---|---|---|---|---|
| TLR 1 | több triacil -lipopeptid | Bakteriális lipoprotein | MyD88 /MAL | sejt felszíne |
|
| TLR 2 | több glikolipid | Bakteriális peptidoglikánok | MyD88/MAL | sejt felszíne |
|
| több lipopeptid és proteolipid | Bakteriális peptidoglikánok | ||||
| lipoteichoinsav | Gram-pozitív baktériumok | ||||
| HSP70 | Gazdasejtek | ||||
| zimozán ( béta-glükán ) | Gombák | ||||
| Számos más | |||||
| TLR 3 | kettős szálú RNS , poli I: C | vírusok | TRIF | cellarekesz |
|
| TLR 4 | lipopoliszacharid | Gram-negatív baktériumok | MyD88/MAL/ TRIF /TRAM | sejt felszíne |
|
| számos hősokk fehérje | Baktériumok és gazdasejtek | ||||
| fibrinogén | gazdasejtek | ||||
| heparán -szulfát -töredékek | gazdasejtek | ||||
| hialuronsav töredékek | gazdasejtek | ||||
| nikkel | |||||
| Különféle opioid gyógyszerek | |||||
| TLR 5 | Bakteriális flagellin | Baktériumok | MyD88 | sejt felszíne |
|
| Profilin | Toxoplasma gondii | ||||
| TLR 6 | több diacil -lipopeptid | Mycoplasma | MyD88/MAL | sejt felszíne |
|
| TLR 7 | imidazoquinolin | kis szintetikus vegyületek | MyD88 | cellarekesz |
|
| loxoribin ( guanozin analóg) | |||||
| bropirimine | |||||
| resiquimod | |||||
| egyszálú RNS | RNS vírusok | ||||
| TLR 8 | kis szintetikus vegyületek; egyszálú vírusos RNS, fagocitizált bakteriális RNS (24) | MyD88 | cellarekesz |
|
|
| TLR 9 | metilálatlan CpG oligonukleotidot DNS | Baktériumok, DNS -vírusok | MyD88 | cellarekesz |
|
| TLR 10 | triacilezett lipopeptidek | ismeretlen | sejt felszíne |
|
|
| TLR 11 | Profilin | Toxoplasma gondii | MyD88 | cellarekesz |
|
| Flagellin | Baktériumok ( E. coli , Salmonella ) | ||||
| TLR 12 | Profilin | Toxoplasma gondii | MyD88 | cellarekesz |
|
| TLR 13 | bakteriális riboszómális RNS -szekvencia "CGGAAAGACC" (de nem a metilezett változat) | Vírus, baktérium | MyD88, TAK-1 | cellarekesz |
|
Ligandok
A vám-szerű receptorok (és más veleszületett immunreceptorok) sajátosságai miatt nem könnyen változtathatók meg az evolúció során, ezek a receptorok felismerik azokat a molekulákat, amelyek állandóan fenyegetésekkel (pl. Kórokozó vagy sejt stressz) járnak együtt, és nagyon specifikusak ezek a fenyegetések (azaz nem téveszthetők össze olyan önmolekulákkal, amelyek általában fiziológiai körülmények között fejeződnek ki). Azoknak a kórokozókkal kapcsolatos molekuláknak, amelyek megfelelnek ennek a követelménynek, úgy gondolják, hogy kritikusak a kórokozó működésében, és nehéz megváltoztatni őket a mutáció révén; állítólag evolúciósan konzerváltak. A kórokozók némileg konzervált jellemzői közé tartoznak a bakteriális sejtfelszíni lipopoliszacharidok (LPS), a lipoproteinek , a lipopeptidek és a lipoarabinomannán ; fehérjék, például a bakteriális flagellából származó flagellin ; a vírusok kétszálú RNS- e; vagy a bakteriális és vírusos DNS metilálatlan CpG szigetei ; valamint az eukarióta DNS -promóterekben található CpG -szigetek; valamint bizonyos más RNS és DNS molekulák. A legtöbb TLR esetében a ligandumfelismerő specificitást mára géncélzással állapították meg (más néven "génkiütés"): ez a technika lehetővé teszi az egyes gének szelektív törlését egerekben. Tekintse meg az alábbi táblázatot az ismert TLR ligandok összegzéséhez.
Endogén ligandumok
A fizetős Like-Receptor aktiválása által kiváltott sztereotip gyulladásos válasz arra enged következtetni, hogy az autópálya-szerű receptorok endogén aktivátorai részt vehetnek az autoimmun betegségekben. A TLR -ek feltételezik, hogy kötődnek a gazdamolekulákhoz, beleértve a fibrinogént (részt vesznek a véralvadásban ), a hősokk -fehérjéket (HSP -ket), a HMGB1 -et , az extracelluláris mátrix komponenseit és a saját DNS -t (általában nukleázok bontják le, de gyulladásos és autoimmun körülmények között kialakulhat) endogén fehérjéket tartalmazó komplex, rezisztenssé válnak ezekkel a nukleázokkal szemben, és hozzáférnek az endoszomális TLR -ekhez, mint TLR7 vagy TLR9). Ezeket az endogén ligandumokat általában nem fiziológiás sejtpusztulás eredményeként állítják elő.
Jelzés
TLR úgy gondolják, hogy funkcionálnak dimerek . Bár úgy tűnik, hogy a legtöbb TLR homodimerként funkcionál , a TLR2 heterodimereket képez a TLR1 -gyel vagy a TLR6 -tal, és mindegyik dimer eltérő ligandum -specifitással rendelkezik. A TLR-ek függhetnek más társreceptoroktól is a teljes ligandum-érzékenység szempontjából, például abban az esetben, ha a TLR4 felismeri az LPS-t , amelyhez MD-2 szükséges. Ismert, hogy a CD14 és az LPS-Binding Protein ( LBP ) elősegíti az LPS megjelenését az MD-2-nek.
A TLR3 -at, TLR7 -et, TLR8 -at és TLR9 -et tartalmazó endoszomális TLR -ek halmaza felismeri a vírusokból származó nukleinsavakat , valamint az endogén nukleinsavakat a patogén események összefüggésében. Ezeknek a receptoroknak az aktiválása gyulladásos citokinek , valamint I. típusú interferonok ( I. típusú interferon ) termelését eredményezi a vírusfertőzés elleni küzdelemben.
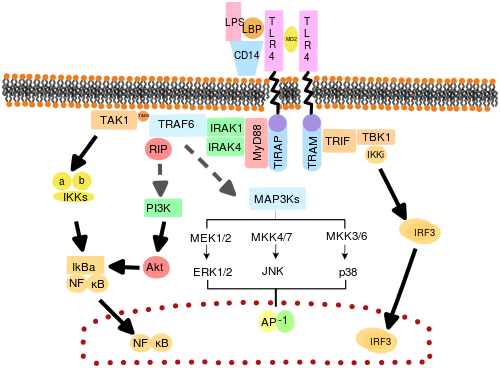
A TLR jelátvitelt közvetítő adapterfehérjéket és kinázokat is megcélozták. Ezenkívül az ENU -val random csíravonal -mutagenezist alkalmaztak a TLR jelátviteli utak megfejtésére. Aktiváláskor a TLR -ek adapter molekulákat toboroznak a sejtek citoplazmájában a jel továbbítására. Ismert, hogy négy adaptermolekula vesz részt a jelzésben. Ezek a fehérjék MyD88 , TIRAP (más néven Mal), TRIF és TRAM (TRIF-hez kapcsolódó adaptermolekula) néven ismertek .
A TLR jelzés két különböző jelzési útra oszlik, a MyD88-függő és a TRIF-függő útra.
MyD88-függő útvonal
A MyD88-függő válasz a TLR receptor dimerizációjánál jelentkezik, és a TLR3 kivételével minden TLR használja. Elsődleges hatása az NFkB és a mitogén-aktivált protein-kináz aktiválása . A receptorban bekövetkező ligandumkötés és konformációs változás a MyD88 adapterfehérjét, a TIR család tagjait toborozza . A MyD88 ezután IRAK4 -et , IRAK1 -et és IRAK2 -t toboroz . Az IRAK kinázok ezután foszforilálják és aktiválják a TRAF6 fehérjét , amely viszont polubikvinálja a TAK1 fehérjét, valamint önmagát, hogy megkönnyítse az IKK-β- hoz való kötődést . Kötődéskor a TAK1 foszforilálja az IKK-β-t, amely ezután foszforilálja az IκB-t, ami annak lebomlását okozza, és lehetővé teszi, hogy az NFκB diffundáljon a sejtmagba, és aktiválja a transzkripciót, és ennek következtében gyulladásos citokinek indukcióját.
TRIF-függő út
Mind a TLR3, mind a TLR4 a TRIF-függő útvonalat használja, amelyet a dsRNS és az LPS vált ki. A TLR3 esetében a dsRNS a receptor aktiválásához vezet, és felveszi a TRIF adaptert . A TRIF aktiválja a TBK1 és RIPK1 kinázokat , amelyek elágazást hoznak létre a jelzőútban . A TRIF/TBK1 jelátviteli komplex foszforilálja az IRF3 -at, lehetővé téve annak transzlokációját a magba és az I. típusú interferon termelését . Eközben a RIPK1 aktiválása a TAK1 és az NFκB transzkripció poliubikvitinációját és aktiválását okozza, ugyanúgy, mint a MyD88-függő útvonalat.
A TLR jelátvitel végső soron a gyulladásos választ irányító gének indukciójához vagy elnyomásához vezet. Összességében több ezer gént aktiválnak a TLR -jelzéssel, és együttesen a TLR -ek az egyik leginkább pleiotróp, mégis szigorúan szabályozott átjárót jelentik a génmodulációhoz.
A TLR4 az egyetlen TLR, amely mind a négy adaptert használja. A TLR4, MD2 és LPS komplexum TIR domént tartalmazó TIRAP és MyD88 adaptereket toboroz, és így kezdeményezi az NFκB (korai fázis) és a MAPK aktiválását. A TLR4-MD2-LPS komplex ezután endocitózison megy keresztül, és endoszómában TRAM és TRIF adapterekkel jelző komplexet képez. Ez a TRIF-függő útvonal ismét az IRF3 aktiválásához és az I. típusú interferonok termeléséhez vezet, de aktiválja a késői fázisú NFκB aktivációt is. A gyulladásos citokinek termeléséhez mind az NFκB késői, mind korai fázisának aktiválása szükséges.
Orvosi relevancia
Az imikvimod (a bőrgyógyászatban kardinálisan használt ) TLR7 agonista, utóda rezikvimodja pedig TLR7 és TLR8 agonista. A közelmúltban a resiquimodot a rákos immunterápia hatóanyagaként fedezték fel, amely a daganatokkal kapcsolatos makrofágok stimulálása révén hat.
Számos TLR ligandum klinikai fejlesztés alatt áll, vagy állatmodelleken tesztelik őket vakcinaadjuvánsként , az első klinikai alkalmazást emberben egy rekombináns herpesz -zoster vakcina tartalmazza, amely 2017 -ben tartalmaz monofoszforil -lipid A komponenst.
TLR7 hírvivő RNS expressziós szinteket jelentettek tejelő állatokban a ragadós száj- és körömfájás természetes kitörése esetén.
A TLR4 fontosnak bizonyult az opioidok hosszú távú mellékhatásai szempontjából . Aktiválása gyulladásos modulátorok, köztük TNF-α és IL-1β felszabadulásához vezet , és ezeknek a modulátoroknak az állandó alacsony szintű felszabadulása vélhetően csökkenti az opioid gyógyszeres kezelés hatékonyságát idővel, és részt vesz az opioid toleranciában, a hiperalgéziában és az allodíniában . A morfin által kiváltott TLR4 aktiváció csökkenti az opioidok által okozott fájdalomcsillapítást , és fokozza az opioid tolerancia és függőség kialakulását , a kábítószerrel való visszaélést és egyéb negatív mellékhatásokat, például a légzési depressziót és a hiperalgéziát. A TNF-α vagy IL-1β hatását gátló gyógyszerekről kimutatták, hogy fokozzák az opioidok fájdalomcsillapító hatását, csökkentik a tolerancia és más mellékhatások kialakulását, és ezt a TLR4-et blokkoló gyógyszerekkel is bebizonyították.
Az opioid gyógyszerek "természetellenes" enantiomerjei, mint például a (+)-morfin és (+)-naloxon nem rendelkeznek affinitással az opioid receptorokhoz, továbbra is ugyanazt az aktivitást mutatják a TLR4-en, mint a "normál" enantiomerek. Tehát az opioidok "természetellenes" entianomerjei, mint például a (+)-naloxon, használhatók az opioid fájdalomcsillapító gyógyszerek TLR4 aktivitásának blokkolására anélkül, hogy affinitást mutatnának a μ-opioid receptorhoz
Felfedezés
Amikor először felismerték a mikrobákat a fertőző betegségek okozójaként, azonnal nyilvánvaló volt, hogy a többsejtű organizmusoknak képesnek kell lenniük arra, hogy felismerjék őket, amikor megfertőződtek, és így képesnek kell lenniük a mikrobákra jellemző molekulák felismerésére. A múlt évszázad nagy részét átfogó nagyszámú irodalom tanúsítja a kulcsmolekulák és receptoraik keresését. Több mint 100 évvel ezelőtt, Richard Pfeiffer , a hallgató Robert Koch , megalkotta a „ endotoxin ” leírni által termelt anyag Gram-negatív baktériumok , amelyek váltanak láz és sokk a kísérleti állatokban . Az ezt követő évtizedekben az endotoxint kémiailag jellemezték és lipopoliszacharidként (LPS) azonosították, amelyet a legtöbb Gram-negatív baktérium termel. Ez a lipopoliszacharid a gram-negatív membrán szerves része, és a baktérium megsemmisülése után szabadul fel. Más molekulákról (bakteriális lipopeptidek , flagellin és metilezetlen DNS ) sorra kimutatták, hogy provokálják a gazdaszervezeti válaszokat, amelyek általában védőek. Ezek a válaszok azonban károsak lehetnek, ha túlságosan elhúzódnak vagy intenzívek. Logikusan következett, hogy az ilyen molekuláknak rendelkezniük kell receptorokkal, amelyek képesek figyelmeztetni a gazdát a fertőzés jelenlétére, de ezek sok éven át megfoghatatlanok maradtak. Az útdíjszerű receptorokat mostantól a kulcsmolekulák közé sorolják, amelyek figyelmeztetik az immunrendszert a mikrobiális fertőzések jelenlétére.
A prototipikus családtag, a útdíj receptor ( P08953 ; Tl) a gyümölcslégy Drosophila melanogaster , fedezte fel 1985-ben 1995-Nobel-díjasok Christiane Nüsslein-Volhard és Eric Wieschaus és munkatársai. Az embriógenezisben kifejlődő funkciójáról ismert volt a dorsalis - ventrális tengely létrehozásával. Nevét Christiane Nüsslein-Volhard 1985-ös felkiáltásáról kapta: " Das ist ja toll ! " ("Ez elképesztő!"), Utalva a gyümölcslégy lárvájának fejletlen hasi részére. Azt klónozták a laboratóriumból Kathryn Anderson 1988-ban 1996- útdíj találtak Jules A. Hoffmann és kollégái, hogy alapvető szerepet játszik a légy immunitás gombás fertőzés , ami azt érjük el, aktiválja a szintézis antimikrobiális peptidek.
Az első jelentett humán autópályaszerű receptort Nomura és munkatársai írták le 1994-ben, Taguchi és munkatársai 1996-ban kromoszómához rendelték. Mivel a Drosophila-i útdíj immunfunkciója akkor még nem volt ismert, feltételezték, hogy a TIL (ma TLR1) részt vehet az emlősök fejlődésében. Azonban 1991-ben (a TIL felfedezése előtt) megfigyelték, hogy az emlősök immunfunkciójában egyértelműen szerepet játszó molekula, az interleukin-1 (IL-1) receptor szintén homológiát mutat a drosophila-járulékkal; mindkét molekula citoplazmatikus része hasonló volt.
1997-ben Charles Janeway és Ruslan Medzhitov kimutatták, hogy a TLR4 néven ismert, vámszerű szerű receptor ellenanyagok felhasználásával mesterségesen ligálva előidézheti az adaptív immunválasz elindításához szükséges bizonyos gének aktiválását . A TLR 4 funkciót LPS érzékelő receptorként Bruce A. Beutler és munkatársai fedezték fel . Ezek a dolgozók helyzeti klónozással bizonyították, hogy az egereknek, amelyek nem tudnak reagálni az LPS -re, mutációik vannak, amelyek megszüntették a TLR4 funkcióját. Ez azonosította a TLR4 -et az LPS receptor egyik kulcskomponenseként.
Viszont a többi TLR gént egerekben abláltuk géncélzással, nagyrészt Shizuo Akira és munkatársai laboratóriumában . Most úgy gondolják, hogy minden TLR detektálja a molekulák különálló gyűjteményét - némelyik mikrobiális eredetű, és néhány sejtkárosodási termék -, és jelzi a fertőzések jelenlétét.
Plant homológok útdíj fedezték fel Pamela Ronald 1995 (rizs Xa21) és Thomas Boller 2000 ( Arabidopsis FLS2).
2011 -ben Beutler és Hoffmann munkájáért orvosi vagy fiziológiai Nobel -díjat kapott. Hoffmann és Akira 2011 -ben megkapta a Canada Gairdner International Award díjat.
Jegyzetek és hivatkozások
Lásd még
Külső linkek
- Toll-Like+Receptors az Egyesült Államok Országos Orvostudományi Könyvtárának orvosi tantárgyai (MeSH)
- Toll+fehérje,+Drosophila az Egyesült Államok Országos Orvostudományi Könyvtárának orvosi tantárgyai (MeSH)
- TollML: Toll-szerű receptorok és ligandumok adatbázis a Müncheni Egyetemen
- A veleszületett immunreceptorok fizetős receptoracsaládja (pdf)
- Toll-Like receptor Pathway
- [1]