Vezikula (biológia és kémia) - Vesicle (biology and chemistry)
A sejtbiológiában a vezikulum a sejten belüli vagy azon kívüli szerkezet , amely folyadékból vagy citoplazmából áll, amelyet egy lipid kettősréteg zár le . A hólyagok természetesen képződnek a szekréció ( exocitózis ), a felvétel ( endocitózis ) és az anyagok plazmamembránon belüli szállítása során. Alternatívaként mesterségesen is előállíthatók, ebben az esetben liposzómáknak nevezik őket (nem tévesztendő össze a lizoszómákkal ). Ha csak egy foszfolipid kettősréteg van , akkor ezeket unilamelláris liposzóma vezikulumoknak nevezzük ; különben multilamellárisnak nevezik őket . A vezikulát körülvevő membrán is lamelláris fázis , hasonlóan a plazmamembránéhoz , és az intracelluláris vezikulák összeolvadhatnak a plazmamembránnal, hogy tartalmukat a sejten kívül szabadítsák fel. A hólyagok összeolvadhatnak a sejt más organelláival is . A sejtből felszabaduló vezikulát extracelluláris vezikulumnak nevezik .
A hólyagok sokféle funkciót látnak el. Mivel el van választva a citoszoltól , a vezikulum belseje eltérhet a citoszol környezetétől. Emiatt a vezikulumok alapvető eszközei, amelyeket a sejt a sejtes anyagok szervezésére használ. A hólyagok részt vesznek az anyagcserében , a szállításban, a felhajtóerő szabályozásában és az élelmiszerek és enzimek ideiglenes tárolásában. Vegyi reakciókamrákként is működhetnek.
Zárt szerkezet, amelyet amfifil molekulák alkotnak, és oldószert (általában vizet) tartalmaz.
A 2013-as Nobel-díjat fiziológiai vagy orvostudományi osztotta James Rothman , Randy Schekman és Thomas Sudhof a szerepük tisztázásához (építve a korábbi kutatások egy része azt a mentorok) a smink és funkciója sejt hólyagok, különösen élesztők és emberek, beleértve az egyes vezikulumok alkatrészeire és azok összeszerelésére vonatkozó információkat is. Úgy gondolják, hogy a vezikulum diszfunkciója hozzájárul az Alzheimer-kórhoz , a cukorbetegséghez , néhány nehezen kezelhető epilepsziás esethez , egyes rákokhoz és immunológiai rendellenességekhez, valamint bizonyos neurovaszkuláris állapotokhoz.
A hólyagos szerkezetek típusai
Vákuumok
A vakuolumok sejtes organellák, amelyek többnyire vizet tartalmaznak.
- A növényi sejtek egy nagy központi vacuole közepén a sejt, hogy használják az ozmotikus szabályozás és tápanyag tárolására.
- Összehúzódó vakuolokat találnak bizonyos protistákban , különösen a Phylum Ciliophora -ban . Ezek a vakuolumok vizet vesznek a citoplazmából, és kiválasztják a sejtből, hogy elkerüljék az ozmotikus nyomás miatti repedést .
Lizoszómák
- A lizoszómák részt vesznek a sejtek emésztésében. Az endocitózisnak nevezett eljárással a táplálék a sejten kívülről az élelmiszer -vakuolákba vihető be . Ezek az élelmiszer -vákuumok összeolvadnak lizoszómákkal, amelyek lebontják az összetevőket, így felhasználhatók a sejtben. A sejtes táplálkozásnak ezt a formáját fagocitózisnak nevezik .
- A lizoszómákat a hibás vagy sérült organellák elpusztítására is használják az autofágia nevű folyamatban. Összeolvadnak a sérült organellák membránjával, emésztik azt.
Szállító vezikulák
- A szállító vezikulumok molekulákat mozgathatnak a sejt belsejében, például fehérjéket a durva endoplazmatikus retikulumból a Golgi készülékbe .
- A membránhoz kötött és kiválasztott fehérjék a durva endoplazmatikus retikulumban található riboszómákon készülnek . Ezeknek a fehérjéknek a nagy része a Golgi -készülékben érik meg, mielőtt végső rendeltetési helyükre mennek, ami lehet lizoszómák , peroxiszómák vagy a sejten kívül. Ezek a fehérjék a szállító vezikulumok belsejében a sejtben utaznak.
Szekréciós hólyagok
A szekréciós vezikulumok olyan anyagokat tartalmaznak, amelyeket ki kell választani a sejtből. A sejteknek számos oka van az anyagok kiválasztására. Ennek egyik oka a hulladékok ártalmatlanítása. Egy másik ok a sejt funkciójához kapcsolódik. Egy nagyobb szervezeten belül egyes sejtek bizonyos vegyi anyagok előállítására specializálódtak. Ezeket a vegyi anyagokat szekréciós vezikulákban tárolják, és szükség esetén felszabadítják.
Típusok
- A szinaptikus vezikulumok a neuronok preszinaptikus termináljain helyezkednek el, és neurotranszmittereket tárolnak . Amikor egy jel lejön egy axonról , a szinaptikus vezikulák összeolvadnak a sejtmembránnal, amely felszabadítja a neurotranszmittert, így a következő idegsejt receptor molekulái észlelhetik .
- Állatokban endokrin szövetekben engedje hormonokat a véráramba. Ezeket a hormonokat a szekréciós vezikulákban tárolják. Jó példa erre a hasnyálmirigy Langerhans -szigetein található endokrin szövet . Ez a szövet számos sejttípust tartalmaz, amelyeket az általuk termelt hormonok határoznak meg.
- Szekréciós vezikulumokban tartsa az enzimeket, hogy használják, hogy a sejtfalak a növények , egysejtűek , gombák , baktériumok és Archaea sejtek, valamint az extracelluláris mátrix az állati sejtek .
- A baktériumok, az Archaea , a gombák és a paraziták változatos, de speciális toxikus vegyületeket és biokémiai jelmolekulákat tartalmazó membránvezikulákat (MV) bocsátanak ki, amelyeket a célsejtekhez szállítanak, hogy folyamatokat indítsanak a mikroba javára, beleértve a gazdasejtek invázióját és a versengő mikrobák elpusztítását. ugyanabban a fülkében.
Extracelluláris vezikulák
Az extracelluláris vezikulumok (EV) olyan kettősrétegű, lipidekkel határolt részecskék, amelyeket az élet minden területe termel, beleértve a komplex eukariótákat, mind a Gram-negatív, mind a Gram-pozitív baktériumokat, mikobaktériumokat és gombákat.
Típusok
- Az ektoszómák/mikrovezikulák közvetlenül a plazmamembránból hullanak ki, és mérete körülbelül 30 nm -től a mikronnál nagyobb átmérőig terjedhet ). Ide tartozhatnak a nagy részecskék, például a haldokló sejtek által kibocsátott apoptotikus vércseppek , egyes rákos sejtek által felszabadított nagy onkoszómák vagy a fonálférgek idegsejtjei és az egér kardiomiocitái által kibocsátott " exoferek ".
- Exoszómák : endocita eredetű hártyás vezikulák (30-100 nm átmérőjű).
Különböző típusú elektromos járművek elválaszthatók a sűrűség (gradiens differenciál centrifugálás ), a méret vagy a felületi markerek alapján. Az EV altípusok azonban átfedő méret- és sűrűségtartományokkal rendelkeznek, és az altípus-egyedi markereket cellánként kell meghatározni. Ezért nehéz meghatározni azt a biogenezis útvonalat, amely egy adott EV kialakulásához vezetett, miután elhagyta a sejtet.
Emberben az endogén extracelluláris vezikulumok valószínűleg szerepet játszanak az alvadásban, az intercelluláris jelátvitelben és a hulladékkezelésben. Szintén részt vesznek több betegség, köztük a rák patofiziológiai folyamataiban. Az extracelluláris vezikulák felkeltették az érdeklődést, mint a biomarker felfedezésének potenciális forrását, mivel szerepet játszanak az intercelluláris kommunikációban, a könnyen hozzáférhető testnedvekbe való felszabadulásukban és molekuláris tartalmuk hasonlóságában a felszabaduló sejtekkel. A (mezenchimális) őssejtek extracelluláris hólyagjait , más néven az őssejtek szekrécióját kutatják és alkalmazzák terápiás célokra, túlnyomórészt degeneratív , autoimmun és/vagy gyulladásos betegségekben.
Gram-negatív baktériumokban az EV-ket a külső membrán lecsípésével állítják elő; azonban még mindig nem ismert, hogy az EV-k hogyan menekülnek ki a Gram-pozitív baktériumok, mikobaktériumok és gombák vastag sejtfalából. Ezek az elektromos járművek változatos rakományt tartalmaznak, beleértve a nukleinsavakat, toxinokat, lipoproteineket és enzimeket, és fontos szerepet játszanak a mikrobiális fiziológiában és a patogenezisben. A gazda-kórokozó kölcsönhatások során a gram-negatív baktériumok hólyagokat termelnek, amelyek szerepet játszanak a kolonizációs rés kialakításában, virulenciafaktorok hordozásában és továbbításában a gazdasejtekben, valamint a gazdaszervezet védekezésének és válaszának modulálásában.
Megállapították, hogy az óceáni cianobaktériumok folyamatosan bocsátanak ki fehérjét, DNS -t és RNS -t tartalmazó hólyagokat a nyílt óceánba. A különböző baktériumokból származó DNS-t hordozó vezikulumok bőségesen megtalálhatók a tengerparti és nyílt tengeri tengervízmintákban.
Más típusok
A gázvezikulákat Archaea , baktériumok és planktonikus mikroorganizmusok használják, esetleg a függőleges migráció szabályozására a gáztartalom és ezáltal a felhajtóerő szabályozásával , vagy esetleg a sejt elhelyezésére a maximális napfénygyűjtés érdekében. Ezek a hólyagok jellemzően citrom alakú vagy hengeres csövek, amelyek fehérjéből készülnek; átmérőjük határozza meg a hólyag erejét, a nagyobbak gyengébbek. A hólyag átmérője befolyásolja a térfogatát és azt is, hogy milyen hatékonyan képes felhajtóerőt biztosítani. A cianobaktériumokban a természetes szelekció olyan hólyagokat hozott létre, amelyek a lehető legnagyobb átmérőjűek, ugyanakkor szerkezetileg stabilak. A fehérjebőr gázokat átereszt, de nem vizet, így a hólyagok nem áradnak el.
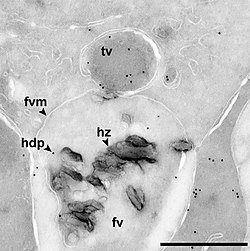
A mátrix vezikulák az extracelluláris térben vagy mátrixban helyezkednek el. Használata elektronmikroszkópia fedezték fel egymástól függetlenül 1967-ben H. Clarke Anderson és Ermanno Bonucci. Ezek a sejtből származó vezikulumok arra specializálódtak, hogy a mátrix biomineralizációját kezdeményezzék különféle szövetekben, beleértve a csontokat , a porcokat és a dentint . A normál meszesedés során a kalcium- és foszfátionok nagy beáramlása a sejtekbe kíséri a sejtes apoptózist (genetikailag meghatározott önpusztítást) és a mátrix vezikulumok képződését. A kalciumterhelés foszfatidil-szerin képződéséhez is vezet : kalcium: foszfát komplexek a plazmamembránban, amelyet részben az annexinek nevű fehérje közvetít . A mátrix vezikulumok a plazmamembránból bimbóznak az extracelluláris mátrixszal való kölcsönhatás helyén. Így a mátrix vezikulumok kalciumot, foszfátot, lipideket és annexineket szállítanak az extracelluláris mátrixba, amelyek az ásványi anyagok képződését befolyásolják. Ezeket a folyamatokat pontosan összehangolják, hogy a megfelelő helyen és időben a szövet mátrixának mineralizációját hozzák létre, kivéve, ha a Golgi nem létezik.
A multikuláris test vagy az MVB egy membránhoz kötött vezikulum, amely számos kisebb hólyagot tartalmaz.
Formálás és szállítás
| Sejtbiológia | |
|---|---|
| Állati sejtdiagram | |
 Egy tipikus állati sejt összetevői:
|
Néhány vezikulum akkor keletkezik, amikor a membrán egy része lecsípődik az endoplazmatikus retikulumról vagy a Golgi -komplexről. Mások akkor készülnek, amikor a sejten kívüli tárgyat a sejtmembrán veszi körül.
Hólyagburok és rakománymolekulák
A vezikuláris "szőrzet" olyan fehérjék gyűjteménye, amelyek a donor membrán görbületének alakítását szolgálják, és lekerekített hólyag alakot alkotnak. A szőrzetfehérjék működhetnek úgy is, hogy különböző transzmembrán receptorfehérjékhez kötődnek, az úgynevezett cargo receptorokhoz. Ezek a receptorok segítenek kiválasztani, hogy milyen anyag endocitózódik a receptor által közvetített endocitózisban vagy az intracelluláris transzportban.
Háromféle vezikulaforgalom kabátok: clathrin , COPI és copii . A különböző típusú szőrzetfehérjék segítenek a vezikulák végső rendeltetési helyükre történő válogatásában. Clathrin -bevonat található a Golgi és a plazmamembrán , a Golgi és az endoszómák, valamint a plazmamembrán és az endoszómák közötti forgalomban lévő vezikulákon . A COPI -val bevont vezikulumok felelősek a Golgi -ból az ER -be történő retrográd szállításért, míg a COPII -vel bevont vezikulumok az ER -ből a Golgi -ba történő anterográd szállításért.
A klatrin bevonatról úgy gondolják, hogy a szabályozó G fehérje hatására összeáll . A fehérjebevonat összeáll és szétszedődik egy ADP ribozilációs faktor (ARF) fehérje miatt.
Vezikula dokkolás
A SNARE -nek nevezett felszíni fehérjék azonosítják a vezikulum rakományát, és a célmembránon lévő kiegészítő SNARE -k a vezikulum és a célmembrán fúzióját okozzák. Az ilyen v-SNARES feltételezések szerint a vezikulum membránon léteznek, míg a célmembránon lévő komplementer t-SNARE-ként ismert.
Gyakran a vezikulákkal vagy célmembránokkal társított SNARE-ket Qa, Qb, Qc vagy R SNARE-k közé sorolják, az egyszerűbb v- vagy t-SNARE-oknál nagyobb eltérések miatt. Különböző SNARE komplexek sora látható különböző szövetekben és szubcelluláris rekeszekben, jelenleg 36 izoformát azonosítanak az emberekben.
Úgy gondolják, hogy a szabályozó Rab fehérjék megvizsgálják a SNARE -k összekapcsolódását. A Rab fehérje egy szabályozó GTP-kötő fehérje, és elég hosszú ideig szabályozza ezen komplementer SNARE-ek kötődését ahhoz, hogy a Rab fehérje hidrolizálja a megkötött GTP-t és rögzítse a vezikulumot a membránra.
A növényi SNARE -k alulvizsgáltak a gombákhoz és az állatokhoz képest. A sejt botanikus Natasha Raikhel tett néhány alapvető kutatásokat ezen a területen. Ő és csapata talált AtVTI1a lényegesnek a Golgi - vacuole közlekedés.
Vezikuláris fúzió
A vezikuláris fúzió kétféleképpen történhet: teljes fúzió vagy csók-fuss fúzió . A fúzióhoz a két membránt 1,5 nm -en belül kell elhelyezni. Ennek megvalósításához vizet kell kiszorítani a vezikulum membrán felületéről. Ez energetikailag kedvezőtlen, és a bizonyítékok arra utalnak, hogy a folyamathoz ATP , GTP és acetil-coA szükséges . A fúzió a bimbózáshoz is kapcsolódik, ezért merül fel a bimbózó és összeolvadó kifejezés.
A receptorok alulszabályozásában
A receptorként szolgáló membránfehérjéket időnként az ubiquitin kapcsolódása jelzi, hogy csökkentik a szabályozást . Miután a fent leírt úton megérkeztek egy endoszómához , vezikulák kezdenek kialakulni az endoszóma belsejében, és magukkal viszik a lebontásra szánt membránfehérjéket; Amikor az endoszóma érik, hogy lizoszómává váljon, vagy egyesüljön vele, a vezikulumok teljesen lebomlanak. E mechanizmus nélkül csak a membránfehérjék extracelluláris része érné el a lizoszóma lumenét, és csak ez a rész degradálódna.
Ezeknek a vezikulumoknak köszönhető, hogy az endoszómát néha multikuláris testnek nevezik . Kialakulásukhoz vezető út nem teljesen érthető; a többi fent ismertetett vezikulával ellentétben a hólyagok külső felülete nem érintkezik a citoszollal .
Készítmény
Elszigetelt hólyagok
A membrán vezikulumok előállítása az egyik módszer a sejt különböző membránjainak vizsgálatára. Miután az élő szövetet szuszpenzióvá zúzták , a különböző membránok apró zárt buborékokat képeznek. A zúzott sejtek nagy töredékeit kis sebességű centrifugálással el lehet dobni, majd később az ismert eredetű frakciót ( plazmalemma , tonoplaszt stb.) Elkülöníthetjük pontos, nagy sebességű centrifugálással a sűrűséggradiensben. Az ozmotikus sokk alkalmazásával lehetséges a vezikulumok ideiglenes kinyitása (a szükséges oldattal való feltöltés), majd ismét centrifugálás és más oldatban történő újraszuszpendálás. Az ionoforok, például a valinomicin alkalmazása elektrokémiai gradienseket hozhat létre, amelyek összehasonlíthatók az élő sejteken belüli gradiensekkel.
A hólyagokat elsősorban kétféle kutatásban használják:
- A membránreceptorok megtalálása és későbbi izolálása, amelyek specifikusan kötik a hormonokat és más fontos anyagokat.
- Különféle ionok vagy más anyagok szállításának vizsgálata az adott típusú membránon keresztül. Míg a szállítás könnyebben vizsgálható patch clamp technikákkal, a hólyagok elkülöníthetők olyan tárgyaktól is, amelyekre a tapaszbilincs nem alkalmazható.
Mesterséges hólyagok
A mesterséges vezikulumokat méretük alapján három csoportba sorolják: kis egyrétegű liposzómák/vezikulák (SUV -k) 20–100 nm mérettartományban, nagy unilamelláris liposzómák/vezikulák (LUV) 100–1000 nm mérettartományban és óriási egyrétegű liposzómák/vezikulák (GUV), 1-200 µm mérettartományban. A biokémiában és a kapcsolódó területeken gyakran használnak kisebb méretű vezikulákat, amelyek ugyanabban a mérettartományban vannak, mint az élő sejtekben található kereskedő vezikulák . Az ilyen vizsgálatokhoz homogén foszfolipid -hólyag -szuszpenziót állíthatunk elő extrudálással vagy ultrahangos kezeléssel , vagy egy foszfolipid -oldat vizes pufferoldatba történő gyors injektálásával. Ily módon vizes vezikulum oldatok készíthetők különböző foszfolipid összetételből, valamint különböző méretű vezikulákból. Nagyobb szintetikusan előállított vezikulákat, például GUV -ket használnak sejtbiológiai in vitro vizsgálatokhoz a sejtmembránok utánzása céljából. Ezek a hólyagok elég nagyok ahhoz, hogy hagyományos fluoreszcens fénymikroszkóppal vizsgálhassák őket. Különféle módszerek léteznek a biológiai reaktánsok, például fehérjeoldatok ilyen vezikulákba történő beágyazására, így a GUV-k ideális rendszerként szolgálnak a sejtfunkciók in vitro helyreállításához (és vizsgálatához) sejtszerű membránmodell-környezetben. Ezek a módszerek közé tartoznak a mikrofluidikus módszerek, amelyek lehetővé teszik a nagy hozamú, egyenletes méretű vezikulák termelését.
Lásd még
- Bleb (sejtbiológia)
- Gazda-kórokozó felület
- Membrán érintkezési helyek
- Membrán nanocső
- Membrán vezikulum -kereskedelem
- Micella
- Mikroszóma
- Protocell
- Spitzenkörper , a gombás hifákban található sok kis hólyag szerkezete
Hivatkozások
További irodalom
- Alberts, Bruce; et al. (1998). Alapvető sejtbiológia: Bevezetés a sejt molekuláris biológiájába . Garland Pub. ISBN 978-0-8153-2971-8.