Ér endothelialis növekedési faktor - Vascular endothelial growth factor
| vaszkuláris endoteliális növekedési faktor | |||||||
|---|---|---|---|---|---|---|---|
| Azonosítók | |||||||
| Álnevek | vaszkuláris endoteliális növekedési faktorok | ||||||
| Külső azonosítók | GeneCards : [1] | ||||||
| Ortológusok | |||||||
| Faj | Emberi | Egér | |||||
| Entrez |
|
|
|||||
| Ensembl |
|
|
|||||
| UniProt |
|
||||||
| RefSeq (mRNS) |
|
|
|||||
| RefSeq (fehérje) |
|
|
|||||
| Helyszín (UCSC) | nincs | nincs | |||||
| PubMed keresés | nincs | nincs | |||||
| Wikidata | |||||||
| |||||||
A vaszkuláris endoteliális növekedési faktor ( VEGF ), eredetileg vaszkuláris permeabilitási faktor ( VPF ), sok sejt által termelt jelfehérje , amely serkenti az erek kialakulását. Pontosabban: a VEGF a növekedési faktorok alcsaládja , a vérlemezke-eredetű növekedési faktor család, a cisztin-csomó növekedési faktorok. Ezek fontos jelzőfehérjék, amelyek részt vesznek mind a vaskulogenezisben (az embrionális keringési rendszer de novo képződésében ), mind az angiogenezisben (az erek növekedése a meglévő érrendszerből).
Ez a rendszer része, amely helyreállítja a szövetek oxigénellátását, ha a vérkeringés nem megfelelő, például hipoxiás körülmények között. A VEGF szérumkoncentrációja magas bronchiális asztmában és cukorbetegségben . A VEGF normál funkciója új erek létrehozása az embrionális fejlődés során , új erek létrehozása sérülés után, izmok edzés után, és új erek ( járulékos keringés ) a blokkolt erek megkerüléséhez. Hozzájárulhat a betegségekhez. A szilárd daganatok megfelelő vérellátás nélkül nem nőhetnek túl egy korlátozott méreten; a VEGF -et expresszáló rákok képesek növekedni és áttéteket okozni. A VEGF túlzott expressziója érrendszeri betegségeket okozhat a szem retinájában és a test más részein. Az olyan gyógyszerek, mint az aflibercept , a bevacizumab , a ranibizumab és a pegaptanib , gátolhatják a VEGF -et , és szabályozhatják vagy lassíthatják ezeket a betegségeket.
Történelem
1970 -ben Judah Folkman et al . leírt egy angiogeneziset okozó daganatok által kiválasztott faktort, és tumor angiogenezis faktornak nevezte . 1983 -ban Senger és mtsai. tengerimalacokban és hörcsögökben daganatok által kiválasztott vaszkuláris permeabilitási faktort azonosított . 1989 -ben Ferrara és Henzel azonos faktort írt le a szarvasmarha hipofízis tüszősejtjeiben, amelyeket tisztítottak, klónoztak és VEGF -nek neveztek el. Hasonló VEGF alternatív illesztést fedeztek fel Tischer és mtsai. 1996 és 1997 között Christinger és De Vos megszerezték a VEGF kristályszerkezetét, először 2,5 Å felbontással, később pedig 1,9 Å -vel.
Ferrara és munkatársai kimutatták, hogy az Fms-szerű tirozin-kináz-1 (flt-1) VEGF-receptor . 1992-ben A kináz inszert dómén receptor (KDR) kimutatták, hogy a VEGF receptor által Terman et al. 1992 -ben is. 1998 -ban kimutatták, hogy a neuropilin 1 és a 2 neuropilin VEGF -receptorként működik.
Osztályozás
Emlősökben a VEGF család öt tagból áll: VEGF-A , placenta növekedési faktor ( PGF ), VEGF-B , VEGF-C és VEGF-D . Az utóbbi tagokat a VEGF-A után fedezték fel; felfedezésük előtt a VEGF-A-t VEGF néven ismerték. Számos, VEGF-hez kapcsolódó, vírusok ( VEGF-E ) és egyes kígyók ( VEGF-F ) által kódolt fehérjét is felfedeztek.
| típus | Funkció |
|---|---|
| VEGF-A |
|
| VEGF-B | Embrionális angiogenezis (specifikus myocardialis szövet) |
| VEGF-C | Lymphangiogenezis |
| VEGF-D | Szükséges a tüdőhörgőket körülvevő nyirokérrendszer kifejlődéséhez |
| PlGF | Fontos a vaskulogenezis szempontjából, Ischaemia, gyulladás, sebgyógyulás és rák során is szükséges az angiogenezishez. |
A VEGF-A aktivitását, amint azt a neve is sugallja, többnyire az érrendszeri endothelium sejtjein tanulmányozták , bár számos más sejttípusra is hatással van (pl. Stimuláló monocita / makrofág migráció, neuronok, rákos sejtek, vesehám sejtek). In vitro a VEGF-A-ról kimutatták, hogy stimulálja az endothelsejtek mitogenezisét és a sejtvándorlást . A VEGF-A értágító is, és növeli a mikrovaszkuláris permeabilitást, és eredetileg vaszkuláris permeabilitási faktornak nevezték.
Izoformák
Vannak több izoformája VEGFA ezen eredmény a alternatív splicing az mRNS egyetlen, 8- exon VEGFA gént. Ezeket két csoportba sorolják, amelyekre a terminális exon (8. exon) illesztési helyük szerint hivatkozunk: a proximális összeillesztési hely (VEGF xxx ) vagy a disztális illesztési hely (VEGF xxx b). Ezenkívül a 6. és 7. exon alternatív illesztése megváltoztatja a heparint megkötő affinitásukat és aminosavszámukat (emberekben: VEGF 121 , VEGF 121 b, VEGF 145 , VEGF 165 , VEGF 165 b, VEGF 189 , VEGF 206 ; a rágcsáló ortológusok) ezen fehérjék eggyel kevesebb aminosavat tartalmaznak). Ezek a domének fontos funkcionális következményekkel járnak a VEGF illesztési változatokra nézve, mivel a terminális (exon 8) illesztési hely határozza meg, hogy a fehérjék pro-angiogenikusak (proximális illesztési hely, az angiogenezis során kifejezve) vagy anti-angiogenikusak (disztális illesztési hely, normálban kifejezve) szövetek). Ezenkívül a 6-os és 7-es exonok befogadása vagy kizárása közvetíti a kölcsönhatásokat a heparán-szulfát- proteoglikánokkal (HSPG-k) és a sejtfelszín neuropilin -receptoraival, fokozva a VEGF-receptorok (VEGFR-ek) megkötési és aktiválási képességét . A közelmúltban a VEGF-C-ről kimutatták, hogy fontos indukálója a neurogenezisnek az egér szubventrikuláris zónában anélkül, hogy angiogén hatást gyakorolna.
Gépezet
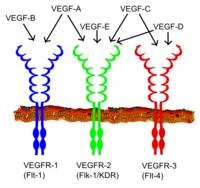
A VEGF család minden tagja stimulálja a sejtválaszokat azáltal, hogy kötődik a tirozin -kináz receptorokhoz ( VEGFR -ek ) a sejtfelszínen, ami miatt dimerizálódnak és aktiválódnak a transzfoszforiláció révén , bár különböző helyeken, időpontokban és mértékben. A VEGF receptoroknak van egy extracelluláris része, amely 7 immunglobulin-szerű domént tartalmaz, egyetlen transzmembrán átfogó régiót és egy osztott tirozin-kináz domént tartalmazó intracelluláris részt . A VEGF-A kötődik a VEGFR-1-hez ( Flt-1 ) és a VEGFR-2-hez ( KDR/Flk-1 ). Úgy tűnik, hogy a VEGFR-2 közvetíti a VEGF-re adott összes ismert celluláris választ. A VEGFR-1 funkciója kevésbé jól meghatározott, bár úgy gondolják, hogy modulálja a VEGFR-2 jelátvitelt. A VEGFR-1 egy másik funkciója lehet, hogy próbabábu/csalétkeztetőként viselkedik, elválasztva a VEGF-et a VEGFR-2 kötődéstől (ez különösen fontosnak tűnik az embrió vasculogenezisében). A VEGF-C és a VEGF-D, de nem a VEGF-A, ligandumok egy harmadik receptorhoz ( VEGFR-3/Flt4 ), amely a limfangiogenezist közvetíti . A receptor (VEGFR3) a fő ligandumok (VEGFC és VEGFD) kötődésének helye, amely közvetíti a ligandumok állandó hatását és működését a célsejteken. A vaszkuláris endoteliális növekedési faktor-C stimulálhatja a limfangiogenezist (VEGFR3-on keresztül) és az angiogenezist a VEGFR2-n keresztül. A vaszkuláris endoteliális növekedési faktor-R3-at számos faj, szarvasmarha, bivaly és főemlősök CL-jében észlelték a nyirokrendszeri endothelsejtekben.
A VEGFR -ekhez való kötődés mellett a VEGF a neuropilinekből és a VEGFR -ekből álló receptor komplexekhez is kötődik . Ez a receptor komplex fokozta a VEGF jelátviteli aktivitást az endothelsejtekben ( erekben ). A neuropilinek (NRP) pleitrofikus receptorok, ezért más molekulák zavarhatják az NRP/VEGFR receptor komplexek jelátvitelét. Például a 3. osztályú szemaforinok versenyeznek a VEGF 165- tel az NRP kötődéséért, és ezért szabályozhatják a VEGF által közvetített angiogenezist .
Kifejezés
A VEGF-A termelés indukálható olyan sejtben, amely nem kap elegendő oxigént . Ha egy sejt oxigénhiányos, akkor HIF-et, hipoxia-indukálható faktort , transzkripciós faktort termel . A HIF stimulálja a VEGF-A felszabadulását, többek között (beleértve az eritropoézis modulációját). A keringő VEGF-A ezután kötődik az endothelsejtek VEGF-receptorához, és kiváltja az angiogenezishez vezető tirozin-kináz útvonalat. Az angiopoietin-2 expressziója VEGF hiányában endoteliális sejthalálhoz és vaszkuláris regresszióhoz vezet. Ezzel szemben egy német in vivo tanulmány kimutatta, hogy a VEGF -koncentrációk valójában csökkentek, miután 25% -kal csökkentették az oxigénbevitelt 30 percen keresztül. A HIF1 alfa és a HIF1 béta folyamatosan termelődik, de a HIF1 alfa erősen O 2 labilis, ezért aerob körülmények között lebomlik. Amikor a sejt hipoxiássá válik, a HIF1 alfa megmarad, és a HIF1alfa/béta komplex stimulálja a VEGF felszabadulását. a mikrovezikulák és az 5-FU együttes alkalmazása a laphámsejtes karcinóma sejtek kemoszenzitivitását fokozta, mint az 5-FU vagy a mikrovezikula önmagában történő alkalmazása. Ezenkívül a VEGF génexpresszió csökkent szabályozása a CD1 gén expressziójának csökkenésével járt.
Klinikai jelentőség
Betegségben
A VEGF-A és a megfelelő receptorok gyorsan felszabályozódnak a központi idegrendszer (CNS) traumás sérülése után . A VEGF-A erősen expresszálódik a központi idegrendszeri károsodás akut és szubakut szakaszában, de a fehérje expresszió idővel csökken. A VEGF-A expressziónak ez az időtartama megfelel a sérülés utáni endogén re-vascularisációs képességnek. Ez azt sugallja, hogy a VEGF-A / VEGF 165 -öt célpontként lehetne használni a központi idegrendszeri sérülések utáni angiogenezis elősegítésére. Azonban ellentmondásos tudományos jelentések vannak a VEGF-A kezelések hatásáról a központi idegrendszeri sérülési modellekben.
Bár nem társították biomarkerként az akut ischaemiás stroke diagnosztizálásához , ha az első 48 órában a VEGF magas szintje a szérumban rossz előrejelzéssel járt a 6 hónapnál és 2 évnél hosszabb agyi infarktusnál.
A VEGF-A rossz prognózisú a mellrákban . Számos tanulmány szerint csökken a teljes túlélés és a betegségmentes túlélés azokban a daganatokban, amelyek túlzottan expresszálják a VEGF-et. A VEGF-A túlexpressziója a metasztázisok folyamatának korai lépése lehet , ami az "angiogenikus" kapcsoló. Bár a VEGF-A-t összefüggésbe hozták a rossz túléléssel, pontos hatásmechanizmusa a daganatok progressziójában továbbra sem világos.
A VEGF-A is felszabadul a rheumatoid arthritis válaszul TNF-α , növekvő endoteliális permeabilitást és duzzanat és serkenti az angiogenezist (képződését kapillárisok).
A VEGF-A fontos a diabéteszes retinopátiában (DR) is. A cukorbetegek retinájában fellépő mikrocirkulációs problémák retinális iszkémiát okozhatnak, ami a VEGF-A felszabadulását eredményezi, és az angiogén VEGF xxx izoformák egyensúlyának megváltozását eredményezi a normálisan expresszált VEGF xxx b izoformákhoz képest. A VEGF xxx új erek kialakulását idézheti elő a retinában és a szem más részein, ami változásokat jelezhet, amelyek veszélyeztethetik a látást.
A VEGF-A szerepet játszik az időskori makuladegeneráció (AMD) nedves formájának betegség patológiájában , amely az iparosodott világ idős korának vezető vakságának fő oka. Az AMD érrendszeri patológiája bizonyos hasonlóságokat mutat a diabéteszes retinopátiával, bár a betegség oka és a neovaszkularizáció tipikus forrása eltér a két betegség között.
A VEGF-D szérumszintje szignifikánsan emelkedett angiosarcoma betegeknél .
A kiadás után a VEGF-A számos választ válthat ki. Ez egy sejt túlélését, mozgását vagy további differenciálódását okozhatja . Ezért a VEGF potenciális célpont a rák kezelésében . Az első anti-VEGF gyógyszert, a bevacizumab nevű monoklonális antitestet 2004-ben hagyták jóvá. A betegek megközelítőleg 10-15% -a részesül a bevacizumab-terápia előnyeiből; a bevacizumab hatékonyságának biomarkerei azonban még nem ismertek.
A jelenlegi tanulmányok azt mutatják, hogy a VEGF -ek nem az egyedüli promóterek az angiogenezisben. Különösen az FGF2 és a HGF erős angiogenikus tényezők.
A pulmonalis emfizémában szenvedő betegeknél csökkent a VEGF szintje a pulmonális artériákban.
Kimutatták, hogy a VEGF-D túlzottan kifejeződik lymphangioleiomyomatosisban, és jelenleg diagnosztikai biomarkerként használják ezt a ritka betegséget.
A vesében a VEGF-A fokozott expressziója a glomerulusokban közvetlenül a glomeruláris hipertrófiát okozza, amely proteinuriával jár.
A VEGF elváltozások előre jelezhetik a pre-eklampsziát .
A refrakter angina génterápiái megalapozzák a VEGF expresszióját az epicardialis sejtekben az angiogenezis elősegítése érdekében.
Lásd még
- Proteázok az angiogenezisben
- Withaferin A , az angiogenezis hatékony inhibitora
Hivatkozások
További irodalom
- Bengoetxea H, Argandoña EG, Lafuente JV (2008). "A vizuális tapasztalatok hatása a vaszkuláris endoteliális növekedési faktor expressziójára a patkányi vizuális kéreg postnatális fejlődése során" . Agykéreg . 18 (7): 1630–39. doi : 10.1093/cercor/bhm190 . PMC 2430152 . PMID 17986606 .
- Zan L, Wu H, Jiang J, Zhao S, Song Y, Teng G, Li H, Jia Y, Zhou M, Zhang X, Qi J, Wang J (2011). "Az Src, az SSeCKS és az angiogenikus tényezők időbeli profilja a fokális agyi ischaemia után: korrelációk az angiogenezissel és az agyi ödémával" . Neurochem. Int . 58. (8): 872–9. doi : 10.1016/j.neuint.2011.02.014 . PMC 3100427 . PMID 21334414 .
- Zan L, Zhang X, Xi Y, Wu H, Song Y, Teng G, Li H, Qi J, Wang J (2014). "Az Src szabályozza az angiogenikus tényezőket és a vaszkuláris permeabilitást a fokális agyi ischaemia-reperfúzió után" . Idegtudomány . 262 : 118–28. doi : 10.1016/j.neuroscience.2013.12.060 . PMC 3943922 . PMID 24412374 .
- Wang J, Fu X, Jiang C, Yu L, Wang M, Han W, Liu L, Wang J (2014). "A csontvelő mononukleáris sejt-transzplantációja elősegíti a terápiás angiogenezist a VEGF-VEGFR2 jelátviteli út felfelé történő szabályozásával az érrendszeri demencia patkánymodelljében" . Behav. Brain Res . 265 : 171–80. doi : 10.1016/j.bbr.2014.02.033 . PMC 4000455 . PMID 24589546 .
- Ferrara N, Gerber HP (2002). "A vaszkuláris endoteliális növekedési faktor szerepe az angiogenezisben". Acta Haematol . 106. (4): 148–56. doi : 10.1159/000046610 . PMID 11815711 . S2CID 46785882 .
- Orpana A, Salven P (2003). "Angiogenikus és limfangiogenikus molekulák hematológiai rosszindulatú daganatokban". Leuk. Limfóma . 43. (2): 219–24. doi : 10.1080/10428190290005964 . PMID 11999550 . S2CID 21908151 .
- Afuwape AO, Kiriakidis S, Paleolog EM (2003). "A VEGF angiogenikus molekula szerepe a rheumatoid arthritis patogenezisében". Histol. Histopathol . 17 (3): 961–72. PMID 12168808 .
- de Bont ES, Neefjes VM, Rosati S, et al. (2003). "Új érképződés és aberráns VEGF/VEGFR jelzés akut leukémiában: számít?" Leuk. Limfóma . 43. (10): 1901–9. doi : 10.1080/1042819021000015844 . PMID 12481883 . S2CID 45095413 .
- Ria R, Roccaro AM, Merchionne F, et al. (2003). "Vascularis endothelialis növekedési faktor és annak receptorai myeloma multiplexben" . Leukémia . 17 (10): 1961–6. doi : 10.1038/sj.leu.2403076 . PMID 14513045 .
- Caldwell RB, Bartoli M, Behzadian MA, et al. (2004). "Vaszkuláris endoteliális növekedési faktor és diabéteszes retinopátia: patofiziológiai mechanizmusok és kezelési perspektívák". Cukorbetegség Metab. Res. Rev . 19 (6): 442–55. doi : 10.1002/dmrr.415 . PMID 14648803 . S2CID 24931730 .
- Patan, Sybill (2004). "Vaszkulogenezis és angiogenezis". Angiogenezis az agydaganatokban . Rákkezelés és kutatás. 117 . 3–32. doi : 10.1007/978-1-4419-8871-3_1 . ISBN 978-1-4613-4699-9. PMID 15015550 .
- Machein, Marcia Regina; Plate, Karl Heinz (2004). "A VEGF szerepe a fejlődési angiogenezisben és a tumor angiogenezisében az agyban". Angiogenezis az agydaganatokban . Rákkezelés és kutatás. 117 . 191–218. doi : 10.1007/978-1-4419-8871-3_13 . ISBN 978-1-4613-4699-9. PMID 15015562 .
- Eremina V., Quaggin SE (2004). "A VEGF-A szerepe a glomeruláris fejlődésben és működésben". Curr. Opin. Nephrol. Hypertens . 13. (1): 9–15. doi : 10.1097/00041552-200401000-00002 . PMID 15090854 . S2CID 24212588 .
- Storkebaum E, Lambrechts D, Carmeliet P (2004). "VEGF: valamikor specifikus angiogenikus tényezőnek tekintették, ma pedig részt vesz a neuroprotekcióban". Bio -esszék . 26 (9): 943–54. doi : 10.1002/bies.20092 . PMID 15351965 . S2CID 871954 .
- Ribatti D (2005). "A vaszkuláris permeabilitási faktor/vaszkuláris endoteliális növekedési faktor döntő szerepe az angiogenezisben: történelmi áttekintés" . Br. J. Haematol . 128 (3): 303–9. doi : 10.1111/j.1365-2141.2004.05291.x . PMID 15667531 .
- Loureiro RM, D'Amore PA (2005). "A vascularis endothelialis növekedési faktor transzkripciós szabályozása rákban". A citokin növekedési faktor rev . 16 (1): 77–89. doi : 10.1016/j.cytogfr.2005.01.005 . PMID 15733833 .
- Herbst RS, Onn A, Sandler A (2005). "Angiogenezis és tüdőrák: prognosztikai és terápiás következmények". J. Clin. Oncol . 23 (14): 3243–56. doi : 10.1200/JCO.2005.18.853 . PMID 15886312 .
- Pufe T, Kurz B, Petersen W, et al. (2006). "A biomechanikai paraméterek hatása a VEGF és az endosztatin expressziójára a csont- és ízületi rendszerben". Ann. Anat . 187 (5–6): 461–72. doi : 10.1016/j.aanat.2005.06.008 . PMID 16320826 .
- Tong JP, Yao YF (2006). "A VEGF és a PEDF hozzájárulása a koroidális angiogenezishez: szükség van a kiegyensúlyozott kifejezésekre". Clin. Biochem . 39 (3): 267–76. doi : 10.1016/j.clinbiochem.2005.11.013 . PMID 16409998 .
- Lambrechts D, Carmeliet P (2007). "VEGF a neurovaszkuláris határfelületen: terápiás következmények a motoros neuron betegségben" . Biochim. Biophys. Acta . 1762 (11–12): 1109–21. doi : 10.1016/j.bbadis.2006.04.005 . PMID 16784838 .
- Matsumoto T, Mugishima H (2006). "Jelátvitel vaszkuláris endoteliális növekedési faktor (VEGF) receptorokon keresztül és szerepük az atherogenezisben" . J. Atheroscler. Tromb . 13 (3): 130–5. doi : 10.5551/jat.13.130 . PMID 16835467 .
- Bogaert E, Van Damme P, Van Den Bosch L, Robberecht W (2006). "Vascularis endothelialis növekedési faktor amyotrophic lateral sclerosisban és más neurodegeneratív betegségekben". Izomideg . 34. (4): 391–405. doi : 10.1002/mus.20609 . PMID 16856151 . S2CID 22086357 .
- Mercurio AM, Lipscomb EA, Bachelder RE (2006). "A VEGF nem angiogenikus funkciói az emlőrákban". Journal of Emlőmirigy Biológia és Neoplasia . 10 (4): 283–90. CiteSeerX 10.1.1.476.2778 . doi : 10.1007/s10911-006-9001-9 . PMID 16924371 . S2CID 16565983 .
- Makinde T, Murphy RF, Agrawal DK (2007). "A vaszkuláris endoteliális növekedési faktor és az angiopoietin-1 immunmoduláló szerepe a légutak átalakításában". Curr. Mol. Med . 6 (8): 831–41. doi : 10.2174/156652406779010795 . PMID 17168735 .
- Rini BI, Rathmell WK (2007). "A vascularis endothelialis növekedési faktor biológiai vonatkozásai és kötési stratégiái a vesesejtes karcinómában" . Clin. Cancer Res . 13. (2 Pt 2): 741–746. doi : 10.1158/1078-0432.CCR-06-2110 . PMID 17255303 .
- Jiang, Chao; Zuo, Fangfang; Wang, Yuejuan; Lu, Hong; Yang, Qingwu; Wang, Jian (2017. január 1.). "A progeszteron megváltoztatja a VEGF és a BDNF expresszióját, és elősegíti a neurogenezist ischaemiás stroke után" . Molekuláris neurobiológia . 54. (1): 571–581. doi : 10.1007/s12035-015-9651-y . PMC 4938789 . PMID 26746666 .
- Rodgers LS, Lalani S, Hardy KM, Xiang X, Broka D, Antin PB, Camenisch TD (2006). "A depolimerizált hialuronán vaszkuláris endothel növekedési faktort indukál, amely a fejlődő hám-mesenchymális transzformáció negatív szabályozója" . Circ. Res . 99 (6): 583–9. doi : 10.1161/01.RES.0000242561.95978.43 . PMID 16931798 .
- Qaum, T; Xu, Q; Joussen, AM; et al. (2001). "VEGF által kezdeményezett vér-retina gát lebontása a cukorbetegség korai szakaszában". Invest Ophthalmol Vis Sci . 42 (10): 2408–2413. PMID 11527957 .
Külső linkek
- Érrendszeri + Endotheliális + Növekedési + tényezők az amerikai National Library of Medicine orvosi tárgyszórendszere (mm)
- Proteopedia Vascular_Endothelial_Growth_Factor - az érrendszeri endoteliális növekedési faktor szerkezete interaktív 3D -ben


