Klór - Chlorine
 | |||||||||||||||||||||||
| Klór | |||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Kiejtés |
/ K L ɔːr I n , - aɪ N / ( KLOR -een, -yne ) |
||||||||||||||||||||||
| Megjelenés | halványsárga-zöld gáz | ||||||||||||||||||||||
| Standard atomsúly A r, std (Cl) | [35.446 , 35.457 ] hagyományos: 35,45 | ||||||||||||||||||||||
| Klór a periódusos rendszerben | |||||||||||||||||||||||
| |||||||||||||||||||||||
| Atomi szám ( Z ) | 17 | ||||||||||||||||||||||
| Csoport | 17. csoport (halogének) | ||||||||||||||||||||||
| Időszak | 3. időszak | ||||||||||||||||||||||
| Blokk | p-blokk | ||||||||||||||||||||||
| Elektron konfiguráció | [ Ne ] 3s 2 3p 5 | ||||||||||||||||||||||
| Elektronok héjonként | 2, 8, 7 | ||||||||||||||||||||||
| Fizikai tulajdonságok | |||||||||||||||||||||||
| Fázis az STP -n | gáz | ||||||||||||||||||||||
| Olvadáspont | (Cl 2 ) 171,6 K (-101,5 ° C, -150,7 ° F) | ||||||||||||||||||||||
| Forráspont | (Cl 2 ) 239,11 K (-34,04 ° C, -29,27 ° F) | ||||||||||||||||||||||
| Sűrűség (STP -n) | 3,2 g/l | ||||||||||||||||||||||
| amikor folyékony ( bp ) | 1,5625 g/cm 3 | ||||||||||||||||||||||
| Kritikus pont | 416,9 K, 7,991 MPa | ||||||||||||||||||||||
| Fúziós hő | (Cl 2 ) 6,406 kJ/mol | ||||||||||||||||||||||
| Párolgás hője | (Cl 2 ) 20,41 kJ/mol | ||||||||||||||||||||||
| Moláris hőkapacitás | (Cl 2 ) 33,949 J/(mol · K) |
||||||||||||||||||||||
Gőznyomás
| |||||||||||||||||||||||
| Atomi tulajdonságok | |||||||||||||||||||||||
| Az oxidációs állapotok | −1 , +1 , +2, +3 , +4, +5 , +6, +7 (erősen savas oxid) | ||||||||||||||||||||||
| Elektronegativitás | Pauling skála: 3.16 | ||||||||||||||||||||||
| Ionizációs energiák | |||||||||||||||||||||||
| Kovalens sugár | 102 ± 16 óra | ||||||||||||||||||||||
| Van der Waals sugara | 175 óra | ||||||||||||||||||||||
| A klór spektrális vonalai | |||||||||||||||||||||||
| Egyéb tulajdonságok | |||||||||||||||||||||||
| Természetes előfordulás | ősi | ||||||||||||||||||||||
| Kristályszerkezet | rombos | ||||||||||||||||||||||
| Hangsebesség | 206 m/s (gáz, 0 ° C -on) | ||||||||||||||||||||||
| Hővezető | 8,9 × 10 - 3 W/(m⋅K) | ||||||||||||||||||||||
| Elektromos ellenállás | > 10 Ω⋅m (20 ° C -on) | ||||||||||||||||||||||
| Mágneses rendezés | diamágneses | ||||||||||||||||||||||
| Moláris mágneses fogékonyság | −40,5 × 10 −6 cm 3 /mol | ||||||||||||||||||||||
| CAS -szám | Cl 2 : 7782-50-5 | ||||||||||||||||||||||
| Történelem | |||||||||||||||||||||||
| Felfedezés és első elszigeteltség | Carl Wilhelm Scheele (1774) | ||||||||||||||||||||||
| Elemként ismerte fel | Humphry Davy (1808) | ||||||||||||||||||||||
| A klór fő izotópjai | |||||||||||||||||||||||
| |||||||||||||||||||||||
A klór egy kémiai elem a szimbólum Cl és atomi száma 17. A második-legkönnyebb a halogének , úgy tűnik, közötti fluor- és brómatom a periódusos, és tulajdonságai többnyire köztes közöttük. A klór sárga-zöld gáz szobahőmérsékleten. Rendkívül reaktív elem és erős oxidálószer : az elemek közül a legnagyobb elektron-affinitással és a harmadik legnagyobb elektronegativitással rendelkezik a felülvizsgált Pauling-skálán , csak az oxigén és a fluor mögött . A felülvizsgált Pauling-skálán kívül számos skálán a nitrogén elektronegativitása is nagyobb, mint a klóré, például az Allen , Allred -Rochow, Martynov-Batsanov, Mulliken-Jaffe , Nagle és Noorizadeh-Shakerzadeh elektronegativitási skálákon.
A klór fontos szerepet játszott a középkori alkimisták által végzett kísérletekben , amelyek általában klorid -sók, például ammónium -klorid ( salmon -ammónia ) és nátrium -klorid ( közönséges só ) hevítését foglalják magukban , különböző klórtartalmú vegyi anyagok, például hidrogén -klorid , higany (II. ) klorid (maró szublimátum) és sósav ( aqua regia formájában ). A szabad klórgáz mint különálló anyag természetét azonban csak 1630 körül ismerte fel Jan Baptist van Helmont . Carl Wilhelm Scheele 1774 -ben írt egy leírást a klórgázról, feltételezve, hogy ez egy új elem oxidja . 1809 -ben a vegyészek azt javasolták, hogy a gáz tiszta elem lehet, és ezt Sir Humphry Davy 1810 -ben megerősítette , aki színe miatt az ókori görögről χλωρός ( khlōrós , "halványzöld") nevet adta .
Nagy reaktivitása miatt a földkéregben lévő összes klór ionos kloridvegyületek formájában van , amely magában foglalja az asztali sót is. Ez a második leggyakoribb halogén (a fluor után) és a huszonegyedik leggyakoribb kémiai elem a földkéregben. Ezek a kéreglerakódások azonban eltörpülnek a tengervíz hatalmas kloridkészletei mellett.
Elemi klórt a kereskedelemben elő sóoldattal által elektrolízissel , főleg a klór-alkáli folyamat. Az elemi klór magas oxidációs potenciálja kereskedelmi fehérítők és fertőtlenítőszerek kifejlesztéséhez vezetett , és reagens a vegyipar számos folyamatához. A klórt a fogyasztási cikkek széles skálájának gyártásához használják, ezek körülbelül kétharmada szerves vegyi anyag, például polivinil-klorid (PVC), sok köztes termék műanyagok előállításához és más, az elemet nem tartalmazó végtermékek. Általános fertőtlenítőszerként az elemi klórt és a klórt előállító vegyületeket közvetlenül használják az úszómedencékben, hogy megőrizzék higiéniájukat . A magas koncentrációjú elemi klór rendkívül veszélyes és mérgező a legtöbb élő szervezetre. Ennek vegyi hadviselés ügynök, klór- használta először az I. világháború , mint a mérges gáz fegyver.
Kloridionok formájában a klór szükséges az összes ismert életfajhoz. Más típusú klórvegyületek ritkák az élő szervezetekben, és a mesterségesen előállított klórozott szerves anyagok az inerttől a mérgezőig terjednek. A felső légkörben klórtartalmú szerves molekulák, például klór-fluor-szénhidrogének vesznek részt az ózonréteg lebontásában . Kis mennyiségű elemi klór keletkezik a kloridnak a neutrofilekben lévő hipoklorittá oxidálásakor, a baktériumok elleni immunrendszer válaszának részeként .
Történelem
A klór leggyakoribb vegyülete, a nátrium -klorid az ókor óta ismert; a régészek bizonyítékokat találtak arra, hogy a kősót már i. e. 3000 -ben, a sóoldatot pedig már ie 6000 -ben használták. Az élelmiszerben betöltött jelentősége a klasszikus ókorban nagyon jól ismert volt, és néha a római tábornokok és katonai tribunusok szolgáltatásaiért fizettek.
Korai felfedezések
900 körül, a szerzők az arab írások tulajdonított Jabir ibn Hayyan (latin: Géber), valamint a perzsa orvos és alkimista Abu Bakr al-Razi ( c. 865-925, latin: Rhazes) kísérleteztek ammóniumkarbonát ( ammónium-klorid ) , amely vitriollal ( különböző fémek hidratált szulfátjai ) együtt desztillálva hidrogén -kloridot termel . Úgy tűnik azonban, hogy ezekben a korai klorid -sókkal végzett kísérletekben a gáz halmazállapotú termékeket elvetették, és a hidrogén -kloridot sokszor előállíthatták, mielőtt felfedezték, hogy vegyi felhasználásra is alkalmas. Az egyik első ilyen felhasználások volt a szintézisét higany (II) kloridot (maró hatású szublimátum), amelynek termelése a fűtési a higany akár timsó és ammónium-kloriddal vagy Fehérgálic és nátrium-klorid le először a De aluminibus et salibus (” a Alums és sók”, egy tizenegyedik vagy tizenkettedik században arab szöveg tévesen tulajdonított Abu Bakr al-Razi és fordította latinra a második felében a tizenkettedik században a Gerard Cremona , 1144-1187). Egy másik fontos fejlesztési felfedezése volt a pszeudo-Geber (a De inventione Veritatis , „On az igazság felfedezése” után c. 1300), hogy a hozzáadott ammónium-klorid, hogy salétromsavat , egy erős oldani képes oldószerrel arany (azaz, aqua regia ) előállítható. Bár az aqua regia egy instabil keverék, amely folyamatosan szabad klórgázt tartalmazó füstöt bocsát ki, úgy tűnik, hogy ezt a klórgázt egészen a kb. 1630 -ban, amikor Jan Baptist van Helmont flamand vegyész és orvos felismerte annak jellegét, mint külön gáznemű anyagot .

Elkülönítés
Az elemet először 1774 -ben tanulmányozta részletesen Carl Wilhelm Scheele svéd vegyész , és neki köszönhetik a felfedezést. Scheele klórt állított elő MnO 2 (ásványi piroluszitként ) és HCl reagáltatásával :
- 4 HCl + MnO 2 → MnCl 2 + 2 H 2 O + Cl 2
Scheele megfigyelt számos tulajdonságait klór: A fehérítő hatás lakmusz , a halálos hatása a rovarokra, a sárga-zöld színű, és a szag hasonló aqua regia . Ezt " deflogisztikált gyömbösav -levegőnek " nevezte, mivel ez egy gáz (akkor " levegőnek " hívták), és sósavból származott (akkor még "muriatsav"). Nem sikerült megállapítani a klórt elemként.
Az akkori általános kémiai elmélet szerint a sav olyan vegyület, amely oxigént tartalmaz (ennek maradványai a német és a holland oxigénnevekben is fennmaradnak : sauerstoff vagy zuurstof , mindkettő savas anyagként angolra fordítva ), ezért számos vegyész, köztük Claude Berthollet azt javasolta, hogy Scheele deflogisztikussav -gátló levegőjének oxigén és a még felfedezetlen elem, a muriaticum kombinációjának kell lennie .
1809-ben Joseph Louis Gay-Lussac és Louis-Jacques Thénard megpróbálták lebontani a deflogizált muriasav-levegőt úgy, hogy szénnel reagálva felszabadították a muriaticum (és a szén-dioxid) szabad elemét . Nem jártak sikerrel, és jelentést tettek közzé, amelyben mérlegelték annak lehetőségét, hogy a deflogisztizált gyömsav -levegő elem, de nem győzték meg.
1810 -ben Sir Humphry Davy ismét megpróbálta ugyanazt a kísérletet, és arra a következtetésre jutott, hogy az anyag elem, nem pedig vegyület. Az eredményeket az év november 15 -én jelentette be a Royal Society -nek. Abban az időben ezt az új elemet "klórnak" nevezte el, a görög χλωρος ( chlōros , "zöld-sárga") szóból, színére való hivatkozással. A " halogén " elnevezést, azaz "sótermelőt" eredetileg Johann Salomo Christoph Schweigger használta 1811 -ben a klórhoz . Ezt a kifejezést később általános kifejezésként használták a klórcsalád összes elemének (fluor, bróm, jód) leírására, Jöns Jakob Berzelius 1826 -os javaslata után . 1823 -ban Michael Faraday először cseppfolyósította a klórt, és bemutatta hogy az akkor "szilárd klórnak" nevezett klórhidrát (Cl 2 · H 2 O) szerkezetű.
Későbbi felhasználások
A klórgázt először Claude Berthollet francia kémikus használta textíliák fehérítésére 1785 -ben. A modern fehérítőszereket Berthollet további munkája eredményezte, aki először 1789 -ben gyártott nátrium -hipokloritot Javel városában (ma Párizs , Franciaország) található laboratóriumában. klórgázt vezetnek át nátrium -karbonát oldatán. A kapott folyadék, amelyet " Eau de Javel " (" Javel víz ") néven ismert, gyenge nátrium -hipoklorit oldat volt . Ez az eljárás nem volt túl hatékony, alternatív gyártási módszereket kerestek. Charles Tennant skót vegyész és iparos először kalcium -hipoklorit ("klórozott mész"), majd szilárd kalcium -hipoklorit (fehérítő por) oldatát állította elő . Ezek a vegyületek alacsony mennyiségű elemi klórt termeltek, és hatékonyabban szállíthatók voltak, mint a nátrium -hipoklorit, amely híg oldatként maradt, mert a víz eltávolítása érdekében veszélyesen erős és instabil oxidálószerré vált. A tizenkilencedik század vége felé ES Smith szabadalmaztatott egy nátrium -hipoklorit -előállítási módszert, amely magában foglalja a sóoldat elektrolízisét , hogy nátrium -hidroxidot és klórgázt állítsanak elő , majd keverés közben nátrium -hipokloritot képeznek. Ez az úgynevezett kloralkáli -eljárás , amelyet először 1892 -ben vezettek be ipari méretekben, és most a legtöbb elemi klór és nátrium -hidroxid forrása. 1884 -ben a német Chemischen Fabrik Griesheim kifejlesztett egy másik klóralkáli eljárást, amely 1888 -ban lépett kereskedelmi forgalomba.
A kémiailag bázikus vízben (nátrium- és kalcium-hipoklorit ) feloldott elemi klóroldatokat először az 1820-as években, Franciaországban, jóval a betegség csíraelméletének megalkotása előtt használták rothadásgátló és fertőtlenítőszerként . Ennek a gyakorlatnak az úttörője Antoine-Germain Labarraque volt , aki Berthollet "Javel water" fehérítőjét és más klórkészítményeket adaptált (a teljes körű történetért lásd alább). Az elemi klór azóta folyamatos funkciót tölt be a helyi antiszeptikában ( seböblítő oldatok és hasonlók) és a közegészségügyben, különösen az úszó- és ivóvízben.
A klórgázt először a német hadsereg használta fegyverként 1915. április 22 -én Ypresben . A szövetségesekre gyakorolt hatás pusztító volt, mert a meglévő gázálarcokat nehéz volt bevetni, és nem terjedt el széles körben.
Tulajdonságok

A klór a második halogén , mivel nem periodikus a periódusos rendszer 17. csoportjában. Tulajdonságai tehát hasonlóak a fluorhoz , a brómhoz és a jódhoz , és jórészt köztesek az első kettő között. A klór elektronkonfigurációja [Ne] 3s 2 3p 5 , a harmadik és legkülső héjban lévő hét elektron vegyértékelektronjaként működik . Mint minden halogén, így egy elektron hiányzik a teljes oktettől, és ezért erős oxidálószer, és számos elemmel reagál annak érdekében, hogy befejezze külső burkolatát. Az időszakos tendenciáknak megfelelően a fluor és a bróm közötti elektronegativitásban közbülső (F: 3,98, Cl: 3,16, Br: 2,96, I: 2,66), és kevésbé reaktív, mint a fluor, és reaktívabb, mint a bróm. Ez is gyengébb oxidálószer, mint a fluor, de erősebb, mint a bróm. Ezzel szemben a kloridion gyengébb redukálószer, mint a bromid, de erősebb, mint a fluorid. Atomsugárban közbenső a fluor és a bróm között, és ez számos atomi tulajdonságához vezet, hasonlóan folytatva a jódtól a brómig terjedő tendenciát, mint például az első ionizációs energia , elektron affinitás , az X 2 molekula disszociációjának entalpiája (X = Cl, Br, I), ion sugár és X – X kötéshossz. (A fluor rendellenes kis mérete miatt.)
Mind a négy stabil halogén intermolekuláris van der Waals vonzóerőt tapasztal, és erősségük növekszik az elektronok számával együtt az összes homonukleáris kétatomos halogénmolekula között. Így a klór olvadáspontja és forráspontja köztes a fluor és a bróm között: a klór -101,0 ° C -on olvad és -34,0 ° C -on forr. A halogének csoporton belüli növekvő molekulatömege miatt a klór fúziós és párolgási sűrűsége és hőjei ismét közbensőek a bróm és a fluor között, bár minden párolgási hőjük meglehetősen alacsony (nagy illékonysághoz vezet) kétatomos molekuláris szerkezetüknek köszönhetően. A halogének a csoport csökkenésével sötétednek: így míg a fluor halványsárga gáz, a klór kifejezetten sárga-zöld. Ez a tendencia azért fordul elő, mert a halogének által elnyelt látható fény hullámhossza nő a csoporton belül. Pontosabban, a színe a halogénatom, például klór-, eredmények a elektron átmenetet közötti legmagasabb elfoglalt antibonding π g molekulapálya és a legalacsonyabb megüresedett antibonding σ u molekulapálya. A szín alacsony hőmérsékleten elhalványul, így a szilárd klór –195 ° C -on szinte színtelen.
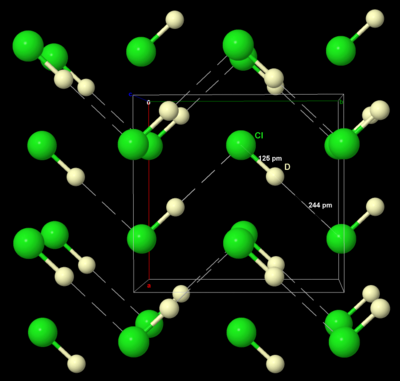
A szilárd brómhoz és a jódhoz hasonlóan a szilárd klór kristályosodik az ortorombikus kristályrendszerben , Cl 2 molekulák réteges rácsában . A Cl – Cl távolság 198 pm (közel a gázhalmazállapotú Cl – Cl távolsághoz 199 pm), és a Cl · ·· Cl távolság a molekulák között 332 pm egy rétegen belül és 382 pm a rétegek között (hasonlítsa össze a van der Waals sugarát klór, 180 pm). Ez a szerkezet azt jelenti, hogy a klór nagyon rossz villamos vezető, és vezetőképessége olyan alacsony, hogy gyakorlatilag mérhetetlen.
Izotópok
A klórnak két stabil izotópja van, 35 Cl és 37 Cl. Ez az egyetlen két természetes izotópja, amelyek mennyiségben fordulnak elő: 35 Cl a természetes klór 76% -át és 37 Cl a fennmaradó 24% -át. Mindkettőt csillagokban szintetizálják az oxigén- és a szilícium-égetési folyamatokban . Mindkét magspin 3/2 +, és így fel lehet használni a nukleáris mágneses rezonancia , bár a centrifugálás nagyságrendje nagyobb, mint 1/2 eredményeket a nem-gömb alakú nukleáris töltés eloszlását és így a rezonancia szélesedés eredményeként egy nem nulla nukleáris kvadrupól pillanatban és négylábú relaxációt eredményez. A többi klórizotóp mind radioaktív, felezési ideje túl rövid ahhoz, hogy a természetben eleinte előfordulhasson . Ezek közül a leggyakrabban használt laboratórium a 36 Cl ( t 1/2 = 3,0 × 10 5 y) és a 38 Cl ( t 1/2 = 37,2 perc), amelyek a természetes klór neutronaktiválásából származhatnak .
A legstabilabb klór radioizotóp 36 Cl. A 35 C -nál könnyebb izotópok elsődleges bomlási módja az elektron -elfogás a kén izotópjaihoz ; a 37 Cl -nál nehezebb izotópok béta -bomlása az argon izotópjaira ; és 36 Cl elkorhadhat bármelyik üzemmódban a stabil 36 S vagy 36 Ar. 36 Cl kis mennyiségben fordul elő a természetben, mint kozmogén nuklid , körülbelül (7–10) × 10–13 : 1 arányban, stabil klórizotópokkal: a légkörben keletkezik 36 Ar szétesésével a kozmikus sugár protonjaival való kölcsönhatás révén . A felső mérő a litoszféra, 36 Cl keletkezik elsősorban a termikus neutron aktiválása 35 Cl és spallációs a 39 K és a 40 Ca . A felszín alatti környezetben, müon Capture által 40 Ca egyre fontosabbá válik, mint úgy, hogy generálni 36 Cl.
Kémia és vegyületek
| x | XX | HX | BX 3 | AlX 3 | CX 4 |
|---|---|---|---|---|---|
| F | 159 | 574 | 645 | 582 | 456 |
| Cl | 243 | 428 | 444 | 427 | 327 |
| Br | 193 | 363 | 368 | 360 | 272 |
| én | 151 | 294 | 272 | 285 | 239 |
A klór köztes reaktivitás a fluor és a bróm között, és az egyik legreaktívabb elem. A klór gyengébb oxidálószer, mint a fluor, de erősebb, mint a bróm vagy a jód. Ez látható az X 2 /X - párok standard elektródpotenciáljaiból (F, +2,866 V; Cl, +1,395 V; Br, +1,087 V; I, +0,615 V; At, körülbelül +0,3 V). Ez a tendencia azonban nem jelenik meg a kötési energiákban, mivel a fluor kis méretének, alacsony polarizáltságának és a hipervalencia képtelenségének köszönhetően egyedülálló . Másik különbségként a klórnak jelentős kémiája van pozitív oxidációs állapotokban, míg a fluornak nincs. A klórozás gyakran magasabb oxidációs állapotokhoz vezet, mint a brómozás vagy a jódozás, de alacsonyabb oxidációs állapotokhoz, mint a fluorozás. A klór hajlamos reagálni az M – M, M – H vagy M – C kötéseket tartalmazó vegyületekkel, hogy M – Cl kötéseket hozzon létre.
Tekintettel arra, hogy E ° (1/2O 2 /H 2 O) = +1,229 V, ami kevesebb, mint +1,395 V, várható, hogy a klórnak képesnek kell lennie arra, hogy a vizet oxigénné és sósavvá oxidálja. Ennek a reakciónak a kinetikája azonban kedvezőtlen, és figyelembe kell venni a buborékok túlzott potenciális hatását is, így a vizes kloridoldatok elektrolízise klórgázt fejleszt, nem pedig oxigéngázt, ami nagyon hasznos a klór ipari előállításához.
Hidrogén klorid
A legegyszerűbb klórvegyület a hidrogén -klorid , a sósav, amely az iparban és a laboratóriumban is fontos vegyi anyag, mind gázként, mind vízben feloldva sósav formájában . Gyakran hidrogéngáz klórgázban való elégetésével vagy klórozó szénhidrogének melléktermékeként állítják elő . Egy másik megközelítés a nátrium-klorid koncentrált kénsavval történő kezelése sósav előállítása céljából, más néven "sós sütemény":
- NaCl + H 2 SO 4 NaHSO 4 + HCl
- NaCl + NaHSO 4 Na 2 SO 4 + HCI
A laboratóriumban hidrogén -klorid -gázt állíthatunk elő a sav koncentrált kénsavval történő szárításával. Deutérium-kloridot, DCI, lehet elő, benzoil-kloridot a nehézvíz (D 2 O).
Szobahőmérsékleten a hidrogén -klorid színtelen gáz, mint a hidrogén -fluoridon kívül minden hidrogén -halogenid , mivel a hidrogén nem képez erős hidrogénkötést a nagyobb elektronegatív klóratommal; gyenge hidrogénkötés azonban jelen van a szilárd kristályos hidrogén -kloridban alacsony hőmérsékleten, hasonlóan a hidrogén -fluorid szerkezetéhez, mielőtt a rendellenesség uralkodni kezd a hőmérséklet emelkedésével. A sósav erős sav (p K a = −7), mert a klórhoz kapcsolódó hidrogénkötések túl gyengék ahhoz, hogy gátolják a disszociációt. A HCI / H 2 O rendszer számos hidrátjai HCI · n H 2 O n = 1, 2, 3, 4, és 6. Beyond egy 1: 1 arányú HCI és H 2 O, a rendszer elválasztja teljesen két külön folyékony fázisok. A sósav azeotropot képez , forráspontja 108,58 ° C, 20,22 g sósav 100 g oldatban; így a sósav lepárlással nem koncentrálható ezen a ponton túl.
A hidrogén -fluoriddal ellentétben a vízmentes folyékony hidrogén -kloriddal nehéz oldószerként dolgozni, mert forráspontja alacsony, folyadéktartománya kicsi, dielektromos állandója alacsony, és nem szétválaszthatóan H 2 Cl + -vá és HCl -vé.-
2ionok - az utóbbiak mindenesetre sokkal kevésbé stabilak, mint a bifluorid -ionok ( HF-
2) a hidrogén és a klór közötti nagyon gyenge hidrogénkötés miatt, bár sói nagyon nagy és gyengén polarizáló kationokkal, például Cs + és NR+
4(R = Me , Et , Bu n ) még mindig izolálható. A vízmentes hidrogén -klorid gyenge oldószer, csak kis molekulájú vegyületeket, például nitrozil -kloridot és fenolt , vagy nagyon alacsony rácsenergiájú sókat , például tetraalkil -ammónium -halogenideket képes feloldani. Könnyen protonálja a magányos párokat vagy π kötéseket tartalmazó elektrofileket . A szolvolízis , a ligandumcsere- reakciók és az oxidációk jól jellemezhetők hidrogén-klorid oldatban:
- Ph 3 SnCl + HCl ⟶ Ph 2 SnCl 2 + PhH (szolvolízis)
- Ph 3 COH + 3 HCl ⟶ Ph
3C+
HCl-
2+ H 3 O + Cl - (szolvolízis) -
Nekem
4N+
HCl-
2+ BCl 3 ⟶ Én
4N+
BCl-
4 + HCl (ligandumcsere) - PCl 3 + Cl 2 + HCI ⟶ pentakloriddal+
4HCl-
2 (oxidáció)
Más bináris kloridok

A periódusos rendszer szinte minden eleme bináris kloridokat képez. A kivételek határozottan kisebbségben és szár minden esetben egy három oka van: extrém inertsége és vonakodnak, hogy részt vegyenek a kémiai reakciók (a nemesgázok , kivéve a xenon a nagyon instabil XeCl 2 és XeCl 4 ); szélsőséges nukleáris instabilitás hátráltató kémiai vizsgálata előtt bomlási és transzmutáció (sok a legnehezebb elemek túl bizmut ); és amelyek elektronegativitása nagyobb, mint a klóré ( oxigén és fluor ), így a kapott bináris vegyületek formailag nem kloridok, hanem inkább klór -oxidok vagy -fluoridok. Annak ellenére, hogy az NCl 3 nitrogénje negatív töltésű, a vegyületet általában nitrogén -trikloridnak nevezik .
Klórozása fémek Cl 2 általában vezet magasabb oxidációs állapotban, mint brómozzuk Br 2 , ha több oxidációs állapotok állnak rendelkezésre, mint például a MoCl 5 és MoBr 3 . A kloridokat úgy állíthatjuk elő, hogy egy elemet vagy annak oxidját, hidroxidját vagy karbonátját sósavval reagáltatjuk, majd enyhén magas hőmérsékleten dehidratáljuk, alacsony nyomáson vagy vízmentes hidrogén -klorid -gázzal kombinálva. Ezek a módszerek akkor működnek a legjobban, ha a kloridtermék stabil a hidrolízisre; ellenkező esetben a lehetőségek közé tartozik az elem magas hőmérsékletű oxidáló klórozása klórral vagy hidrogén-kloriddal, egy fém-oxid vagy más halogenid klórral, illékony fém-kloriddal, szén-tetrakloriddal vagy szerves kloriddal végzett magas hőmérsékletű klórozása . Például, cirkónium-dioxid reakcióba lép a klórral standard körülmények között, hogy készítsen cirkónium-tetrakloridot , és az urán-trioxid reagál hexaklórpropén alatt hevítve visszafolyatás így urán-tetraklorid . A második példa magában foglalja az oxidációs állapot csökkentését is , amelyet úgy is elérhetünk, hogy magasabb kloridot redukálunk hidrogénnel vagy fémmel redukálószerként. Ezt hőbomlással vagy aránytalanítással is el lehet érni az alábbiak szerint:
- EuCl 3 +1/2H 2 ⟶ EuCl 2 + HCl
- ReCl 5 Recl 3 + Cl 2
- AuCl 3 AuCl + Cl 2
A legtöbb klorid, az 1., 2. és 3. csoportba tartozó fémek, valamint a +2 és +3 oxidációs állapotú lantanidok és aktinidek , többnyire ionos, míg a nemfémek hajlamosak kovalens molekuláris kloridok képződésére, akárcsak a nagy oxidációjú fémek állapotok a +3 és a felette. Az ezüst -klorid vízben nagyon oldhatatlan, ezért gyakran használják a klór minőségi vizsgálatára.
Poliklórvegyületek
Bár a diklór erős oxidálószer, magas első ionizációs energiával, extrém körülmények között oxidálódhat a klór+
2kation. Ez nagyon instabil, és csak az elektronikus sávspektrum jellemzi, ha kisnyomású kisülési csőben gyártják. A sárga Cl+
3 A kation stabilabb, és a következőképpen állítható elő:
- Cl 2 + ClF + AsF 5 Cl+
3AsF-
6
Ezt a reakciót oxidáló oldószerben, arzén -pentafluoridban hajtjuk végre . A triklorid -anion, Cl-
3, szintén jellemezték; analóg a trijóddal .
Klór -fluoridok
A klór három fluoridja az interhalogén vegyületek részhalmazát képezi , amelyek mindegyike diamágneses . Ismert néhány kationos és anionos származék, például a ClF-
2, ClF-
4, ClF+
2, És Cl 2 F + . Néhány pszeudohalogenidek klórt is ismertek, mint például a cianogén-klorid (klór-cián, lineáris), klór -cianát (ClNCO), klór -tiocianát (ClSCN, ellentétben a oxigén megfelelője), és a klór -azid (összegképletre 3 ).
A klór-monofluorid (ClF) rendkívül hőstabil, és a kereskedelemben 500 grammos acél előadópalackokban értékesítik. Színtelen gáz, amely -155,6 ° C -on olvad és -100,1 ° C -on forr. Előállítható elemeinek iránya szerint 225 ° C -on, bár ezt követően el kell választani és tisztítani kell a klór -trifluoridtól és reaktánsaitól. Tulajdonságai többnyire közbensőek a klór és a fluor között. Sok fémmel és nemfémmel reagál szobahőmérsékleten vagy annál magasabb hőmérsékleten, fluorozva és klórt szabadítva fel. Ezenkívül klór -fluorozó szerként is működik, klórt és fluort adva többszörös kötésen keresztül vagy oxidáció útján: például megtámadja a szén -monoxidot, és karbonil -klór -fluoridot, COFCl -t képez. Hasonlóan reagál hexafluor -acetonnal (CF 3 ) 2 CO, kálium -fluorid katalizátorral, és heptafluor -izopropil -hipokloritot (CF 3 ) 2 CFOCl képződik; a nitrilek RCN termelni RCF 2 NCI 2 ; és a kén-oxidok SO 2 és SO 3 termelni ClSO 2 F és ClOSO 2 F volt. Exoterm módon és hevesen reagál az –OH és –NH csoportokat tartalmazó vegyületekkel, például vízzel:
- H 2 O + 2 ClF ⟶ 2 HF + Cl 2 O
A klór -trifluorid (ClF 3 ) illékony színtelen molekuláris folyadék, amely -76,3 ° C -on olvad és 11,8 ° C -on forr. Létrehozható gázhalmazállapotú klór vagy klór -monofluorid közvetlen fluorozásával 200-300 ° C -on. Ez az egyik legreaktívabb ismert kémiai vegyület, amely sok olyan anyaggal reagál, amelyek rendes körülmények között kémiailag semlegesnek minősülnek, mint például az azbeszt , beton és homok. Vízzel és a legtöbb szerves anyaggal érintkezve felrobban. Az általa felgyújtott elemek listája változatos: hidrogént , káliumot , foszfort , arzént , antimont , kénet , szelént , tellúrt , brómot , jódot és porított molibdént , volfrámot , ródiumot , irídiumot és vasat tartalmaz . A vízáteresztő fluoridréteget nátrium , magnézium , alumínium , cink , ón és ezüst képezi , amelyek melegítéssel eltávolíthatók. Hevítéskor még az olyan nemesfémeket is megtámadják , mint a palládium , a platina és az arany, és még a nemesgázok, a xenon és a radon sem menekülnek a fluorozás elől. A nikkeltartályokat általában azért használják, mert a fém nagy ellenállást mutat a klór -trifluorid támadásával szemben, ami egy nem reagáló nikkel -fluoridréteg kialakulásának köszönhető. A hidrazinnal hidrogén -fluoridot, nitrogént és klórgázokat képező reakcióját kísérleti rakétahajtóművekben használták, de problémái nagyrészt abból adódnak, hogy extrém hipergolicitása mérhető késedelem nélkül gyullad. Ma már többnyire a nukleáris üzemanyag-feldolgozó, oxidálódnak urán az urán-hexafluorid annak gazdagító és hogy elkülönüljön a plutónium . Fluoridion -donorként vagy -elfogadóként (Lewis -bázis vagy sav) működhet, bár nem szétválaszthatóan ClF -re+
2és ClF-
4 ionokat.
A klór-pentafluorid (ClF 5 ) készül egy nagyszabású közvetlen fluorozzuk klór- feleslegben fluorral gázt 350 ° C hőmérsékleten és 250 atm, és egy kis méretű reagáltatásával fém-kloridok fluorgázzal 100-300 ° C. -103 ° C -on olvad és -13,1 ° C -on forr. Nagyon erős fluorozó szer, bár még mindig nem olyan hatékony, mint a klór -trifluorid. Csak néhány specifikus sztöchiometrikus reakciót jellemeztek. Az arzén -pentafluorid és az antimon -pentafluorid [ClF 4 ] + [MF 6 ] - (M = As, Sb) formájú ion adduktokat képez , és a víz erőteljesen reagál az alábbiak szerint:
- 2 H 2 O + ClF 5 ⟶ 4 HF + FClO 2
A termék, a kloril -fluorid , az öt ismert klór -oxid -fluorid egyike. Ezek a termikusan instabil FClO -tól a kémiailag nem reagáló perkloril -fluoridig (FClO 3 ) terjednek , a másik három FClO 2 , F 3 ClO és F 3 ClO 2 . Mind az öt szerkezetileg és kémiailag is hasonlóan viselkedik, mint a klór -fluoridok, és Lewis -savakként vagy -bázisokként működhetnek azáltal, hogy fluoridionokat nyernek vagy veszítenek el, vagy nagyon erős oxidáló és fluorozó szerekként.
Klór -oxidok


A klór-oxidokat instabilitásuk ellenére jól tanulmányozták (mindegyik endoterm vegyület). Ezek azért fontosak, mert akkor keletkeznek, amikor a klór -fluorozott szénhidrogének fotolízisnek vetik alá a felső légkört, és az ózonréteg pusztulását okozzák. Egyik sem állítható elő az elemek közvetlen reakciójával.
A diklór-monoxid (Cl 2 O) barnássárga gáz (vörösesbarna, ha szilárd vagy folyékony), amelyet a klórgáz sárga higany (II) -oxiddal való reagáltatásával nyerhetünk . Nagyon jól oldódik vízben, amelyben egyensúlyban van a hipoklórsavval (HOCl), amelynek anhidridje. Így hatékony fehérítőszer, és leginkább hipokloritok készítésére használják . Hevítéskor, szikrázáskor vagy ammóniagáz jelenlétében felrobban.
A klór -dioxid (ClO 2 ) volt az első klór -oxid, amelyet 1811 -ben Humphry Davy fedezett fel . Ez egy sárga paramagnetikus gáz (mélyvörös, mint szilárd vagy folyadék), ahogyan az páratlan számú elektronból áll: a párosítatlan elektron delokalizációja miatt stabil a dimerizáció felé. -40 ° C felett robban, mint folyadék, és nyomás alatt, mint gáz, ezért alacsony koncentrációban kell előállítani a fa-pépes fehérítéshez és a vízkezeléshez. Általában a klorát redukálásával állítják elő az alábbiak szerint:
-
ClO-
3+ Cl - + 2 H + ⟶ ClO 2 +1/2Cl 2 + H 2 O
Termelése tehát szorosan összefügg a klór -oxosavak redoxreakcióival. Erős oxidálószer, kénnel , foszforral , foszfor -halogeniddel és kálium -bór -hidriddel reagál . Vízben exoterm módon oldódik, sötétzöld oldatokat képezve, amelyek nagyon lassan bomlanak a sötétben. A kristályos klatrát -hidrátok ClO 2 · n H 2 O ( n ≈ 6–10) alacsony hőmérsékleten elválnak. Fény jelenlétében azonban ezek az oldatok gyorsan fotodomponálódnak, és klór- és sósav -keveréket képeznek. Az egyes ClO 2 molekulák fotolízise ClO és ClOO gyököket eredményez, míg szobahőmérsékleten többnyire klór, oxigén és néhány ClO 3 és Cl 2 O 6 keletkezik. Cl 2 O 3 is keletkezik a szilárd anyag −78 ° C -on történő fotolízisekor: ez egy sötétbarna szilárd anyag, amely 0 ° C alatt felrobban. A ClO gyök a légköri ózonréteg kimerüléséhez vezet, ezért környezetvédelmi szempontból az alábbiak szerint fontos:
- Cl • + O 3 ⟶ ClO • + O 2
- ClO • + O • ⟶ Cl • + O 2
A klór -perklorát (ClOClO 3 ) halványsárga folyadék, amely kevésbé stabil, mint a ClO 2, és szobahőmérsékleten bomlik, és klórt, oxigént és diklór -hexoxidot (Cl 2 O 6 ) képez . A klór -perklorát a perklórsav (HOClO 3 ) klórszármazékának is tekinthető , hasonlóan más oxosavak termikusan instabil klórszármazékaihoz: példák közé tartozik a klór -nitrát (ClONO 2 , erőteljesen reakcióképes és robbanásveszélyes) és a klór -fluor -szulfát (ClOSO 2 F, stabilabb, de még nedvességérzékeny és nagyon reaktív). A diklór-hexoxid sötétvörös folyadék, amely lefagy, és szilárd anyagot képez, amely –180 ° C-on sárgul: általában klór-dioxid és oxigén reakciójával keletkezik. Annak ellenére, hogy megpróbálták racionalizálni, mint a ClO 3 dimerjét, inkább úgy reagál, mintha klór -perklorát, [ClO 2 ] + [ClO 4 ] - lenne , ami megerősítést nyert, hogy a szilárd anyag helyes szerkezete. Vízben hidrolizálva klór- és perklórsav -keveréket kap: a vízmentes hidrogén -fluoriddal analóg reakció nem megy végbe.
A diklór -heptoxid (Cl 2 O 7 ) a perklórsav (HClO 4 ) anhidridje, és könnyen előállítható belőle, ha -10 ° C -on foszforsavval dehidratáljuk, majd -35 ° C -on és 1 Hgmm -en desztilláljuk. Ez ütésérzékeny, színtelen olajos folyadék. Ez a klór -oxidok közül a legkevésbé reakcióképes, mivel egyedüliként nem gyújtja fel a szerves anyagokat szobahőmérsékleten. Feloldható vízben a perklórsav regenerálására, vagy vizes lúgokban a perklorátok regenerálására. Azonban termikusan robbanásszerűen lebomlik az egyik központi Cl – O kötés megszakításával, a ClO 3 és ClO 4 gyököket állítva elő, amelyek a köztes oxidokon keresztül azonnal az elemekre bomlanak.
Klór -oxosavak és oxianionok
| E ° (pár) |
a (H + ) = 1 (sav) |
E ° (pár) |
a (OH - ) = 1 (bázis) |
|---|---|---|---|
| Cl 2 /Cl - | +1,358 | Cl 2 /Cl - | +1,358 |
| HOCl/Cl - | +1,484 | ClO - /Cl - | +0,890 |
|
ClO- 3/Cl - |
+1,459 | ||
| HOCl/Cl 2 | +1,630 | ClO - /Cl 2 | +0,421 |
| HClO 2 /Cl 2 | +1,659 | ||
|
ClO- 3/Cl 2 |
+1,486 | ||
|
ClO- 4/Cl 2 |
+1,277 | ||
| HClO 2 /HOCl | +1,701 |
ClO- 2/ClO - |
+0,681 |
|
ClO- 3/ClO - |
+0,488 | ||
|
ClO- 3/HClO 2 |
+1,181 |
ClO- 3/ ClO- 2 |
+0,295 |
|
ClO- 4/ ClO- 3 |
+1,201 |
ClO- 4/ ClO- 3 |
+0,374 |
Klór formák négy oxoacids: hipoklórossav (HOCl), klórossav (HOClO), klórsav (HOClO 2 ), és a perklórsavat (HOClO 3 ). Amint a szomszédos táblázatban megadott redoxpotenciálokból látható, a klór sokkal stabilabb az aránytalanság szempontjából savas oldatokban, mint lúgos oldatokban:
Cl 2 + H 2 O ⇌ HOCl + H + + Cl - K ac = 4,2 × 10 −4 mol 2 l −2 Cl 2 + 2 OH - ⇌ OCl - + H 2 O + Cl - K alk = 7,5 × 10 15 mol −1 l
A hipoklorit -ionok tovább aránytalanul kloridot és klorátot (3 ClO - ⇌ 2 Cl - + ClO) termelnek-
3), de ez a reakció meglehetősen lassú 70 ° C alatti hőmérsékleten, a nagyon kedvező egyensúlyi 10 27 ellenére . A klorátionok maguk is aránytalanok lehetnek klorid és perklorát ( 4ClO) képződéséhez-
3⇌ Cl - + 3 ClO-
4), de ez még 100 ° C -on is nagyon lassú, annak ellenére, hogy nagyon kedvező 10 20 egyensúlyi állandó van . A klór -oxianionok reakciósebessége a klór oxidációs állapotának csökkenésével nő. A klór -oxi -savak erőssége nagyon gyorsan növekszik, ahogy a klór oxidációs állapota növekszik, mivel a töltés fokozódó delokalizációja a konjugált bázisok egyre több oxigénatomján keresztül történik.
A klór -oxosavak nagy része előállítható ezen aránytalansági reakciók felhasználásával. A hipoklórsav (HOCl) erősen reakcióképes és meglehetősen instabil; sóit leginkább fehérítő és sterilizáló képességeikhez használják. Nagyon erős oxidálószerek, oxigénatomot szállítanak a legtöbb szervetlen fajhoz. A klórsav (HOClO) még instabilabb, bomlás nélkül nem izolálható vagy koncentrálható: a vizes klór -dioxid bomlásából ismert. A nátrium -klorit azonban stabil só, és alkalmas textíliák fehérítésére és eltávolítására, oxidálószerként és klór -dioxid -forrásként. A klórsav (HOClO 2 ) egy erős sav, amely hideg vízben egészen stabil 30% -os koncentrációig, de felmelegedéskor klórt és klór -dioxidot eredményez. A csökkentett nyomáson történő elpárologtatás lehetővé teszi, hogy tovább koncentrálódjon körülbelül 40%-ra, de ezután perklórsavra, klórra, oxigénre, vízre és klór -dioxidra bomlik. Legfontosabb sója a nátrium -klorát , amelyet leginkább klór -dioxid előállítására használnak a papírmassza fehérítésére. A klorát kloriddá és oxigénné történő bomlása gyakori módja annak, hogy kis mennyiségben oxigént termeljenek a laboratóriumban. A klorid és a klorát az alábbiak szerint összekapcsolódva klórt képezhet:
-
ClO-
3+ 5 Cl - + 6 H + ⟶ 3 Cl 2 + 3 H 2 O
A perklorátok és a perklórsav (HOClO 3 ) a klór legstabilabb oxo-vegyületei, összhangban azzal a ténnyel, hogy a klórvegyületek akkor a legstabilabbak, ha a klóratom a lehető legalacsonyabb (-1) vagy legmagasabb (+7) oxidációs állapotban van . A perklórsav és a vizes perklorátok hevítéskor erőteljes és néha erőszakos oxidálószerek, éles ellentétben a többnyire inaktív természetükkel szobahőmérsékleten, mivel ezek a reakciók kinetikai okokból nagy aktiválási energiát okoznak. A perklorátokat nátrium -klorát elektrolitikus oxidálásával állítják elő, és a perklórsavat úgy állítják elő, hogy a vízmentes nátrium -perklorátot vagy bárium -perklorátot tömény sósavval reagáltatják, a kicsapódott kloridot kiszűrik, és a szűrletet desztillálják. A vízmentes perklórsav színtelen mozgó folyadék, amely érzékeny az ütésekre, és a legtöbb szerves vegyülettel felrobban , felgyújtja a hidrogén -jodidot és a tionil -kloridot , sőt oxidálja az ezüstöt és az aranyat. Bár ez egy gyenge ligandum, gyengébb a víznél, néhány vegyület összehangolt ClO -t tartalmaz-
4 ismertek.
Klór -szerves vegyületek

A többi szén -halogén kötéshez hasonlóan a C -Cl kötés egy gyakori funkcionális csoport, amely a szerves szerves kémia része . Formálisan az e funkciós csoporttal rendelkező vegyületek a klorid -anion szerves származékainak tekinthetők. A klór (3.16) és a szén (2.55) közötti elektronegativitás különbsége miatt a C – Cl kötésben lévő szén elektronhiányos és így elektrofil . A klórozás módosítja a fizikai tulajdonságait szénhidrogének több módon: klór-szénhidrogének jellemzően sűrűbb, mint a víz miatt a magasabb klór atomsúlya versus hidrogénatom, valamint alifás, tartalmazó szerves vannak alkilezőszerek , mert klorid egy kilépő csoport .
Az alkánok és aril- alkánok szabad gyökök körülményei között, UV-fénnyel klórozhatók . A klórozás mértékét azonban nehéz szabályozni: a reakció nem regioszelektív, és gyakran különböző izomerek keverékét eredményezi, különböző klórozási fokokkal, bár ez megengedhető, ha a termékek könnyen elválaszthatók. Az aril-kloridokat a Friedel-Crafts halogénezéssel , klór és Lewis-sav katalizátor alkalmazásával állíthatjuk elő. A haloform reakció klór és nátrium -hidroxid alkalmazásával alkil -halogenideket is képes előállítani metil -ketonokból és rokon vegyületekből. A klór növeli az alkének és alkinek többszörös kötéseit, így di- vagy tetra-klórvegyületeket kap. A klór költsége és reaktivitása miatt azonban a klór -szerves vegyületeket leggyakrabban hidrogén -klorid vagy klórozószerek, például foszfor -pentaklorid (PCl 5 ) vagy tionil -klorid (SOCl 2 ) alkalmazásával állítják elő . Az utolsó nagyon kényelmes a laboratóriumban, mert minden melléktermék gáz halmazállapotú, és nem kell desztillálni.
Számos klór -szerves vegyületet izoláltak természetes forrásokból, a baktériumoktól az emberekig. A klórozott szerves vegyületek a biomolekulák szinte minden osztályában megtalálhatók, beleértve az alkaloidokat , terpéneket , aminosavakat , flavonoidokat , szteroidokat és zsírsavakat . A szerves kloridok, beleértve a dioxinokat is , az erdőtüzek magas hőmérsékletű környezetében keletkeznek, és a szintetikus dioxinok előtti villámgyújtó tüzek megőrzött hamvaiban dioxinokat találtak. Ezenkívül számos egyszerű klórozott szénhidrogént, köztük diklór -metánt, kloroformot és szén -tetrakloridot izoláltak tengeri algákból. A klór -metán nagy része a környezetben természetes módon biológiai bomlás, erdőtüzek és vulkánok által keletkezik.
Néhány szerves klorid típus, bár nem mindegyik, jelentős toxicitást mutat a növényekre vagy állatokra, beleértve az embereket is. A dioxinok, amelyek szerves anyagok klór jelenlétében történő elégetésekor keletkeznek, és egyes rovarölő szerek, például a DDT , tartós szerves szennyező anyagok, amelyek veszélyt jelentenek a környezetbe kerülve. Például a DDT, amelyet a 20. század közepén széles körben használtak a rovarok elleni védekezésre, szintén felhalmozódik az élelmiszerláncokban, és bizonyos madárfajokban szaporodási problémákat (pl. Tojáshéj elvékonyodását) okoz. A C -Cl kötés homolitikus hasadásának köszönhetően klórgyököket hoz létre a felső légkörben, a klórozott fluorozott szénhidrogéneket megszüntették az ózonrétegnek okozott károk miatt.
Előfordulás és előállítás
A klór túlságosan reaktív ahhoz, hogy szabad elemként jelenjen meg a természetben, de klorid -sói formájában nagyon bőséges. Ez a huszonegyedik legelterjedtebb elem a földkéregben, és 126 milliomodrészét teszi ki, a kloridos ásványok, különösen a nátrium-klorid nagy lerakódásai révén , amelyeket elpárologtak a víztestekből. Mindezek sápadtak a tengervíz kloridion -tartalékaihoz képest: kisebb mennyiség nagyobb koncentrációban fordul elő egyes belvizekben és földalatti sós kutakban, például a Utah -i Nagy Sóstóban és az izraeli Holt -tengeren .
A klórgáz kis adagjait a laboratóriumban sósav és mangán -dioxid kombinálásával állítják elő , de a készenlét miatt ritkán merül fel az igény. Az iparban az elemi klórt általában vízben oldott nátrium -klorid elektrolízisével állítják elő. Ez a módszer, az 1892 -ben iparosodott klór -lúgos eljárás , ma a legtöbb ipari klórgázt biztosítja. A módszer a klórral együtt hidrogéngázt és nátrium -hidroxidot eredményez , amely a legértékesebb termék. A folyamat a következő kémiai egyenlet szerint megy végbe :
- 2 NaCl + 2 H 2 O → Cl 2 + H 2 + 2 NaOH
A kloridoldatok elektrolízise a következő egyenletek szerint történik:
- Katód: 2 H 2 O + 2 e - → H 2 + 2 OH -
- Anód: 2 Cl - → Cl 2 + 2 e -
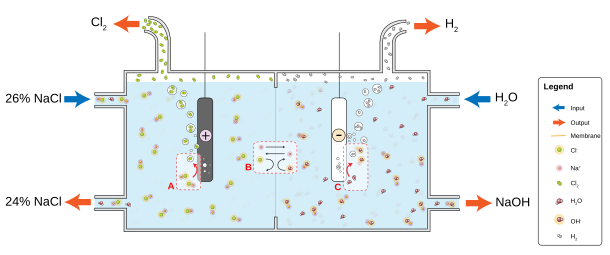
A membráncellás elektrolízis során azbeszt (vagy polimer-szál) membrán választja el a katódot és az anódot , megakadályozva, hogy az anódon keletkező klór újra keveredjen a nátrium-hidroxiddal és a katódon képződött hidrogénnel. A sóoldatot (sóoldatot) folyamatosan az anódrekeszbe táplálják, és a membránon keresztül a katódrekeszbe áramlik, ahol a lúgos lúg keletkezik, és a sóoldat részben kimerül. A membrános módszerek híg és enyhén szennyezett lúgokat termelnek, de nem terhelik őket a higany elvezetésének problémája, és energiahatékonyabbak.
Membrán sejt elektrolízis alkalmaz permeábilis membránnal , mint egy ioncserélő . A telített nátrium- (vagy kálium) -klorid -oldatot alacsonyabb koncentrációban hagyjuk át az anód rekeszen . Ez a módszer nagyon tiszta nátrium- (vagy kálium) -hidroxidot is termel, de hátránya, hogy nagy koncentrációban nagyon tiszta sóoldatot igényel.
A diakóniás eljárás során a klór -szerves klórvegyületek előállításából visszanyert hidrogén -kloridot klór formájában nyerik ki. A folyamat az oxigén felhasználásával történő oxidáción alapul:
- 4 HCl + O 2 → 2 Cl 2 + 2 H 2 O
A reakcióhoz katalizátor szükséges. Amint azt Deacon bevezette, a korai katalizátorok rézen alapultak. A kereskedelmi folyamatok, mint például a Mitsui MT-Chlorine Process, króm- és ruténium-alapú katalizátorokra váltottak át. Az előállított klór 450 g és 70 kg közötti méretű palackokban, valamint dobokban (865 kg), tartálykocsikban (15 tonna utakon, 27–90 tonna vasúton) és uszályokban (600–1200 tonna) kapható. .
Alkalmazások
A nátrium -klorid a leggyakoribb klórvegyület, és a vegyipar iránti kereslet fő klórforrása. Körülbelül 15 000 klórtartalmú vegyületet forgalmaznak a kereskedelemben, beleértve a különböző vegyületeket, például klórozott metánt , etánokat , vinil-kloridot , polivinil-kloridot (PVC), alumínium-trikloridot a katalízishez , magnézium- , titán- , cirkónium- és hafnium- kloridokat, amelyek a prekurzorok ezen elemek tiszta formájának előállítása.
Mennyiségileg az összes előállított elemi klór körülbelül 63% -át szerves vegyületek előállítására, 18% -át pedig szervetlen klórvegyületek gyártására használják fel. A kereskedelemben körülbelül 15 000 klórvegyületet használnak. A keletkező klór fennmaradó 19% -át fehérítőkre és fertőtlenítőszerekre használják fel. A termelési volumen szempontjából a legjelentősebb szerves vegyületek az 1,2-diklór-etán és a vinil-klorid , amelyek a PVC előállításának közbenső termékei . További különösen fontos szerves klór a metil -klorid , metilén -klorid , kloroform , vinilidén -klorid , triklór -etilén , perklór -etilén , allil -klorid , epiklór -hidrin , klór -benzol , diklór -benzolok és triklór -benzolok . A nagyobb szervetlen vegyületek közé HCI, Cl 2 O, HOCl, NaCIO 3 , klórozott izocianurátok, AICI 3 , SiCl 4 , SnCl 4 , PCl 3 , PCl 5 , POCI 3 , Ascl 3 , SbCl 3 , SbCl 5 , BiCl 3 , S 2 Cl 2 , SCI 2 , SOCI 2 , ClF 3 , ICI , ICI 3 , TiCl 3 , TiCl 4 , MoCl 5 , FeCl 3 , ZnCI 2 , és így tovább.
Fertőtlenítés, fertőtlenítés és fertőtlenítés
A rothadás elleni küzdelem
Franciaországban (akárcsak máshol) az állati beleket feldolgozták hangszer húrok, Goldbeater bőr és egyéb termékek előállítására. Ezt " bélgyárakban " ( boyauderies ) végezték , és ez kellemetlen és egészségtelen folyamat volt. Körülbelül 1820 -ban a Société d'encouragement pour l'industrie nationale díjat ajánlott fel egy kémiai vagy mechanikai módszer felfedezéséért, amellyel rothadás nélkül elválasztják az állati belek hashártyáját . A díjat Antoine-Germain Labarraque , egy 44 éves francia vegyész és gyógyszerész nyerte el , aki felfedezte, hogy Berthollet klórozott fehérítő oldatai (" Eau de Javel ") nemcsak az állati szövetek bomlásának szagát pusztítják el, hanem késleltette a bomlást.
Labarraque kutatásai eredményeként mész ( kalcium -hipoklorit ) és nátrium ( nátrium -hipoklorit ) kloridokat és hipokloritokat alkalmaztak a boyauderiesben. Ugyanezeket a vegyszereket hasznosnak találták a mellékhelyiségek , csatornák , piacok, vágóhidak , anatómiai színházak és hullaházak rutinszerű fertőtlenítésében és szagtalanításában . Sikeresek voltak kórházakban , lazaretekben , börtönökben , betegszobákban (szárazföldön és tengeren egyaránt), nagybányákban , istállókban , szarvasmarha-istállókban stb .; és jótékony hatásúak voltak a exhumációk , balzsamozások , járványos megbetegedések, láz és feketelábszarvasmarhák idején.
Fertőtlenítés
A Labarraque klórozott mész- és szódaoldatait 1828 óta szorgalmazzák a fertőzés (az úgynevezett „fertőző fertőzés”, amelyet feltételezhetően „ miazmák ” továbbítanak ) megelőzésére , valamint a meglévő sebek rothadásának kezelésére, beleértve a szeptikus sebeket is. 1828 -ban megjelent munkájában Labarraque azt javasolta az orvosoknak, hogy lélegezzenek be klórt, mossanak kezet klórozott mészben, és még a klórmészt is szórják a betegek ágyára „fertőző fertőzés” esetén. 1828 -ban a fertőzések fertőzése jól ismert volt, annak ellenére, hogy a mikrobák kórokozóját csak több mint fél évszázaddal később fedezték fel.
Az 1832-es párizsi kolerajárvány idején nagy mennyiségű úgynevezett mész - kloridot használtak a főváros fertőtlenítésére. Ez nem egyszerűen modern kalcium-klorid volt , hanem mészvízben (híg kalcium-hidroxid ) feloldott klórgáz , amely kalcium-hipokloritot (klórozott mész) képzett. Labarraque felfedezése segített eltüntetni a kórházakból és a boncolószobákból a bomlás szörnyű szagát, és ezzel hatékonyan szagtalanította a párizsi Latin negyedet . Sokan úgy gondolták, hogy ezek a "rothadó miazmák" a "fertőzés" és a "fertőzés" terjedését okozzák - mindkettőt a fertőzés csíraelmélete előtt használták. A mész -kloridot a szagok és a „rothadó anyagok” elpusztítására használták. Az egyik forrás azt állítja, hogy Dr. John Snow mész-kloridot használt a víz fertőtlenítésére a kolera-szennyezett kútból, amely a Broad Street-i szivattyút táplálta 1854-ben Londonban, bár három másik neves forrás, amelyek leírják a híres kolerajárványt, nem említik az esetet. Egy hivatkozás egyértelművé teszi, hogy a klorid mész használunk fertőtleníteni a belsőségeket és a mocsok az utcákon körülvevő Broad Street szivattyú - bevett gyakorlat a tizenkilencedik század közepén Angliában.
Semmelweis és antiszeptikus kísérletek
A Labarraque klór- és kémiai bázisoldatainak talán leghíresebb alkalmazása 1847-ben történt, amikor Semmelweis Ignaz klór-vizet (tiszta vízben feloldott klórral, amely olcsóbb volt, mint a klórozott mészoldatok) használta az osztrák orvosok kezének fertőtlenítésére, amit Semmelweis még mindig észrevett a bomlás bűzét hordta a boncoló helyiségekből a betegvizsgáló helyiségekbe. Semmelweis jóval a betegség csíraelmélete előtt azt feltételezte, hogy a „kadaverikus részecskék” a friss orvosi holttestekből származó bomlást közvetítik az élő betegek felé, és a jól ismert „Labarraque-oldatokat” használta az egyetlen ismert módszerként a bomlás és a szövetek szagának eltávolítására. bomlás (amit megállapított, hogy a szappan nem). A megoldások sokkal hatékonyabb antiszeptikumoknak bizonyultak, mint a szappan (Semmelweis is tisztában volt a nagyobb hatékonyságukkal, de nem az okával), és ez Semmelweis ünnepélyes sikerét eredményezte a gyermekágyi láz ("gyermekágyi láz") átadásának megállításában a szülési időszakban osztályokon bécsi Általános Kórház az Ausztriában 1847-ben.
Sokkal később, az első világháború idején, 1916 -ban Henry Drysdale Dakin (aki teljes mértékben elismeri Labarraque korábbi munkáját ezen a területen) kifejlesztett egy szabványosított és hígított módosítást Labarraque oldatának, amely hipokloritot (0,5%) és bórsavat tartalmazott savas stabilizátorként . . A Dakin -megoldásnak nevezett klórozott oldatokkal végzett seböblítési módszer lehetővé tette a nyílt sebek széles skálájának antiszeptikus kezelését, jóval a modern antibiotikumok kora előtt. Ennek a megoldásnak egy módosított változatát alkalmazzák a sebek öntözésében a modern időkben is, ahol hatékony marad a több antibiotikummal szemben rezisztens baktériumok ellen (lásd: Century Pharmaceuticals ).
Nyilvános higiénia
A klórozás első folyamatos alkalmazását az amerikai ivóvízben 1908 -ban telepítették a New Jersey -i Jersey City -ben. 1918 -ra az Egyesült Államok Pénzügyminisztériuma felszólította az ivóvizet klórral fertőtleníteni. A klór jelenleg fontos vegyi anyag a víztisztításban (például vízkezelő üzemekben), fertőtlenítőszerekben és fehérítőszerekben . Még a kis vízkészleteket is rutinszerűen klórozzák.
A klórt általában ( hipoklórsav formájában ) használják baktériumok és egyéb mikrobák elpusztítására az ivóvízellátásban és a nyilvános uszodákban. A legtöbb magán úszómedencék, klórt önmagában nem használják, hanem a nátrium-hipoklorit , kialakítva klór és nátrium-hidroxid , vagy szilárd tabletták klórozott izocianurátok. A klórnak az uszodákban való alkalmazásának hátránya, hogy a klór reagál az emberi haj és bőr fehérjeivel. A közhiedelemmel ellentétben az úszómedencékhez kapcsolódó jellegzetes "klór -aroma" nem maga az elemi klór eredménye, hanem a kloramin , egy kémiai vegyület, amely szabad oldott klór és szerves anyagokban lévő aminok reakciójával keletkezik. Vízben fertőtlenítőszerként a klór több mint háromszor olyan hatékony Escherichia coli ellen, mint a bróm , és több mint hatszor olyan hatékony, mint a jód . Egyre inkább a monoklóramint közvetlenül az ivóvízhez adják fertőtlenítés céljából - ezt a folyamatot klóraminálásnak nevezik .
Gyakran nem praktikus mérgező klórgázt tárolni és használni vízkezeléshez, ezért alternatív klór hozzáadási módszereket alkalmaznak. Ide tartoznak a hipoklorit oldatok, amelyek fokozatosan klórt engednek a vízbe, és olyan vegyületek, mint a nátrium-diklór-s-triazinetrion (dihidrát vagy vízmentes), néha „diklórnak” nevezik, és a triklór-s-triazinetrion , más néven „triklór” . Ezek a vegyületek szilárdak és stabilak, és por, szemcsés vagy tabletta formában is használhatók. Ha kis mennyiségben hozzáadják a medencevizekhez vagy az ipari vízrendszerekhez, a klóratomok hidrolizálódnak a molekula többi részéből, hipoklórsavat (HOCl) képezve, amely általános biocidként hat , elpusztítva a kórokozókat, mikroorganizmusokat, algákat stb.
Fegyverként használni
Első Világháború
A klórgázt, más néven bertolitot, Németország használta először fegyverként az I. világháborúban , 1915. április 22 -én, a második Ypres -i csatában . A katonák leírása szerint a bors és az ananász keverékének jellegzetes illata volt. Fémes íze is volt, és szúrta a torok hátsó részét és a mellkasát. A klór a vízzel reagálva a tüdő nyálkahártyájában sósavat képez , ami romboló hatású az élő szövetekre és potenciálisan halálos. Az emberi légzőrendszereket aktív szénnel vagy más szűrővel ellátott gázálarcokkal lehet megvédeni a klórgáztól , így a klórgáz sokkal kevésbé halálos, mint más vegyi fegyverek. A német tudós úttörője volt később, Nobel -díjas, Fritz Haber , a berlini Kaiser Wilhelm Intézet munkatársa, az IG Farben német vegyipari konglomerátummal együttműködve , amely módszereket fejlesztett ki a klórgáz elvezetésére egy megrögzött ellenséggel szemben. Az első használat után a konfliktus mindkét fele vegyi fegyverként klórt használt, de hamarosan felváltotta a halálosabb foszgén és mustárgáz .
Irak
Klórgáz is használták alatt iraki háború Anbar tartomány 2007-ben, a felkelők csomagolás targonca bombák a habarcs kagyló és a klór tankok. A támadások során két ember életét vesztette a robbanóanyagok miatt, és több mint 350 -en betegedtek meg. A legtöbb haláleset a robbanás ereje, nem pedig a klór hatása miatt következett be, mivel a robbanás következtében a mérgező gáz könnyen eloszlik és felhígul a légkörben. Egyes robbantásokban több mint száz civil került kórházba légzési nehézségek miatt. Az iraki hatóságok szigorították az elemi klór biztonságát, ami elengedhetetlen a lakosság biztonságos ivóvízellátásához.
2014. október 23 -án jelentették, hogy az Irak Iszlám Állam és a Levant klórgázt használt az iraki Duluiyah városában . A ruházat és a talajminták laboratóriumi elemzése megerősítette, hogy klórgázt használtak a kurd Peshmerga erők ellen a járművön keresztül szállított, robbanószerkezetes támadásban 2015. január 23-án a 47-es számú Kiske csomópontnál, Moszul közelében.
Szíria
A szíriai kormány használt klórt vegyi fegyver szállított hordó bombák és rakéták. 2016-ban az OPCW és az ENSZ közös vizsgálati mechanizmusa arra a következtetésre jutott, hogy a szíriai kormány három különálló támadásban klórt használt vegyi fegyverként. Az OPCW vizsgáló és azonosító csoportjának későbbi vizsgálatai arra a következtetésre jutottak, hogy a szír légierő volt felelős a klór támadásokért 2017 -ben és 2018 -ban.
Biológiai szerep
A klorid -anion alapvető tápanyag az anyagcserében. Klór szükséges a sósav előállításához a gyomorban és a sejtpumpa működésében. A fő táplálékforrás az asztali só vagy a nátrium -klorid. A túl alacsony vagy magas kloridkoncentráció a vérben az elektrolit -zavarok példái . Hipoklórémia (túl kevés kloridtartalmú) ritkán fordul elő egyéb rendellenességek hiányában. Néha hipoventilációval jár . Krónikus légúti acidózishoz társulhat . A hiperklorémia (túl sok klorid) általában nem okoz tüneteket. Amikor tünetek jelentkeznek, hajlamosak hasonlítani a hipernatrémia tüneteire (túl sok nátriumot tartalmaznak ). A vér kloridjának csökkenése agyi kiszáradáshoz vezet; tüneteit leggyakrabban a gyors rehidratáció okozza, ami agyi ödémát eredményez . A hiperklorémia befolyásolhatja az oxigénszállítást.
Veszélyek
| Veszélyek | |
|---|---|
| GHS piktogramok |
  
|
| GHS Jelszó | Veszély |
| H270 , H315 , H319 , H331 , H335 , H400 | |
| P220 , P244 , P261 , P304 , P340 , P312 , P403 , P233 , P410 , P403 | |
| NFPA 704 (tűzgyémánt) | |
A klór mérgező gáz, amely megtámadja a légzőrendszert, a szemet és a bőrt. Mivel sűrűbb, mint a levegő, hajlamos felhalmozódni a rosszul szellőző terek alján. A klórgáz erős oxidálószer, amely reakcióba léphet gyúlékony anyagokkal.
A klór mérőeszközökkel már 0,2 ppm (ppm) koncentrációban és 3 ppm szaggal kimutatható. Köhögés és hányás fordulhat elő 30 ppm -nél, és tüdőkárosodás 60 ppm -nél. Körülbelül 1000 ppm halálos lehet néhány mély gázlégzés után. Az IDLH (azonnal életveszélyes és egészségre veszélyes) koncentráció 10 ppm. Az alacsonyabb koncentráció belélegzése súlyosbíthatja a légzőrendszert, és a gáznak való kitettség irritálhatja a szemet. Ha a klórt 30 ppm -nél nagyobb koncentrációban lélegezzük be, az a vízzel reakcióba lép a tüdőben, sósavat (HCl) és hipoklórsavat (HClO) fejlesztve.
Ha a klórt vízzel való fertőtlenítés céljából meghatározott szinteken használják, a klór reakciója nem jelent komoly aggodalmat az emberi egészségre nézve. A vízben lévő egyéb anyagok fertőtlenítő melléktermékeket hozhatnak létre , amelyek negatív hatással lehetnek az emberi egészségre.
Az Egyesült Államokban a Munkahelyi Biztonsági és Egészségügyi Hatóság (OSHA) az elemi klór megengedett expozíciós határértékét 1 ppm -ben vagy 3 mg/m 3 -ben állapította meg . Az Országos Munkavédelmi és Egészségügyi Intézet az ajánlott expozíciós határértéket , 0,5 ppm -t jelölte ki 15 perc alatt.
Otthon balesetek történnek, amikor a hipoklorit fehérítő oldatok bizonyos savas lefolyó-tisztítószerekkel érintkeznek, és klórgázt termelnek. A hipoklorit fehérítő (népszerű mosodai adalékanyag) ammóniával (egy másik népszerű mosodai adalékanyag) kombinálva klóraminokat termel , a vegyi anyagok másik mérgező csoportját.
Klór okozta repedések szerkezeti anyagokban

A klórt széles körben használják a víz tisztítására, különösen az ivóvízellátásra és az uszodákban használt vízre. Az úszómedence mennyezetének több katasztrofális összeomlása történt a rozsdamentes acél felfüggesztő rudak klór okozta feszültségkorróziós repedése miatt . Egyes polimerek szintén érzékenyek a támadásokra, beleértve az acetálgyantát és a polibutént . Mindkét anyagot meleg- és hidegvizes háztartási vízvezetékekben használták, és a feszültségkorróziós repedések széles körű meghibásodásokat okoztak az USA -ban az 1980 -as és 1990 -es években.
Klór-vas tűz
A vas elem magas hőmérsékleten klórral kombinálódva erős exoterm reakcióban klór-vas tüzet hozhat létre . A klór-vas tüzek veszélyt jelentenek a vegyi feldolgozó üzemekben, ahol a klórgázt szállító csővezetékek nagy része acélból készül.
Lásd még
Hivatkozások
Megjegyzések
Bibliográfia
- Greenwood, Norman N .; Earnshaw, Alan (1997). Az elemek kémiája (2. kiadás). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
Külső linkek
- Klór a videók periódusos rendszerében (Nottinghami Egyetem)
- Toxikus Anyagok és Betegségek Nyilvántartó Ügynöksége : Klór
- Elektrolitikus termelés
- Klór előállítása és cseppfolyósítása
- Klórtermelés higany felhasználásával, környezetvédelmi szempontok és alternatívák
- Nemzeti szennyezőanyag -jegyzék - klór
- Nemzeti Munkavédelmi Intézet - Klóroldal
- Klórintézet - A klóripart képviselő kereskedelmi szövetség
- Chlorine Online- az Eurochlor-az európai klór-alkáli ipar üzleti szövetsége-internetes portálja
- . Encyclopædia Britannica . 6 (11. kiadás). 1911. 254–56.