HSPA8 - HSPA8
Heat shock 70 kDa-os fehérje 8 néven is ismert hősokk rokon 71 kD fehérje vagy Hsc70 vagy Hsp73 egy hősokk-fehérje , amely emberekben által kódolt HSPA8 gén 11-es kromoszóma tagjaként a hősokk-fehérje 70 család és a chaperon fehérje, megkönnyíti az újonnan lefordított és rosszul összehajtott fehérjék megfelelő összecsukását, valamint stabilizálja vagy lebontja a mutáns fehérjéket. Funkciói hozzájárulnak a biológiai folyamatokhoz, beleértve a jelátvitelt , az apoptózist , az autofágia , a fehérje homeosztázis, valamint a sejtek növekedését és differenciálódását . Azt társítva kiterjedt számú rák , neurodegeneratív betegségek , sejt öregedés , és az öregedés.
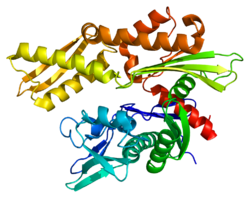
Szerkezet
Ez a gén egy 70 kDa hősokk fehérjét kódol, amely a hősokk fehérje 70 (Hsp70) család tagja. Hsp70 fehérjeként C-terminális fehérje szubsztrát-kötő domén és N-terminális ATP- kötő domén van benne. A szubsztrát-kötő domén két aldomainből, egy kétrétegű β-szendvics aldomainből (SBDβ) és egy α-spirális aldomainből (SBDα) áll, amelyeket az Lα, β hurok köti össze. Az SBDβ tartalmazza a peptidkötő zsebet, míg az SBDα fedőként szolgál a szubsztrátkötő hasadék lefedésére. Az ATP -kötő domén négy aldomainből áll, amelyeket egy központi ATP/ADP kötőzseb két lebenyre oszt. A két terminális domént egy konzervált régió köti össze, amelyet LL, 1 huroknak neveznek, ami kritikus az alloszterikus szabályozás szempontjából . A strukturálatlan régió a legvégén a C-terminális úgy véljük, hogy a dokkoló helyszínen co-chaperonok .
Funkció
A hősokk-fehérje 70 ( Hsp70 ) család egyaránt tartalmaz hővel indukálható és konstitutívan expresszált tagokat. Ez utóbbiakat hősokk rokon (Hsc) fehérjéknek nevezik. A hősokk 70 kDa fehérje 8, más néven Hsc70 a hősokk rokon alcsoportba tartozik. Ez a fehérje kötődik a születő polipeptidekhez, hogy megkönnyítse a megfelelő fehérjehajtást . A nem natív fehérjék megfelelő hajtogatása érdekében a Hsp70 chaperonok ATP-szabályozott módon lépnek kölcsönhatásba a fehérjék hidrofób peptidszegmenseivel. Bár a pontos mechanizmus még mindig tisztázatlan, legalább két alternatív hatásmód létezik: a kinetikus felosztás és a helyi kibontás. A kinetikus partícionálás során a Hsp70s ismételten kötődik és felszabadítja a szubsztrátokat olyan ciklusokban, amelyek fenntartják a szabad szubsztrát alacsony koncentrációját. Ez hatékonyan megakadályozza az aggregációt, miközben lehetővé teszi a szabad molekulák természetes állapotba hajtogatását. A helyi kibontakozás során a kötési és felszabadulási ciklusok lokalizált kibontakozást indukálnak a szubsztrátban, ami segít leküzdeni a natív állapotba hajtogatás kinetikai akadályait. Végső soron a fehérje -hajtogatásban betöltött szerepe hozzájárul a jelátvitelben, az apoptózisban, a fehérje -homeosztázisban, valamint a sejtek növekedésében és differenciálódásában betöltött funkciójához. Ismeretes, hogy a Hsc70 a citoplazmában és a lizoszómában lokalizálódik , ahol részt vesz a chaperone-mediált autofágiaban , elősegítve a szubsztrátproteinek kibontását és transzlokációját a membránon keresztül a lizoszomális lumenbe . Ezen az úton a Hsc70 hozzájárul a proapoptotikus BBC3/PUMA degradációjához is normál körülmények között, ezáltal citoprotekciót biztosítva.
A Hsc70 ezenkívül a sejtciklus -átmenet és a karcinogenezis pozitív szabályozója. Például a Hsc70 szabályozza a ciklin D1 nukleáris felhalmozódását, amely kulcsszereplő a G1 -S fázisú sejtciklus -átmenetben.
Egy másik funkciója a Hsc70 van, mint egy ATPáz a szétszerelését clathrin -bevonatú vezikulumok szállítás során a membrán komponensek a cellán keresztül. Úgy működik, auxilin eltávolítására clathrin bevonatos vezikulumok. Az idegsejtekben a szinaptojanin szintén fontos fehérje, amely részt vesz a vezikulák bevonatában. A Hsc70 a chaperone-mediált autofágia kulcsfontosságú alkotóeleme, ahol szelektivitást kölcsönöz a lizoszomális úton lebomló fehérjéknek.
Hsc70 vs Hsp70 összehasonlítás
A humán Hsc70 85% -ban azonos az emberi Hsp70 -tel (SDSC munkaasztal, blosom26 alapértelmezett elemzés). A tudományos közösség régóta feltételezi, hogy a Hsp70 és a Hsc70 hasonló sejtszereppel bír, de ez a feltételezés hiányosnak bizonyult. Míg a Hsc70 normál körülmények között chaperone funkciókat is végzett, ellentétben a kanonikus hősokk -fehérjékkel, a Hsc70 konstitutívan expresszálódik, és olyan funkciókat lát el, amelyek a normál sejtfolyamatokhoz kapcsolódnak, mint például a fehérje mindenütt való jelenléte és lebomlása.
Klinikai jelentőség
A Hsp70 tagfehérjék fontos apoptotikus alkotórészek. Normál embriológiai folyamatok vagy sejtkárosodás (például iszkémia-reperfúziós sérülés szívrohamok és agyvérzések során) vagy a rákos folyamatok és folyamatok során az apoptotikus sejt szerkezeti változásokon megy keresztül, beleértve a sejtzsugorodást, a plazmamembrán szivárgását, a nukleáris kondenzációt és a fragmentációt a DNS -ből és a magból . Ezt követi az apoptotikus testekre való töredezés, amelyeket a fagociták gyorsan eltávolítanak , ezáltal megakadályozva a gyulladásos választ. Ez a sejtpusztulás módja, amelyet jellegzetes morfológiai, biokémiai és molekuláris változások határoznak meg. Először "zsugorodási nekrózis" -ként írták le, majd ezt a kifejezést apoptózis váltotta fel, hogy hangsúlyozza a mitózissal szembeni szerepét a szövetkinetikában. Az apoptózis későbbi szakaszaiban az egész sejt fragmentálódik, és számos plazmamembránnal határolt apoptotikus testet képez, amelyek nukleáris és vagy citoplazmatikus elemeket tartalmaznak. A nekrózis ultrastrukturális megjelenése egészen más, a fő jellemzői a mitokondriális duzzanat, a plazmamembrán lebomlása és a sejtek szétesése. Az apoptózis számos fiziológiai és kóros folyamatban fordul elő . Fontos szerepet játszik az embrionális fejlődés során, mint programozott sejthalál, és számos normális involúciós folyamatot kísér, amelyekben mechanizmusként szolgál a "nem kívánt" sejtek eltávolítására.
A Hsp70 tagfehérjék, beleértve a Hsp72-t is, gátolják az apoptózist a kaszpázfüggő útvonalon és az apoptózist kiváltó ágensek, például tumor nekrózis faktor α (TNFα), staurosporin és doxorubicin ellen . Ez a szerep számos kóros folyamatban való részvételhez vezet, például az onkogenezisben, a neurodegenerációban és az öregedésben. Különösen, overexpressziója HSP72 összefüggésbe hozták a fejlődés bizonyos rákok, mint például a hepatocelluláris karcinóma , gyomorrák , vastagbélrák , mellrák , és a tüdőrák , ami a használatát, mint a prognosztikus markerként az ilyen rákok. A daganatsejtekben megnövekedett Hsp70 -szintek fokozhatják a rosszindulatú daganatokat és a terápiával szembeni ellenállást az onkofetális fehérjék és termékek komplexelésével, ezáltal stabilizálásával, és ezek intracelluláris helyekre történő szállításával, ezáltal elősegítve a tumorsejtek proliferációját. Ennek eredményeképpen a Hsp70 -ek daganatos vakcinázási stratégiái nagyon sikeresek voltak állatmodellekben, és klinikai vizsgálatokig terjedtek. Az egyik kezelés, a Hsp72/AFP rekombinált vakcina, erős védő immunitást váltott ki az AFP-t expresszáló daganatok ellen egérkísérletekben. Ezért a vakcina ígéretes a májsejtes karcinóma kezelésére. Alternatív megoldásként a Hsp70 túlzott expressziója mérsékelheti az iszkémia - a szívizom reperfúziója , valamint a neurodegeneratív betegségek, például az Alzheimer -kór , a Parkinson -kór , a Huntington -kór és a spinocerebelláris ataxia okozta károkat , valamint az öregedést és a sejtek öregedését, amint azt a centenáriánusok is megfigyelték. hősokk kihívás. A Hsc70 különösen védő szerepet játszik a fent említett betegségekben, valamint más neuropszichiátriai rendellenességekben, például a skizofréniában. Védő szerepét tovább hangsúlyozta egy tanulmány, amely a HSPA8-at más HSP70 fehérjék mellett azonosította a szélesebb chaperome interakta maghálózatában. betegségben szenvedő betegek.
Interakciók
A Hsc70 chaperone komplexet képez azáltal, hogy kölcsönhatásba lép a 40 kDa hősokk fehérjével ( Hsp40 ), a 90 kDa hősokk fehérjével ( Hsp90 ), a hsc70 kölcsönhatásba lépő fehérjével ( HIP ), a hsc70-hsp90 szervező fehérjével ( HOP ) és a Bcl2-asszociált athanogén 1 fehérje ( BAG1 ).
A HSPA8 kölcsönhatásba lépett a következőkkel is:
Hivatkozások
További irodalom
- Kiang JG (2004. december). "Indukálható hősokk fehérje 70 kD és indukálható nitrogén-monoxid szintáz vérzés/újraélesztés okozta sérülés esetén" . Sejtkutatás . 14 (6): 450–9. doi : 10.1038/sj.cr.7290247 . PMID 15625011 . S2CID 21654486 .
- Rasmussen HH, van Damme J, Puype M, Gesser B, Celis JE, Vandekerckhove J (1992. december). "145 fehérje mikroszekvenciái rögzítve a normál emberi epidermális keratinociták kétdimenziós gélfehérje adatbázisában". Elektroforézis . 13 (12): 960–9. doi : 10.1002/elps.11501301199 . PMID 1286667 . S2CID 41855774 .
- Hattori H, Liu YC, Tohnai I, Ueda M, Kaneda T, Kobayashi T, Tanabe K, Ohtsuka K (1992. február). "Stressz által indukálható 40 kDa fehérje sejten belüli lokalizációja és részleges aminosavszekvenciája HeLa sejtekben". A sejt szerkezete és működése . 17. (1): 77–86. doi : 10.1247/csf.17.77 . PMID 1586970 .
- DeLuca-Flaherty C, McKay DB, Parham P, Hill BL (1990. szept.). "A bevonat nélküli fehérje (hsc70) megköti a klatrin könnyű lánc LCa konformációilag labil doménjét, hogy stimulálja az ATP hidrolízist". Cell . 62. (5): 875–87. doi : 10.1016/0092-8674 (90) 90263-E . PMID 1975516 . S2CID 9501568 .
- Lim MY, Davis N, Zhang JY, Bose HR (1990. március). "A v-rel onkogén termék sejtfehérjékkel komplex, beleértve a proto-onkogén termékét és a 70-es hősokk fehérjét". Virológia . 175 (1): 149–60. doi : 10.1016/0042-6822 (90) 90195-W . PMID 2155506 .
- Welch WJ, Mizzen LA (1988. ápr.). "A hőtoleráns sejt jellemzése. II. Hatások a hősokk-fehérje 70, a köztes szálak és a kis nukleáris ribonukleoproteinkomplexek intracelluláris eloszlására" . The Journal of Cell Biology . 106. (4): 1117–30. doi : 10.1083/jcb.106.4.1117 . PMC 2115010 . PMID 2966179 .
- Dworniczak B, Mirault ME (1987. július). "71 kd hősokk" rokon "fehérjét kódoló emberi gén szerkezete és expressziója . Nukleinsavak kutatása . 15 (13): 5181–97. doi : 10.1093/nar/15.13.5181 . PMC 305955 . PMID 3037489 .
- Rensing SA, Maier UG (1994. július). "A stressz-70 fehérjecsalád filogenetikai elemzése". Journal of Molecular Evolution . 39 (1): 80–6. doi : 10.1007/BF00178252 . PMID 7545947 . S2CID 37505045 .
- Lain B, Iriarte A, Mattingly JR, Moreno JI, Martinez-Carrion M (1995. október). "A hsp70 -hez kötődésért felelős mitokondriális aszpartát -aminotranszferáz prekurzorának szerkezeti jellemzői" . The Journal of Biological Chemistry . 270 (42): 24732–9. doi : 10.1074/jbc.270.42.24732 . PMID 7559589 .
- Benaroudj N, Batelier G, Triniolles F, Ladjimi MM (1995. november). "A HSC70 molekuláris chaperon önálló asszociációja". Biokémia . 34 (46): 15282–90. doi : 10.1021/bi00046a037 . PMID 7578144 .
- Nunes SL, Calderwood SK (1995. augusztus). "A hősokk-1-es faktor és a hősokk-rokon 70-es fehérje nagy molekulatömegű komplexekben társul az NIH-3T3 sejtek citoplazmájában". Biokémiai és biofizikai kutatási kommunikáció . 213. (1): 1–6. doi : 10.1006/bbrc.1995.2090 . PMID 7639722 .
- Inoue A, Torigoe T, Sogahata K, Kamiguchi K, Takahashi S, Sawada Y, Saijo M, Taya Y, Ishii S, Sato N, Kikuchi K (1995. szept.). "A 70 kDa hősokk rokon fehérje közvetlenül kölcsönhatásba lép a pRb retinoblasztóma géntermék N-terminális régiójával. A pRb-közvetítő fehérje kölcsönhatás új régiójának azonosítása" . The Journal of Biological Chemistry . 270 (38): 22571–6. doi : 10.1074/jbc.270.38.22571 . PMID 7673249 .
- Abe T, Konishi T, Hirano T, Kasai H, Shimizu K, Kashimura M, Higashi K (1995. január). "Lehetséges összefüggés a hidrogén -peroxid által kiváltott DNS -károsodás és a hősokk 70 fehérje sejtmagba történő transzlokációja között". Biokémiai és biofizikai kutatási kommunikáció . 206 (2): 548–55. doi : 10.1006/bbrc.1995.1078 . PMID 7826371 .
- Furlini G, Vignoli M, Re MC, Gibellini D, Ramazzotti E, Zauli G, La Placa M (1994. január). "Az 1. típusú humán immunhiányos vírus kölcsönhatása a CD4+ sejtek membránjával 70K hősokk fehérje szintézisét és nukleáris transzlokációját indukálja" . The Journal of General Virology . 75 (1): 193–9. doi : 10.1099/0022-1317-75-1-193 . PMID 7906708 .
- Maruyama K, Sugano S (1994. január). "Oligo-capping: egyszerű módszer az eukarióta mRNS-ek sapkaszerkezetének oligoribonukleotidokkal történő helyettesítésére". Gene . 138 (1–2): 171–4. doi : 10.1016/0378-1119 (94) 90802-8 . PMID 8125298 .
- Tavaria M, Gabriele T, Anderson RL, Mirault ME, Baker E, Sutherland G, Kola I (1995. szept.). "Az emberi hősokk rokon fehérjét, a HSP73 -at kódoló gén lokalizálása a 11. kromoszómához". Genomika . 29. (1): 266–8. doi : 10.1006/geno.1995.1242 . PMID 8530083 .
- Gao B, Eisenberg E, Greene L (1996. július). "A konstitutív 70 kDa hősokk fehérje polimerizáció hatása a fehérje szubsztráttal való kölcsönhatására" . The Journal of Biological Chemistry . 271 (28): 16792-7. doi : 10.1074/jbc.271.28.16792 . PMID 8663341 .
- Egerton M, Moritz RL, Druker B, Kelso A, Simpson RJ (1996. július). "A 70 kD-os hősokk rokon fehérje (Hsc70) és az alfa-aktinin-1 azonosítása új foszfotirozint tartalmazó fehérjékként a T-limfocitákban". Biokémiai és biofizikai kutatási kommunikáció . 224 (3): 666–74. doi : 10.1006/bbrc.1996.1082 . PMID 8713105 .
- Lamian V, Small GM, Feldherr CM (1996. október). "Bizonyíték a Hsc70 nukleáris importjának új mechanizmusának létezésére". Kísérleti sejtkutatás . 228 (1): 84–91. doi : 10.1006/excr.1996.0302 . PMID 8892974 .
- Hansen S, Midgley CA, Lane DP, Freeman BC, Morimoto RI, Hupp TR (1996. november). "Két különböző COOH-terminális domén módosítása szükséges az egér p53 bakteriális Hsp70 általi aktiválásához" . The Journal of Biological Chemistry . 271 (48): 30922–8. doi : 10.1074/jbc.271.48.30922 . PMID 8940078 .
Külső linkek
- Hsc70 + Protein az amerikai National Library of Medicine orvosi tárgyszórendszere (mm)
- A PDBe-KB áttekintést nyújt a humán hősokk rokon 71 kDa-os fehérje előzetes adatlapjában rendelkezésre álló összes strukturális információról