Feketeállomány - Substantia nigra
| Feketeállomány | |
|---|---|
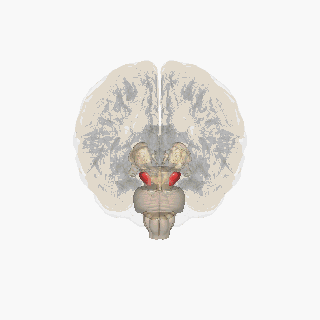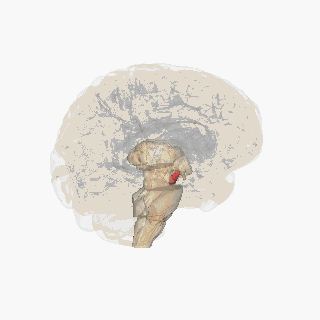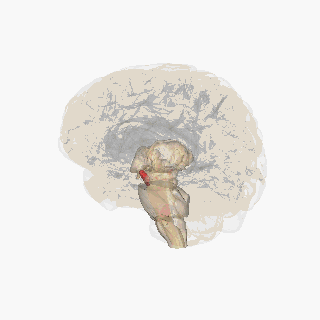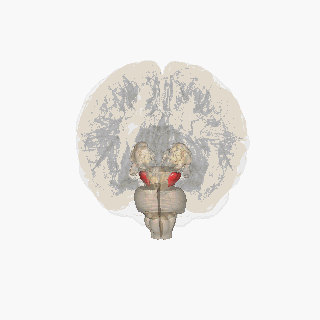 A Substantia nigra pirossal kiemelve.
| |
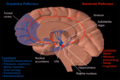
 A Substantia nigra -t mutató metszés a kiváló colliculuson keresztül .
| |
| Részletek | |
| Része | Középagy , bazális ganglionok |
| Azonosítók | |
| latin | Feketeállomány |
| Háló | D013378 |
| NeuroNames | 536 |
| NeuroLex azonosító | birnlex_789 |
| TA98 | A14.1.06.111 |
| TA2 | 5881 |
| FMA | 67947 |
| A neuroanatómia anatómiai terminusai | |
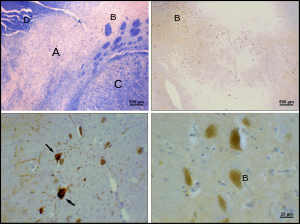
A substantia nigra ( SN ) a középagyban elhelyezkedő bazális ganglion szerkezet , amely fontos szerepet játszik a jutalomban és a mozgásban . Szubsztancia nigra van latin a „fekete anyag”, amely tükrözi azt, hogy részei a substantia nigra sötétebb, mint a szomszédos területek miatt magas a neuromelanin a dopaminerg neuronok . A Parkinson -kórra jellemző a dopaminerg neuronok elvesztése a substantia nigra pars compacta -ban .
Annak ellenére, hogy a substantia nigra folyamatos sávként jelenik meg az agyszakaszokban , az anatómiai vizsgálatok azt találták, hogy valójában két részből áll, amelyek nagyon különböző kapcsolatokkal és funkciókkal rendelkeznek: a pars compacta (SNpc) és a pars reticulata (SNpr). A pars compacta főként a bazális ganglionok körének kivetüléseként szolgál, ellátva a striatumot dopaminnal. A pars reticulata jeleket közvetít a bazális ganglionokból számos más agyi struktúrába.
Szerkezet
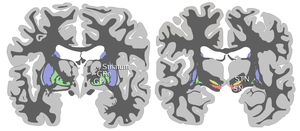
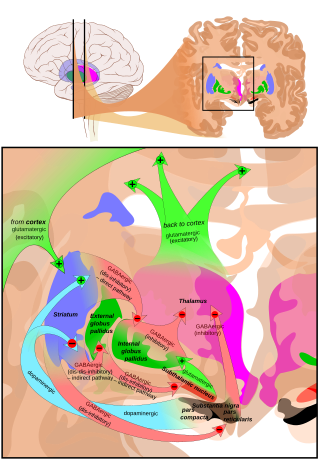
A substantia nigra négy másik maggal együtt a bazális ganglionok része . Ez a középső agy legnagyobb magja, amely az agytörzshez képest hátul fekszik . Az embereknek két anyacsigája van, egy a középvonal mindkét oldalán.
Az SN két részre oszlik: a pars reticulata (SNpr) és a pars compacta (SNpc), amely a pars reticulata felé mediálisan fekszik. Néha megemlítenek egy harmadik régiót, a pars lateralis -t, bár általában a pars reticulata részeként sorolják be. Az (SNpr) és a belső globus pallidus (GPi) a belső kapszulával van elválasztva .
Pars reticulata
A pars reticulata erős szerkezeti és funkcionális hasonlóságot mutat a globus pallidus belső részével. A kettőt néha ugyanazon szerkezet részének tekintik, amelyeket a belső kapszula fehérállománya választ el egymástól. A globus pallidushoz hasonlóan a pars reticulata neuronjai is főként GABAerg eredetűek .
Afferens kapcsolatok
Az SNpr fő bemenete a striatumból származik . Két útvonalon halad keresztül, amelyeket közvetlen és közvetett utaknak neveznek . A közvetlen útvonal a striatum közepes tüskés sejtjeiből származó axonokból áll, amelyek közvetlenül a pars reticulata -ra vetülnek. Az indirekt útvonal három láncszemből áll: vetület a striatális közepes tüskés sejtekből a globus pallidus külső részébe ; egy GABAerg vetület a globus pallidus -tól a szub -allamikus mag felé , és egy glutamatergikus vetület a szub -allamikus magból a pars reticulata -ba. Így a striatális aktivitás a közvetlen útvonalon gátló hatást fejt ki az (SNpr) idegsejtjeire, de az indirekt úton izgató hatást fejt ki. A közvetlen és közvetett útvonalak a striatális közepes tüskés sejtek különböző alcsoportjaiból származnak: szorosan keverednek egymással, de különböző típusú dopamin receptorokat fejeznek ki, valamint egyéb neurokémiai különbségeket mutatnak.
Hatékony kapcsolatok
Jelentős vetületek fordulnak elő a thalamus (ventrális laterális és ventralis elülső magok), superior colliculus és más caudalis magok számára a pars reticulata -ból (a nigrothalamicus útból), amelyek GABA -t használnak neurotranszmitterként. Ezenkívül ezek az idegsejtek legfeljebb öt biztosítékot képeznek, amelyek a pars compacta és a pars reticulata területén is elágaznak, valószínűleg módosítva a pars compacta dopaminerg aktivitását.
Funkció
A substantia nigra fontos szerepet játszik az agyműködésben, különösen a szemmozgásban , a motoros tervezésben , a jutalomkeresésben , a tanulásban és a függőségben . A substantia nigra számos hatása a striatumon keresztül közvetül . A nigrális dopaminerg bemenet a striatumba a nigrostriatális úton keresztül szorosan összefügg a striatum funkciójával. A striatum és a substantia nigra közötti együttes függőség így látható: ha a substantia nigra elektromos stimulációra kerül, nem történik mozgás; a Parkinson -kór miatti nigrális degeneráció tünetei azonban megindító példái a substantia nigra mozgásra gyakorolt hatásának. A striatum által közvetített funkciók mellett a substantia nigra a GABAerg gátlás fő forrásaként is szolgál a különböző agyi célpontok számára.
Pars reticulata
A substantia nigra pars reticulata fontos feldolgozó központ a bazális ganglionokban. A pars reticulata GABAerg neuronjai továbbítják a bazális ganglionok végső feldolgozott jeleit a thalamus és a superior colliculus felé . Ezenkívül a pars reticulata gátolja a dopaminerg aktivitást is a pars compacta -ban axon -biztosítékok révén, bár ezeknek a kapcsolatoknak a funkcionális szerveződése továbbra sem világos.
A GABAerg neuronok pars reticulata spontán tűz akciós potenciálok . Patkányokban az akciós potenciálok gyakorisága nagyjából 25 Hz. Ezeknek a spontán akciós potenciáloknak az a célja, hogy gátolják a bazális ganglionok célpontjait, és a gátlás csökkenése a mozgással jár. A szubhalamikus mag gerjesztő bemenetet ad, amely modulálja ezen spontán akciós potenciálok tüzelési sebességét. Mindazonáltal a szub -allamikus mag sérülése csak 20% -kal csökkenti a pars reticulata tüzelési sebességét, ami arra utal, hogy a pars reticulata akciópotenciáljainak generálása nagyrészt autonóm, ezt példázza a pars reticulata szerepe a szakadikus szemmozgásban . A GABAerg neuronok egy csoportja a pars reticulata -tól a felső colliculusig terjed, és magas szintű gátló aktivitást mutat. A caudate magtól a superior colliculus -ig terjedő vetületek szintén modulálják a szakadikus szemmozgást. A pars reticulata tüzelés megváltozott mintái, például az egy tüske vagy a tüzelés a Parkinson-kórban és az epilepsziában fordulnak elő .
Pars compacta
A pars compacta legkiemelkedőbb funkciója a motorvezérlés , bár a substantia nigra szerepe a motorvezérlésben közvetett; a substantia nigra elektromos stimulációja nem eredményez mozgást, mivel a striatum közvetíti a mozgás nigrális hatását. A pars compacta gerjesztő bemenetet küld a striatumba a D1 útvonalon keresztül, amely gerjeszti és aktiválja a striatumot, ennek eredményeként a GABA felszabadul a globus pallidusra, hogy gátolja a thalamikus magra gyakorolt gátló hatását. Ennek hatására a thalamocorticalis útvonalak izgatottak, és motoros neuronjeleket továbbítanak az agykéregbe, hogy lehetővé tegyék a mozgást, ami a Parkinson -kórban hiányzik. A pars compacta neuronok hiánya azonban nagy hatással van a mozgásra, amint azt a Parkinson -kór tünetei is bizonyítják. A pars compacta motoros szerepe magában foglalhatja a finom motoros vezérlést, amint azt az adott régióban sérült állatmodellek is megerősítették.
A pars compacta erősen részt vesz az ingerekre adott tanult válaszokban. A főemlősöknél a dopaminerg neuron aktivitás növekszik a nigrostriatális pályán, amikor új inger kerül bemutatásra. A dopaminerg aktivitás csökken az ismételt ingerbemutatással. A viselkedési szempontból jelentős ingerbemutatás (azaz jutalom) azonban továbbra is aktiválja a dopaminerg neuronokat a substantia nigra pars compacta -ban. Dopaminerg vetületek a ventrális tegmentális területről (a "középső agy" vagy a mesencephalon alsó része) a prefrontális kéregbe (mezokortikális útvonal) és a nucleus accumbens -be (mezolimbikus útvonal - "meso" utalva a "a mesencephalonból" ... konkrétan a ventrális tegmentális terület ) a jutalom, az öröm és az addiktív viselkedés. A pars compacta szintén fontos a térbeli tanulásban, a környezetre és a térben való tartózkodásra vonatkozó megfigyeléseken. A pars compacta elváltozásai tanulási zavarokhoz vezetnek az azonos mozdulatok ismétlésében, és egyes tanulmányok rámutatnak arra, hogy részt vesz egy dorsalis striatalis-függő, válaszon alapuló memóriarendszerben, amely viszonylag független a hippokampusztól , és amelyről hagyományosan úgy vélik, hogy térbeli vagy epizodikus -mint a memória funkciók.
A pars compacta szintén szerepet játszik az időbeli feldolgozásban, és aktiválódik az idő reprodukciója során. A pars compacta elváltozásai időbeli hiányokhoz vezetnek. Az utóbbi időben a pars compacta gyanúja szerint szabályozza az alvás-ébrenlét ciklust, ami összhangban van olyan tünetekkel, mint az álmatlanság és a REM alvászavarok , amelyeket a Parkinson-kórban szenvedő betegek jelentettek . Ennek ellenére a részleges dopaminhiány, amely nem befolyásolja a motoros vezérlést, zavart okozhat az alvás-ébrenlét ciklusban, különösen a REM-szerű idegi aktivitás mintáiban ébren, különösen a hippocampusban .
Klinikai jelentőség
A substantia nigra kulcsfontosságú számos betegség és szindróma, köztük a parkinsonizmus és a Parkinson -kór kialakulásában . Létezik egy tanulmány, amely kimutatja, hogy a nagyfrekvenciás stimuláció bal anyacsigába történő átadása átmeneti akut depressziós tüneteket válthat ki.
Parkinson kór
A Parkinson -kór neurodegeneratív betegség , amelyet részben az SNpc dopaminerg idegsejtjeinek elhalása jellemez. A Parkinson -kór fő tünetei közé tartozik a remegés , akinesia , bradykinesia és merevség. További tünetek a testtartás zavarai, fáradtság , alvászavarok és depressziós hangulat .
Az SNpc -ben lévő dopaminerg neuronok halálának oka ismeretlen. Mindazonáltal bizonyos szerepet játszottak a pars compacta dopaminerg idegsejtjeinek egyedi érzékenységében. Egyrészt a dopaminerg neuronok rendellenességeket mutatnak az 1. mitokondriális komplexben , ami az alfa-szinuklein aggregációját okozza ; ez a fehérjék rendellenes kezeléséhez és a neuronok halálához vezethet. Másodszor, a pars compacta dopaminerg neuronjai kevesebb kalbindint tartalmaznak, mint más dopaminerg neuronok. A calbindin egy fehérje, amely részt vesz a kalciumionok szállításában a sejteken belül, és a sejtekben lévő felesleges kalcium mérgező. A calbindin elmélet megmagyarázná a Parkinson -kór magas citotoxicitását a substantia nigra -ban a ventrális tegmentális területhez képest. A neuronális halál okától függetlenül a pars compacta plaszticitása nagyon robusztus; A Parkinson -kór tünetei csak akkor jelentkeznek, ha a pars compacta dopaminerg neuronok 50-80% -a meghalt. E plaszticitás nagy része neurokémiai szinten jelentkezik; a dopamin transzportrendszerek lelassulnak, így a dopamin hosszabb ideig maradhat a striatum kémiai szinapszisaiban.
Menke, Jbabdi, Miller, Matthews és Zari (2010) diffúziós tenzoros képalkotást, valamint T1 -leképezést alkalmaztak az SNpc és az SNpr térfogati különbségeinek felmérésére a Parkinson -kóros résztvevőkben az egészséges egyénekhez képest. Ezek a kutatók azt találták, hogy a Parkinson -kórban szenvedő betegeknek következetesen kisebb volt a substantia nigra, különösen az SNpr -ben. Mivel az SNpr a hátsó thalamushoz, a ventrális thalamushoz és különösen a motoros kéreghez kapcsolódik, és mivel a Parkinson -kórban szenvedő résztvevők kisebb SNp -értékkel rendelkeznek (Menke, Jbabdi, Miller, Matthews és Zari, 2010), ennek a régiónak a kis térfogata felelős lehet a Parkinson -kórban szenvedő betegek motoros károsodásáért. Ez a kis térfogat felelős lehet a gyengébb és/vagy kevésbé szabályozott motoros mozgásokért, ami a Parkinson -kórban szenvedők által gyakran tapasztalt remegéshez vezethet.
Az oxidatív stressz és az SNpc oxidatív károsodása valószínűleg kulcsfontosságú hajtóerő a Parkinson -kór etiológiájában az egyének életkorával. Az oxidatív stressz okozta DNS-károsodások az alfa-szinuklein által modulált folyamatokkal helyrehozhatók . Az alfa -szinukleint a substantia nigra fejezi ki, de úgy tűnik, hogy a DNS -javító funkciója sérült a Lewy -testbe való befogadást hordozó idegsejtekben . Ez a veszteség sejthalált okozhat.
Skizofrénia
A megnövekedett dopamin szint már régóta szerepet játszik a skizofrénia kialakulásában . Azonban a mai napig sok vita folyik a skizofrénia dopamin -hipotézise körül . A viták ellenére a dopamin -antagonisták továbbra is a skizofrénia standard és sikeres kezelése. Ezek az antagonisták közé tartoznak az első generációs (tipikus) antipszichotikumok , például butirofenonok , fenotiazinok és tioxantének . Ezeket a gyógyszereket nagyrészt felváltották a második generációs (atipikus) antipszichotikumok, például a klozapin és a paliperidon . Általában ezek a gyógyszerek nem magukra a dopamint termelő idegsejtekre hatnak, hanem a posztszinaptikus neuron receptorokra.
A substantia nigra-val kapcsolatos dopamin-hipotézist alátámasztó egyéb, nem farmakológiai bizonyítékok közé tartoznak a pars compacta szerkezeti változásai, például a szinaptikus terminális méret csökkentése. A substantia nigra egyéb változásai közé tartozik az NMDA -receptorok fokozott expressziója a substantia nigra -ban és a csökkent dysbindin -expresszió. Fokozott NMDA receptor pont bevonásával glutamát - dopamin kölcsönhatások skizofrénia. A (vitatottan) a skizofréniához köthető Dysbindin szabályozhatja a dopamin felszabadulását, és a dysbindin alacsony expressziója a substantia nigra -ban fontos lehet a skizofrénia etiológiájában. A szkizofrén agyban a substantia nigra változásai miatt végül lehetségessé válhat speciális képalkotó technikák (például neuromelanin-specifikus képalkotás) alkalmazása a szkizofrénia fiziológiai jeleinek kimutatására a substantia nigra-ban.
Fa mellkasi szindróma
A fából készült mellkas , más néven fentanil mellkasfal merevség szindróma, a szintetikus opioidok, például a fentanil , szulfentanil, Alfentanil , Remifentanil ritka mellékhatása . Ez a vázizomzat tónusának általános növekedését eredményezi . Úgy gondolják, hogy a mechanizmus a fokozott dopamin -felszabaduláson és a GABA -felszabadulás csökkentésén keresztül történik a substantia nigra/striatum idegeiben. A hatás leginkább a mellkasfal izmain jelentkezik, és a szellőzés károsodásához vezethet. Az állapotot leggyakrabban érzéstelenítésben figyelik meg, ahol ezeknek a gyógyszereknek a gyors és nagy dózisát intravénásan adják be.
Többszörös rendszeri sorvadás
A többszörös rendszeri sorvadást, amelyet a striatum és a substantia nigra neuronális degenerációja jellemez, korábban striatonigralis degenerációnak nevezték .
A substantia nigra kémiai módosítása
A substantia nigra kémiai manipulálása és módosítása fontos a neurofarmakológia és a toxikológia területén . Különféle vegyületeket, például levodopát és MPTP -t használnak a Parkinson -kór kezelésében és tanulmányozásában, és sok más gyógyszer is hatással van a substantia nigra -ra.
Amfetamin és nyomelemek
Tanulmányok kimutatták, hogy bizonyos agyi régiókban az amfetamin és a nyomelemek növelik a dopamin koncentrációját a szinaptikus hasadékban , ezáltal fokozzák a posztszinaptikus neuron válaszát. A különböző mechanizmusok, amelyek révén az amfetamin és nyomokban aminok befolyásolja dopaminkoncentráció már alaposan tanulmányozták, és ismertek egyaránt érintenek DAT és VMAT2 . Az amfetamin szerkezete hasonló a dopaminhoz és a nyomelemekhez; ennek következményeként bejuthat a preszinaptikus neuronba a DAT -on keresztül , valamint közvetlenül a neurális membránon keresztül. A preszinaptikus neuronba való belépéskor az amfetamin és a nyomelemek aktiválják a TAAR1-et , amely a protein-kináz jelátvitel révén dopamin-kiáramlást, foszforiláció-függő DAT internalizációt és nem versenyképes visszavétel gátlást indukál . Az amfetamin és a nyomelemek közötti hasonlóság miatt a monoamin transzporterek szubsztrátja is; ennek következtében (versenyszerűen) gátolja a dopamin és más monoaminok újrafelvételét azáltal, hogy versenyez velük a felvételért is.
Ezenkívül az amfetamin és a nyomelemek a neuronális vezikuláris monoamin transzporter, a vezikuláris monoamin 2 transzporter (VMAT2) szubsztrátjai . Amikor amfetamin felvesszük által VMAT2 , a vezikulum kibocsátások (effluxes) dopamin molekulák a citoszolba cserébe.
Kokain
A kokain hatásmechanizmusa az emberi agyban magában foglalja a dopamin újrafelvételének gátlását, amely a kokain addiktív tulajdonságainak köszönhető, mivel a dopamin a jutalom szempontjából kritikus neurotranszmitter. A kokain azonban aktívabb a ventrális tegmentális terület dopaminerg neuronjaiban, mint a substantia nigra. A kokain beadása fokozza az anyagcserét a substantia nigra-ban, ami megmagyarázhatja a megváltozott motoros funkciót, amelyet a kokaint használóknál tapasztaltak. A kokain dopamin -visszavételének gátlása szintén gátolja a pars compacta spontán akciós potenciáljának tüzelését. A mechanizmus, amellyel a kokain gátolja a dopamin újrafelvételt, magában foglalja annak kötődését a dopamin transzporter fehérjéhez. A tanulmányok azonban azt mutatják, hogy a kokain a DAT mRNS szintjének csökkenését is okozhatja , valószínűleg a kokain gátló dopamin receptorok miatt, nem pedig a transzkripciós vagy transzlációs útvonalakba való közvetlen beavatkozás miatt.
A substantia nigra inaktiválása a kokainfüggőség lehetséges kezelésének bizonyulhat. Egy kokainfüggő patkányokon végzett vizsgálatban a substantia nigra inaktiválása beültetett kanülökkel nagymértékben csökkentette a kokainfüggőség visszaesését.
Levodopa
A substantia nigra a Parkinson -kór kezelésére szolgáló vegyi terápiák célpontja. A levodopa (közismert nevén L-DOPA), a dopamin prekurzora, a leggyakrabban előírt gyógyszer a Parkinson-kórra, annak ellenére, hogy a dopamin és az L-DOPA neurotoxicitásáról viták vannak. A gyógyszer különösen hatékony a Parkinson -kór korai stádiumában lévő betegek kezelésében, bár idővel elveszíti hatékonyságát. A Levodopa áthatol a vér -agy gáton, és növeli a dopamin szintjét a substantia nigra -ban, ezáltal enyhíti a Parkinson -kór tüneteit. A levodopa -kezelés hátránya, hogy a Parkinson -kór tüneteit (alacsony dopaminszint) kezeli, nem pedig az okot (a dopaminerg neuronok elhalása a substantia nigra -ban).
MPTP
Az MPTP egy neurotoxin, amely specifikus az agy dopaminerg sejtjeire, különösen a substantia nigra -ban. Az MPTP 1982-ben került a figyelem középpontjába, amikor a kaliforniai heroinhasználók Parkinson-kórhoz hasonló tüneteket mutattak az MPTP- vel szennyezett MPPP használata után . A merev és szinte teljesen mozdulatlan betegek reagáltak a levodopa -kezelésre. A Parkinson-kórhoz hasonló tünetek remissziójáról nem számoltak be, ami a dopaminerg neuronok visszafordíthatatlan halálára utal. Az MPTP javasolt mechanizmusa magában foglalja a mitokondriális funkció megzavarását, beleértve az anyagcsere zavarait és a szabad gyökök keletkezését .
Röviddel ezután az MPTP -t állatmodelleken tesztelték a Parkinson -kór kiváltó hatékonyságában (sikerrel). Az MPTP főemlősökben akineziát, merevséget és remegést váltott ki, és neurotoxicitása nagyon specifikusnak bizonyult a substantia nigra pars compacta esetében. Más állatoknál, például rágcsálóknál a Parkinson -kór MPTP általi indukciója nem teljes, vagy sokkal nagyobb és gyakrabban szükséges adagokat igényel, mint a főemlősöknél. Ma az MPTP továbbra is a legkedveltebb módszer a Parkinson -kór állatmodellekben való kiváltására .
Történelem
A substantia nigra-t 1784-ben fedezte fel Félix Vicq-d'Azyr , és Samuel Thomas von Sömmerring 1791-ben utalt erre a szerkezetre. A substantia nigra pars reticulata és a compacta közötti különbséget először Sano javasolta 1910-ben. 1963-ban Oleh Hornykiewicz megfigyeléséből arra a következtetésre jutott, hogy "a (Parkinson -kórban szenvedő betegek) substantia nigra sejtvesztése lehet az oka a striatum dopaminhiányának".