Endometriális rák - Endometrial cancer
| Endometriális rák | |
|---|---|
| Más nevek | Méhrák |
 | |
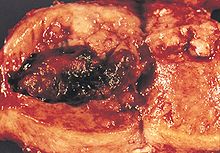
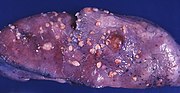
| Az endometrium rák lokalizációja és fejlődése. | |
| Különlegesség | Onkológia , nőgyógyászat |
| Tünetek | Hüvelyi vérzés , fájdalom vizeléssel vagy nemi közösüléssel , medencefájdalom |
| Szokásos kezdet | Menopauza után |
| Rizikó faktorok | Elhízás , túlzott ösztrogén expozíció, magas vérnyomás , cukorbetegség , családi anamnézis |
| Diagnosztikai módszer | Endometrium biopszia |
| Kezelés | Hasi méheltávolítás , sugárterápia , kemoterápia , hormonterápia |
| Prognózis | Ötéves túlélési arány ~ 80% (USA) |
| Frekvencia | 3,8 millió (összesen érintett 2015 -ben) |
| Halálozások | 89 900 (2015) |
Az endometrium rák olyan rák , amely az endometriumból ( a méh vagy a méh nyálkahártyájából) ered . Ez a sejtek rendellenes növekedésének eredménye , amelyek képesek behatolni vagy elterjedni a test más részeire. Az első jel leggyakrabban a menstruációhoz nem kapcsolódó hüvelyi vérzés . További tünetek közé tartozik a fájdalom vizelés , fájdalom közösülés során , vagy a kismedencei fájdalom . Az endometrium rák leggyakrabban a menopauza után fordul elő .
Az esetek körülbelül 40% -a elhízáshoz kapcsolódik . Az endometrium rák is társul túlzott ösztrogén expozícióhoz, magas vérnyomáshoz és cukorbetegséghez . Míg az ösztrogén önmagában történő alkalmazása növeli az endometriális rák kockázatát, mind az ösztrogén, mind a progesztogén együttes alkalmazása, mint a legtöbb fogamzásgátló tabletta , csökkenti a kockázatot. Az esetek két -öt százaléka a szülőktől örökölt génekhez kapcsolódik. Az endometrium rákot néha lazán " méhráknak " nevezik , bár különbözik a méhrák más formáitól, például a méhnyakráktól , a méhszarkómától és a trofoblasztos betegségektől . Az endometrium rák leggyakoribb típusa az endometrioid carcinoma , amely az esetek több mint 80% -át teszi ki. Az endometrium rákot általában endometrium biopsziával diagnosztizálják, vagy mintát vesznek a dilatáció és a curettage néven ismert eljárás során . A pap -kenet általában nem elegendő az endometrium rák kimutatására. A normál kockázatnak kitett személyek rendszeres szűrése nem szükséges.
Az endometriális rák vezető kezelési lehetősége a hasi méheltávolítás (a méh teljes eltávolítása műtéttel ), a kétoldali petevezetékek és petefészkek eltávolításával együtt, kétoldalú salpingo-oophorectomia . Előrehaladottabb esetekben sugárterápia , kemoterápia vagy hormonterápia is javasolható. Ha a betegséget korai stádiumban diagnosztizálják , az eredmény kedvező, és az Egyesült Államokban a teljes ötéves túlélési arány meghaladja a 80%-ot.
2012 -ben 320 000 nőnél jelentkezett újonnan méhnyálkahártya -rák, és 76 000 halálesetet okozott. Ezzel a harmadik leggyakoribb halálok a rákos megbetegedésekben, amelyek csak a nőket érintik, a petefészek- és méhnyakrák mögött . A fejlett világban gyakoribb, és a fejlett országokban a női reproduktív traktus leggyakoribb rákja . A méhnyálkahártya rákos megbetegedések aránya számos országban emelkedett az 1980 -as és 2010 -es évek között. Ez feltehetően az időskorúak növekvő számának és az elhízás gyakoriságának köszönhető.
jelek és tünetek
A hüvelyi vérzés vagy foltosodás a nőknél a menopauza után az endometrium rák 90% -ában fordul elő. A vérzés különösen gyakori adenokarcinóma esetén , az esetek kétharmadában fordul elő. A rendellenes menstruációs ciklus vagy a rendkívül hosszú, erős vagy gyakori vérzés a nőknél a menopauza előtt is az endometrium rák jele lehet.
A vérzéstől eltérő tünetek nem gyakoriak. Egyéb tünetek közé tartozik a vékony fehér vagy tiszta hüvelyváladék a posztmenopauzás nőknél. A fejlettebb betegség nyilvánvalóbb tüneteket vagy jeleket mutat, amelyek fizikai vizsgálaton észlelhetők . A méh megnagyobbodhat, vagy a rák elterjedhet, ami alsó hasi fájdalmat vagy medencei görcsöket okozhat. A fájdalmas szexuális kapcsolat vagy fájdalmas vagy nehéz vizelés kevésbé gyakori jelei az endometrium ráknak. A méh gennyes ( pyometrea ) is megtelhet . Az ilyen ritkább tünetekkel (hüvelyváladék, kismedencei fájdalom és genny) rendelkező nők 10-15% -a rákos.
Rizikó faktorok
Rizikófaktorai méhnyálkahártya rák közé elhízás , cukorbetegség , mellrák , használata tamoxifen , sosem volt gyermeke , késő menopauza, a magas ösztrogén , és a növekvő életkor. A bevándorlási tanulmányok (migrációs tanulmányok), amelyek a rákkockázat változását vizsgálják a különböző arányú országok között mozgó populációkban, azt mutatják, hogy az endometrium ráknak van valamilyen környezeti összetevője. Ezek a környezeti kockázati tényezők nincsenek jól jellemezve.
Hormonok
Az endometriális rák kockázati tényezőinek nagy része magas ösztrogénszintet tartalmaz. A becslések szerint az esetek 40% -a összefügg az elhízással. Elhízás esetén a zsírszövet feleslege növeli az androstenedion ösztronné , ösztrogénné történő átalakulását . Magasabb ösztronszint a vérben kevesebb vagy egyáltalán nem okoz ovulációt, és az endometriumot folyamatosan magas ösztrogénszintnek teszi ki. Az elhízás miatt kevesebb ösztrogén is távozik a vérből. A policisztás petefészek -szindróma (PCOS), amely szintén szabálytalan vagy egyáltalán nem okoz ovulációt, magasabb endometriális rákos megbetegedésekkel jár együtt, ugyanazon okok miatt, mint az elhízás. Konkrétan az elhízás, a II. Típusú cukorbetegség és az inzulinrezisztencia az I. típusú endometrium rák kockázati tényezői. Az elhízás 300-400%-kal növeli az endometrium rák kockázatát.
Az ösztrogénpótló terápia a menopauza idején, amikor a progesztinnel nincs kiegyensúlyozott (vagy "ellentétes"), egy másik kockázati tényező. Nagyobb dózisok vagy hosszabb ösztrogén terápia esetén nagyobb az endometrium rák kockázata. Az alacsonyabb súlyú nők nagyobb kockázatot jelentenek az ellenállás nélküli ösztrogén miatt. A hosszabb termékenységi időszak - akár a korai első menstruáció, akár a késői menopauza óta - szintén kockázati tényező. Az ellenállás nélküli ösztrogén 2-10 -szeresére növeli az egyén endometriális rák kockázatát, a testsúlytól és a terápia hosszától függően. A transz -férfiaknál, akik tesztoszteront szednek, és nem végeztek méheltávolítást, a tesztoszteron ösztrogénné történő átalakítása androsztendionon keresztül magasabb endometriális rák kockázatához vezethet.
Genetika
A genetikai rendellenességek is okozhatnak méhnyálkahártya -rákot. Összességében az örökletes okok járulnak hozzá az endometriális rákos esetek 2–10% -ához. A Lynch -szindróma , egy autoszomális domináns genetikai rendellenesség, amely főként vastagbélrákot okoz , szintén méhnyálkahártya -rákot okoz, különösen a menopauza előtt. A Lynch -szindrómában szenvedő nőknél 40–60% az endometriális rák kialakulásának kockázata, magasabb, mint a vastag- és végbélrák vagy a petefészekrák kialakulásának kockázata. A petefészekrák és az endometrium rák egyidejűleg alakul ki az emberek 20% -ában. Az endometriális rák szinte mindig a vastagbélrák előtt alakul ki, átlagosan 11 évvel azelőtt. A Lynch -szindrómában a karcinogenezis az MLH1 vagy az MLH2 mutációjából származik: olyan gének, amelyek részt vesznek az eltérések helyreállításában , ami lehetővé teszi a sejt számára, hogy kijavítsa a DNS hibáit. A Lynch -szindrómában mutált egyéb gének közé tartozik az MSH2 , az MSH6 és a PMS2 , amelyek szintén nem egyező javító gének. A Lynch -szindrómás nők az endometriális rákos esetek 2-3% -át teszik ki; egyes források szerint ez akár 5%is lehet. A génmutációtól függően a Lynch -szindrómában szenvedő nők különböző endometriális rák kockázatokkal rendelkeznek. MLH1 mutációk esetén a kockázat 54%; MSH2 -vel 21%; és MSH6 esetén 16%.
Azok a nők, akiknek családjában előfordult méhnyálkahártya -rák, nagyobb kockázatnak vannak kitéve. Két gén, amelyek leggyakrabban társulnak más nők rákos megbetegedéseihez, a BRCA1 és a BRCA2 , nem okoznak méhnyálkahártya -rákot. Látható összefüggés van ezekkel a génekkel, de ez a tamoxifen alkalmazásának tulajdonítható, amely gyógyszer önmagában is endometrium rákot okozhat emlő- és petefészekrákokban. Az öröklött genetikai állapot A Cowden -szindróma endometrium rákot is okozhat. Az ilyen rendellenességben szenvedő nők 5–10% -kal kockáztatják életük során az endometriális rák kialakulását, szemben az érintetlen nők 2-3% -os kockázatával.
A közös genetikai eltérésekről azt is kimutatták, hogy befolyásolják az endometrium rák kockázatát nagyméretű, genomra kiterjedő asszociációs vizsgálatokban . Tizenhat genomiális régió társult endometriális rákhoz, és a közös változatok a családi relatív kockázat 7% -át magyarázzák.
Egyéb egészségügyi problémák
A rák más formáinak bizonyos terápiái növelik az endometriális rák élettartamának kockázatát, ami 2-3%. A tamoxifen, az ösztrogén-pozitív emlőrák kezelésére használt gyógyszer, a felhasználók körülbelül 0,1% -ánál, különösen az idősebb nőknél társult endometrium-rákhoz, de a tamoxifen túlélésének előnyei általában meghaladják az endometrium-rák kockázatát. Egy-két éves tamoxifen-kúra körülbelül megkétszerezi az endometrium-rák kockázatát, az ötéves terápia pedig megnégyszerezi ezt a kockázatot. A raloxifen , hasonló gyógyszer, nem emelte az endometrium rák kockázatát. Korábban a petefészekrák kockázati tényezője volt az endometrium ráknak, akárcsak a kismedencei sugárkezelés. Pontosabban, a petefészek granulosa sejtdaganatok és a kómák endometriális rákhoz társuló daganatok.
Az endometriális rákban az alacsony immunfunkció is szerepet játszik. A magas vérnyomás szintén kockázati tényező, de ennek oka lehet az elhízás. A hosszabb ideig tartó rendszeres ülés magasabb endometriális rák okozta halálozással jár. A kockázatot nem csökkenti a rendszeres testmozgás, bár csökkenti.
Védő tényezők
A dohányzás és a progesztin használata egyaránt véd az endometrium rák ellen. A dohányzás védelmet nyújt az ösztrogén anyagcseréjének megváltoztatásával, valamint a fogyás és a korai menopauza elősegítésével. Ez a védő hatás a dohányzás abbahagyása után is sokáig tart. A progesztin a kombinált orális fogamzásgátló tablettában és a méhen belüli hormonális eszközben (IUD) van jelen. A kombinált orális fogamzásgátlók annál tovább csökkentik a kockázatot, minél hosszabb ideig szedik őket: 56% -kal négy év után, 67% -kal nyolc év után és 72% -kal tizenkét év után. Ez a kockázatcsökkentés legalább tizenöt évig folytatódik a fogamzásgátló használatának abbahagyása után. Az elhízott nőknek nagyobb dózisú progesztinre lehet szükségük a védelemhez. Ötnél több csecsemő születése (nagy multiparitás) szintén védő tényező, és legalább egy gyermek születése 35%-kal csökkenti a kockázatot. A több mint 18 hónapos szoptatás 23%-kal csökkenti a kockázatot. A fokozott fizikai aktivitás 38–46%-kal csökkenti az egyén kockázatát. Előzetes bizonyítékok vannak arra, hogy a szója fogyasztása védelmet nyújt.
Patofiziológia
|
Az endometrium rák akkor alakul ki, ha a normális endometriumsejtek növekedése hibás . Általában, amikor a sejtek megöregednek vagy megsérülnek, meghalnak , és új sejtek lépnek a helyükre. A rák akkor kezdődik, amikor új sejtek keletkeznek szükségtelenül, és a régi vagy sérült sejtek nem pusztulnak el megfelelően. Az extra sejtek felhalmozódása gyakran szövettömeget képez növekedésnek vagy tumornak. Ezeknek a kóros rákos sejteknek számos genetikai rendellenessége van , amelyek túlzott növekedést okoznak.
Az endometrium rákos megbetegedéseinek 10–20% -ában, többnyire 3. fokozatban (a legmagasabb szövettani fokozat ) mutációk találhatók egy tumorszuppresszor génben, általában a p53 -ban vagy a PTEN -ben . A 20% endometriális hiperpláziák és 50% a endometrioid rákok , PTEN szenved loss-of-function mutáció vagy null mutáció , így kevésbé hatékony, vagy teljesen hatástalan. A PTEN funkció elvesztése a PI3k/Akt/mTOR útvonal szabályozásához vezet, ami sejtnövekedést okoz. A p53 útvonal elnyomható vagy erősen aktiválható endometriális rák esetén. Amikor a p53 mutáns változata túlexpresszálódik, a rák különösen agresszív. A P53 mutációk és a kromoszóma instabilitás serozus karcinómákkal jár, amelyek hajlamosak a petefészek és a petefészekrákra hasonlítani. A véres karcinómák feltehetően endometrium intraepithelialis karcinómából alakulnak ki .
A PTEN és a p27 funkciómutációk elvesztése jó prognózissal jár, különösen elhízott nőknél. A Her2/neu onkogén , amely rossz prognózist jelez, az endometrioid és a savós karcinómák 20% -ában fejeződik ki. A CTNNB1 (béta-katenin; transzkripciós gén) mutációk az endometrium rák 14–44% -ában fordulnak elő, és jó prognózist jelezhetnek, de az adatok nem egyértelműek. A béta-katenin mutációkat általában laphámsejtek endometriális rákjaiban találják meg . Az FGFR2 mutációk az endometriális rákok körülbelül 10% -ában fordulnak elő, és prognosztikai jelentőségük nem egyértelmű. A SPOP egy másik tumorszuppresszor gén, amelyről kimutatták, hogy az endometriumrák bizonyos esetekben mutálódott: a tiszta sejtes endometriális karcinómák 9% -ánál és a savós endometrium -karcinómák 8% -ánál mutációk vannak ebben a génben.
Az I. és II. Típusú rákok (amelyeket alább ismertetünk) általában különböző mutációkkal járnak. Az ARID1A, amely gyakran pontmutációt hordoz az I. típusú endometriális rákban, az endometrium tiszta sejtes karcinómáinak 26% -ában és a savós karcinómák 18% -ában is mutálódik. Az I. típusú endometriális rákban általában számos gén epigenetikus elnémítása és pontmutációi találhatók. A tumorszuppresszor gének mutációi gyakoriak a II. Típusú endometrium rákban. A PIK3CA általában mind az I., mind a II. A Lynch-szindrómával összefüggő endometrium-rákban szenvedő nőknél gyakori a mikroszatellit-instabilitás .
Az endometrium hiperplázia ( endometriumsejtek túlnövekedése) kialakulása jelentős kockázati tényező, mivel a hiperpláziák adenokarcinómává válhatnak és gyakran alakulnak ki, bár a rák hiperplázia jelenléte nélkül is kialakulhat. Tíz éven belül az atipikus endometrium hiperpláziák 8–30% -a rákosodik, míg a nem atipikus hiperpláziák 1–3% -a. Az atipikus hiperplázia a magokban látható rendellenességeket mutat . A rák előtti endometrium hyperplasiákat endometrium intraepithelialis neoplasiának is nevezik . A KRAS gén mutációi endometrium hiperpláziát és ezáltal I. típusú endometrium rákot okozhatnak. Az endometrium hiperplázia jellemzően 40 éves kor után jelentkezik. Az endometrium mirigy diszplázia a p53 túlzott expressziója esetén fordul elő, és savós karcinómává fejlődik.
Diagnózis
Az endometrium rák diagnosztizálását először fizikális vizsgálat, endometrium biopszia vagy dilatáció és curettage (endometriumszövet eltávolítása; D & C) végzi. Ezt a szövetet ezután szövettanilag megvizsgálják a rák jellemzői szempontjából. Ha rákot találnak, orvosi képalkotást lehet végezni annak megállapítására, hogy a rák elterjedt vagy behatolt a szövetbe.
Vizsgálat
A tünetmentes emberek rutinszerű szűrése nem indokolt, mivel a betegség korai, tüneti stádiumában jól gyógyítható. Ehelyett a nőknek, különösen a menopauzás nőknek tisztában kell lenniük az endometriális rák tüneteivel és kockázati tényezőivel. A méhnyak -szűrővizsgálat , például a Pap -kenet , nem hasznos diagnosztikai eszköz az endometriális rák kezelésére, mivel a kenet 50% -ban normális lesz. A Pap -kenet segítségével kimutatható a méhnyakra terjedő betegség. A kismedencei vizsgálat eredményei gyakran normálisak, különösen a betegség korai szakaszában. Ha a betegség előrehaladottabb, a méh vagy a környező, tartószerkezetek mérete, alakja vagy állaga megváltozhat. A méhnyak -szűkület , a méhnyaknyílás szűkülése az endometrium rák jele, amikor genny vagy vér található a méhben (pyometra vagy hematometra ).
A Lynch-szindrómás nőknek 35 éves korukban el kell kezdeniük az éves biopsziás szűrést. Néhány Lynch-szindrómás nő profilaktikus méheltávolítást és salpingo-oophorectomiát választ, hogy jelentősen csökkentse az endometrium- és a petefészekrák kockázatát.
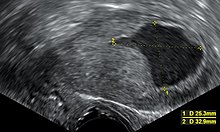
A posztmenopauzális vérzésben szenvedő nők endometrium vastagságának vizsgálatára szolgáló transzvaginális ultrahangot egyre inkább használják az endometriumrák diagnosztizálására az Egyesült Államokban. Az Egyesült Királyságban mind az endometriális biopszia , mind a transzvaginális ultrahang együttes alkalmazása az endometriális rák diagnosztizálásának standardja. A transzvaginális ultrahangon látható szövet homogenitása segíthet annak megállapításában, hogy a vastagság rákos -e. Az ultrahangos eredmények önmagukban nem meggyőzőek a méhnyálkahártya rákos megbetegedéseiben, ezért egy másik szűrési módszert (például endometrium biopsziát) kell alkalmazni együtt. Más képalkotó vizsgálatok korlátozottan használhatók. A CT-vizsgálatot olyan daganatok műtét előtti képalkotására használják, amelyek a fizikális vizsgálat során előrehaladottnak tűnnek, vagy magas kockázati altípussal rendelkeznek (nagy áttét kockázata ). Használhatók extrapelvicus betegségek vizsgálatára is. Az MRI segíthet annak megállapításában, hogy a rák átterjedt -e a méhnyakra, vagy endocervicalis adenocarcinoma -e. Az MRI a közeli nyirokcsomók vizsgálatához is hasznos.
A dilatációt és a kuretátust vagy az endometriális biopsziát szövetmintának veszik a szövettani vizsgálathoz. Az endometrium biopszia a kevésbé invazív lehetőség, de nem biztos, hogy minden alkalommal meggyőző eredményeket ad. A hiszteroszkópia csak az endometrium teljes anatómiáját mutatja, amely gyakran nem utal rákra, ezért nem használják, kivéve, ha biopsziával együtt. A hiszteroszkópia alkalmazható a rák diagnózisának megerősítésére. Az új bizonyítékok azt mutatják, hogy a D&C hamis negatív aránya magasabb, mint az endometrium biopsziája.
A kezelés megkezdése előtt számos más vizsgálat javasolt. Ezek közé tartozik a mellkasröntgen, a májfunkciós tesztek , a veseműködés-vizsgálatok , valamint a CA-125 szintjének vizsgálata , amely daganatjelző , amely megemelkedhet endometriális rák esetén.
Osztályozás
Az endometrium rákos megbetegedései lehetnek hámsejtekből származó daganatok (karcinómák), vegyes hám- és mesenchymális daganatok (carcinosarcomas) vagy mesenchymalis tumorok.
Az endometriális karcinómák hagyományos besorolása vagy klinikai és endokrin jellegzetességeken (I. és II. Típus), vagy szövettani jellegzetességein (endometrioid, szerózus és tiszta sejt) alapul. Egyes daganatokat nehéz osztályozni, és jellemzőik egynél több kategóriát fednek át. Különösen a magas fokú endometrioid tumorok jellemzően mind az I, mind a II.
Karcinóma
Az endometrium rákos megbetegedéseinek túlnyomó többsége karcinóma (általában adenokarcinóma), ami azt jelenti, hogy az endometriumot szegélyező és a méhnyálkahártya -mirigyeket alkotó hámsejtek egyetlen rétegéből származnak . Az endometriális karcinóma számos mikroszkopikus altípusa létezik, de a klinikai jellemzők és a patogenezis alapján nagyjából két kategóriába sorolhatók, I. és II. A két altípus genetikailag különbözik egymástól.
Az I. típusú endometriális karcinómák leggyakrabban a menopauza előtt és környékén fordulnak elő. Az Egyesült Államokban gyakoribbak a fehér nőknél , különösen azoknál, akiknek kórelőzményében endometrium hyperplasia szerepel. Az I. típusú endometrium rák gyakran alacsony fokú, minimálisan invazív a méhfal alá ( myometrium ), ösztrogénfüggő, és jó kimenetelű a kezelés során. Az I. típusú karcinómák az endometrium rák 75-90% -át teszik ki.
A II. Típusú endometrium karcinóma általában idősebb, posztmenopauzális embereknél fordul elő, az Egyesült Államokban gyakoribb a fekete nőknél , és nem jár együtt az ösztrogén fokozott expozíciójával vagy az endometrium hiperpláziájával. A II. Típusú endometriális rák gyakran magas fokú, mélyen behatol a méhfalba (myometrium), szerózus vagy tiszta sejt típusú, és rosszabb prognózissal rendelkezik. A tünetek értékelésekor epiteliális petefészekráknak tűnhetnek . Hajlamosak később megjelenni, mint az I. típusú daganatok, és agresszívebbek, nagyobb a kiújulás és/vagy áttét veszélye.
Endometrioid adenokarcinóma
Az endometrioid adenokarcinóma esetén a rákos sejtek a normál méhnyálkahártyára emlékeztető mintákban nőnek, sok új mirigy képződik az oszlopos hámból néhány kóros maggal . Az alacsony fokú endometrioid adenokarcinómák jól differenciált sejtekkel rendelkeznek, nem hatoltak be a myometriumba, és az endometrium hyperplasia mellett láthatók. A daganat mirigyei nagyon közel állnak egymáshoz, anélkül, hogy a sztrómaszövet normálisan elválasztaná őket. A magasabb fokozatú endometrioid adenokarcinómák kevésbé jól differenciált sejtekkel rendelkeznek, több szilárd sejtrétegük van a daganatsejtekből, amelyek már nem szerveződnek mirigyekbe, és atrófiás endometriumhoz kapcsolódnak. Az endometrioid adenokarcinóma számos altípusa hasonló prognózisú, beleértve a villoglandularis, szekréciós és csillósejtes variánsokat. Van egy altípus is, amelyet a lapos differenciálódás jellemez . Néhány endometrioid adenokarcinómában nyálkahártya -karcinóma van.
Az endometrioid adenokarcinómához leggyakrabban társuló genetikai mutációk a PTEN génekben, a tumorszuppresszorban találhatók; PIK3CA, kináz ; KRAS, egy GTPáz, amely a jelátvitelben működik ; és CTNNB1, amelyek részt vesznek az adhézióban és a sejtek jelzésében. A CTNNB1 (béta-katenin) gén leggyakrabban az endometrioid adenokarcinóma lapos altípusában mutálódik.
Séros karcinóma
A savós karcinóma egy II. Típusú endometriális daganat, amely a diagnosztizált endometriumrák 5-10% -át teszi ki, és gyakori a posztmenopauzális nőknél, akiknél sorvadt méhnyálkahártya és fekete nők vannak. A savós méhnyálkahártya -karcinóma agresszív, gyakran behatol a myometriumba, és áttéteket okoz a hashártyán belül ( omentális csomósodásnak tekinthető ) vagy a nyirokrendszerben. Szövettanilag sok atipikus maggal, papilláris struktúrával és az endometrioid adenokarcinómákkal ellentétben az oszlopos sejtek helyett lekerekített sejtekkel jelenik meg. Az endometrium szerózus karcinómáinak nagyjából 30% -a psammoma testtel is rendelkezik . A savós karcinómák másképp terjednek, mint a legtöbb más méhnyálkahártya -rák; a méhen kívül is elterjedhetnek anélkül, hogy behatolnának a myometriumba.
A savós karcinóma genetikai mutációi a kromoszóma instabilitás és a TP53 , egy fontos daganatszuppresszor gén mutációi.
Tiszta sejtes karcinóma
A tiszta sejtes karcinóma II. Típusú endometriális daganat, amely a diagnosztizált endometriális rák kevesebb mint 5% -át teszi ki. A savós sejtes karcinómához hasonlóan általában agresszív és rossz prognózissal jár. Szövettanilag az összes tiszta sejtre jellemző tulajdonságok jellemzik : az azonos nevű tiszta citoplazma, amikor H&E festett és látható, különálló sejtmembrán. A p53 sejt jelzőrendszer nem aktív endometrium tiszta sejtes karcinóma esetén. Az endometrium ráknak ez a formája gyakoribb a posztmenopauzás nőknél.
Nyálkahártya -karcinóma
A nyálkahártya -karcinóma az endometriális rák ritka formája, amely az összes diagnosztizált endometrium -rák kevesebb mint 1-2% -át teszi ki. A nyálkahártya -endometriális karcinómák leggyakrabban I. és I. fokozatúak, jó prognózist biztosítanak számukra. Jellemzően jól differenciált oszlopos sejtjeik vannak, amelyek mirigyekbe vannak rendezve , a citoplazmában jellemző mucinokkal . A nyálkahártya -karcinómákat meg kell különböztetni a nyaki adenokarcinómától .
Vegyes vagy differenciálatlan karcinóma
Vegyes karcinómák azok, amelyek I. és II. Típusú sejteket is tartalmaznak, és az egyik a tumor legalább 10% -át teszi ki. Ezek közé tartozik a rosszindulatú vegyes Müller -féle daganat , amely az endometrium hámjából származik és rossz prognózissal rendelkezik.
A differenciálatlan endometriális karcinómák a diagnosztizált endometriális rákok kevesebb mint 1-2% -át teszik ki. Rosszabb a prognózisuk, mint a III. Szövettanilag ezek a daganatok azonos hámsejteket tartalmaznak, azonosítható mintázat nélkül.
Egyéb karcinómák
A nem metasztatikus laphám- és átmeneti sejtes karcinóma nagyon ritka az endometriumban. Az endometrium laphámsejtes karcinómája rossz prognózissal rendelkezik. Az orvosi szakirodalomban kevesebb, mint 100 -szor jelentették az 1892. évi jellemzése óta. Az endometrium primer laphámsejtes karcinómájának (PSCCE) diagnosztizálásához nem lehet más primer rák az endometriumban vagy a méhnyakban, és nem lehet a nyaki hámhoz kapcsolódik. Ennek a daganatnak a ritkasága miatt nincsenek irányelvek a kezelésre, és nincs tipikus kezelés sem. A gyakori genetikai okok továbbra is jellemzetlenek. Az endometrium primer átmeneti sejtes karcinómái még ritkábbak; 2008 -tól 16 esetet jelentettek. Patofiziológiáját és kezeléseit nem jellemezték. Szövettanilag a TCCE hasonlít az endometrioid karcinómára, és különbözik a többi átmeneti sejtes karcinómától.
Szarkóma
Az endometriális karcinómákkal ellentétben a ritkán előforduló endometrium sztróma- szarkóma olyan rák, amely az endometrium nem mirigyes kötőszövetéből származik. Általában nem agresszívak, és ha ismétlődnek, évtizedekig is eltarthatnak. A metasztázisok a tüdőben és a kismedencei vagy peritoneális üregekben a leggyakoribbak. Általában ösztrogén- és/vagy progeszteronreceptorokkal rendelkeznek. Az alacsony fokú endometriális stroma szarkóma prognózisa jó, az ötéves túlélés 60–90%. A magas fokú differenciálatlan endometrium-szarkóma (HGUS) rosszabb prognózisú, magas kiújulási aránya és 25% -os ötéves túlélése. A HGUS prognózisát az határozza meg, hogy a rák behatolt -e az artériákba és a vénákba. Vaszkuláris invázió nélkül az ötéves túlélés 83%; 17% -ra csökken, ha vaszkuláris inváziót figyelnek meg. Az I. stádiumú ESS a legjobb prognózisú, ötéves túlélése 98%, tízéves túlélése 89%. Az ESS a méhrák 0,2% -át teszi ki.
Metasztázis
Az endometriális rák gyakran áttéteket okoz a petefészkekben és a petevezetékekben, amikor a rák a méh felső részében található, és a méhnyak, amikor a rák a méh alsó részében van. A rák általában először a myometriumba és a szerosába terjed , majd más reproduktív és kismedencei struktúrákba. Amikor a nyirokrendszer érintett, a medencei és para-aorta csomópontok általában először érintettek, de nem specifikus mintázatban, ellentétben a méhnyakrákkal. A távolabbi áttéteket a vér terjeszti, és gyakran előfordulnak a tüdőben, valamint a májban, az agyban és a csontokban. Az endometriális rák az esetek 20-25% -ában áttétet ad a tüdőbe, többet, mint bármely más nőgyógyászati rák.
Szövettani
Az endometriális rákok szövettani osztályozására háromlépcsős rendszer létezik, a jól differenciált sejtekkel (I. fokozat) a nagyon gyengén differenciált sejtekkel (III. Fokozat) terjed. Az I. fokozatú rák a legkevésbé agresszív és a legjobb prognózisú, míg a III. A II. Fokú rákos megbetegedések az I. és III.
Az endometrium rákos szövettani szövettana nagyon változatos. A leggyakoribb megállapítás egy jól differenciált endometrioid adenokarcinóma, amely számos, kicsi, zsúfolt mirigyből áll, különböző fokú nukleáris atípiával, mitotikus aktivitással és rétegződéssel. Ez gyakran megjelenik az endometrium hyperplasia hátterében. A Frank adenokarcinómát meg lehet különböztetni az atipikus hiperpláziától az egyértelmű stróma invázió vagy a "hátsó hátsó" mirigyek megállapításával, amelyek az endometriális sztróma roncsolásmentes cseréjét jelentik a rákkal. A betegség előrehaladtával a myometrium beszivárog.
Staging
Az endometrium karcinómát sebészeti úton állítják elő a FIGO rákos stádiumrendszer segítségével. A 2009 -es FIGO átmeneti rendszer a következő:
| Színpad | Leírás |
|---|---|
| IA | A daganat a méhre korlátozódik, a myometrium inváziójának kevesebb mint a fele |
| IB | A daganat a méhre korlátozódik, a myometrium inváziójának több mint a fele |
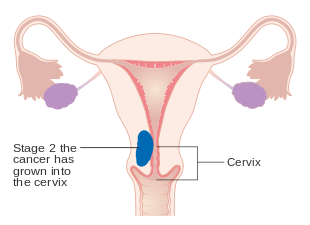
| II | A daganat magában foglalja a méhet és a nyaki sztrómát |
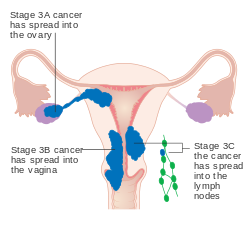
| IIIA | A daganat behatol a serosa vagy az adnexa területére |
| IIIB | Hüvelyi és/vagy paraméteres érintettség |
| IIIC1 | Kismedencei nyirokcsomók érintettsége |
| IIIC2 | Para-aorta nyirokcsomó érintettség, medencecsomó érintettséggel vagy anélkül |
| IVA | A daganat behatol a hólyag nyálkahártyájába és/vagy a bélnyálkahártyába |
| IVB | Távoli áttétek, beleértve a hasi áttéteket és/vagy inguinalis nyirokcsomókat |
A myometriális invázió és a kismedencei és para-aorta nyirokcsomók érintettsége a leggyakrabban észlelt terjedési minták. Néha a 0. szakasz is szerepel, ebben az esetben " in situ carcinoma " -nak nevezik . A feltehetően korai stádiumú rákok 26% -ában az intraoperatív stádium kismedencei és távoli áttéteket tárt fel, ami átfogó sebészeti beavatkozást tesz szükségessé.
Menedzsment
Sebészet
Az endometrium rák kezdeti kezelése műtét; Az endometriumrákban szenvedő nők 90% -át valamilyen műtéttel kezelik. A sebészeti kezelés jellemzően méheltávolításból áll, beleértve a kétoldalú salpingo-oophorectomiát , amely a méh eltávolítását jelenti, valamint a petefészkeket és a petevezetékeket. A limfadenektómiát vagy a kismedencei és para-aorta nyirokcsomók eltávolítását II. Vagy annál magasabb szövettani osztályú daganatok esetén végzik. A limfadenektómiát rendszeresen végzik az Egyesült Államokban az endometriális rák minden stádiumában, de az Egyesült Királyságban a nyirokcsomókat általában csak a II. Vagy annál magasabb stádiumú betegség esetén távolítják el. A limfadenektómia témája és az, hogy milyen túlélési előnyöket kínál az I. stádiumú betegségben, még vita tárgya. A feltételezett I. stádiumú betegségben szenvedő nők esetében a 2017 -es szisztematikus áttekintés nem talált bizonyítékot arra, hogy a limfadenektómia csökkenti a halál vagy a rák kiújulásának kockázatát, összehasonlítva a limfadenektómia hiányával. A nyirokcsomó -eltávolításon átesett nők nagyobb valószínűséggel tapasztalnak műtéttel vagy nyiroködémával/limfociszták kialakulásával kapcsolatos szisztémás morbiditást. A III és IV stádiumú rákos megbetegedésekben a citoreduktív műtét a normális, és az omentum biopsziája is szerepelhet. A IV. Stádiumú betegségben, ahol távoli áttétek vannak, a sebészeti beavatkozás alkalmazható a palliatív terápia részeként. A laparotomia , a nyitott hasi eljárás a hagyományos sebészeti beavatkozás; azonban a feltételezett korai stádiumú primer endometrium rákos betegeknél a laparoszkópia (kulcslyukműtét) csökkent műtéti morbiditással és hasonló általános és betegségmentes túléléssel jár. A méh eltávolítása a hason keresztül ajánlott a hüvelyen keresztül történő eltávolítás helyett, mivel ez lehetőséget ad a hasüreg vizsgálatára és mosására , hogy felfedezzék a rák további jeleit. A rák stádiumát a műtét során végzik.
A műtét kevés ellenjavallata a működésképtelen daganat, a tömeges elhízás, a különösen magas kockázatú műtét vagy a termékenység megőrzése. Ezek az ellenjavallatok az esetek 5-10% -ában fordulnak elő. Azok a nők, akik meg akarják őrizni termékenységüket és alacsony fokú I. stádiumú rákban szenvednek, progesztinekkel kezelhetők, egyidejű tamoxifen-terápiával vagy anélkül. Ez a terápia addig folytatható, amíg a rák nem reagál a kezelésre, vagy amíg a gyermekvállalás meg nem történik. A méh perforációja előfordulhat D & C vagy endometrium biopszia során. Az endometriális rák eltávolítására irányuló műtét mellékhatásai közé tartozhat a szexuális diszfunkció, az ideiglenes inkontinencia és a nyiroködéma , valamint a műtétek gyakoribb mellékhatásai, beleértve a székrekedést is .
Kiegészítő terápia
Számos lehetséges kiegészítő terápia létezik. A műtétet sugárkezelés és/vagy kemoterápia követheti magas kockázatú vagy magas fokú rák esetén. Ezt hívják adjuváns terápiának .
Kemoterápia
Az adjuváns kemoterápia egy közelmúltbeli újítás, amely paklitaxel (vagy más taxánok, például docetaxel ), doxorubicin (és más antraciklinek ) és platinok (különösen ciszplatin és karboplatin ) kombinációjából áll . Azt találták, hogy az adjuváns kemoterápia jobban növeli a túlélést a III. És IV. Stádiumú rákban, mint a hozzáadott sugárkezelés . A nem megfelelő illeszkedést javító gének mutációi, mint például a Lynch -szindrómában, a platinokkal szembeni rezisztenciához vezethetnek, ami azt jelenti, hogy a platinokkal végzett kemoterápia hatástalan az ilyen mutációjú embereknél. A kemoterápia mellékhatásai gyakoriak. Ezek közé tartozik a hajhullás , az alacsony neutrofilszint a vérben és az emésztőrendszeri problémák.
Azokban az esetekben, amikor a műtét nem javallott, a palliatív kemoterápia egy lehetőség; a nagyobb dózisú kemoterápia hosszabb túléléssel jár. A palliatív kemoterápiát, különösen a kapecitabint és a gemcitabint alkalmazva , gyakran használják a visszatérő endometriális rák kezelésére is.
Az alacsony bizonyosságú bizonyítékok arra utalnak, hogy a visszatérő endometriális rákos nőknél, akik kemoterápiás kezelésben részesültek, az mTOR útvonalat gátló gyógyszerek alkalmazása csökkentheti a betegség súlyosbodásának kockázatát a több kemoterápiához vagy hormonterápiához képest. Bár az mTOR inhibitorok növelhetik az emésztőrendszeri fekélyek kialakulásának esélyét.
Sugárterápia
Az adjuváns sugárterápiát általában korai stádiumú (I. vagy II. Stádiumú) endometriális rákban alkalmazzák. Hormonális brachyterápiával (VBT), amely a csökkent toxicitás miatt az előnyben részesített módszernek, vagy külső sugárkezeléssel (EBRT) szállítható. A brachyterápia során sugárforrást helyeznek az érintett szervbe; endometrium rák esetén sugárforrást helyeznek közvetlenül a hüvelybe. A külső sugárkezelés magában foglalja a testen kívülről az érintett területre irányuló sugárnyalábot. A VBT -t kizárólag a hüvelyben maradt rák kezelésére használják, míg az EBRT -t a műtét után a medence más részein lévő rák kezelésére. Az adjuváns sugárkezelés előnyei azonban vitatottak. Bár az EBRT jelentősen csökkenti a medence kiújulásának arányát, a teljes túlélés és a metasztázisok aránya nem javul. A VBT jobb életminőséget biztosít, mint az EBRT.
A sugárterápia bizonyos esetekben a műtét előtt is alkalmazható. Ha a műtét előtti képalkotás vagy klinikai értékelés azt mutatja, hogy a daganat behatol a méhnyakba, sugárzás adható a teljes méheltávolítás előtt . A brachyterápia és az EBRT önmagában vagy kombinációban is alkalmazható, ha a méheltávolítás ellenjavallt. A sugárkezelés mindkét szállítási módja mellékhatásokkal jár, különösen a gyomor -bél traktusban .
Hormonális terápia
A hormonális terápia csak bizonyos típusú endometriális rák esetén előnyös. Valamikor azt hitték, hogy a legtöbb esetben hasznos. Ha a daganat jól differenciált, és ismert, hogy progeszteron- és ösztrogénreceptorokkal rendelkezik, akkor a progesztinek alkalmazhatók a kezelésben. Nincs bizonyíték arra, hogy az újonnan diagnosztizált endometriális rákos műtét mellett a progesztagén alkalmazását alátámasztanák. Az áttétes endometrioid rákok körülbelül 25% -a reagál a progesztinekre. Ezenkívül az endometrium stróma szarkómái hormonális szerekkel, például tamoxifennel, hidroxiprogeszteron -kaproáttal , letrozollal , megesztrol -acetáttal és medroxiprogeszteronnal kezelhetők . Ez a kezelés hatékony a méhnyálkahártya sztrómás szarkómáiban, mivel jellemzően ösztrogén- és/vagy progesztinreceptorokkal rendelkeznek . A progesztin receptorok tumorszuppresszorokként működnek az endometrium rákos sejtjeiben. Az előzetes kutatások és klinikai vizsgálatok kimutatták, hogy ezek a kezelések magas metasztatikus betegségek esetén is nagy választ adnak.
2010 -ben a hormonterápia tisztázatlan hatású az előrehaladott vagy visszatérő méhnyálkahártya -rákos betegeknél. Nincs elegendő bizonyíték a hormonpótló terápiát fontolóra vevő nők tájékoztatására az endometriális rák kezelése után.
Célzott terápia
A Dostarlimabot az FDA jóváhagyta az endometrium rák specifikus biomarkerrel történő kezelésére
Monitoring
A CA-125 daganatjelző gyakran emelkedett endometriális rák esetén, és felhasználható a kezelésre adott válasz nyomon követésére, különösen savós sejtrák vagy előrehaladott betegség esetén. Időszakos MRI -t vagy CT -vizsgálatot javasolnak előrehaladott betegség esetén, és a nőknek, akiknek kórelőzményében méhnyálkahártya -rák szerepel, gyakrabban kell medencevizsgálatot végezni a kezelést követő öt évben. A három -négy havonta végzett vizsgálatokat a kezelés utáni első két évben, a következő három évben pedig félévente ajánlják.
Az endometriumrákban szenvedő nőknek nem szabad rutinszerű felügyeleti képalkotást végezniük a rák megfigyelésére, kivéve, ha új tünetek jelennek meg, vagy a daganatjelzők emelkedni kezdenek. Az ilyen jelzések nélküli képalkotás nem ajánlott, mert nem valószínű, hogy kiújulást észlel vagy javítja a túlélést, és mert saját költségei és mellékhatásai vannak. Ismétlődés gyanúja esetén PET/CT vizsgálat javasolt.
Prognózis
Túlélési arányok
| Színpad | 5 éves túlélési arány |
|---|---|
| IA | 88% |
| IB | 75% |
| II | 69% |
| III-A | 58% |
| III-B | 50% |
| III-C | 47% |
| IV-A | 17% |
| IV-B | 15% |
Az endometrium adenokarcinóma ötéves túlélési aránya megfelelő kezelés után 80%. A legtöbb nő, 70%feletti, rendelkezik a FIGO I. stádiumú rákjával, amely a legjobb prognózissal rendelkezik. A III. És különösen a IV. Stádiumú rákok rosszabb prognózisúak, de ezek viszonylag ritkák, csak az esetek 13% -ában fordulnak elő. A III – IV. Stádiumú endometriális rák átlagos túlélési ideje kilenc -tíz hónap. Az idősebb kor rosszabb prognózist jelez. Az Egyesült Államokban a fehér nők magasabb túlélési arányt mutatnak, mint a fekete nők, akik hajlamosak a betegség agresszívabb formáinak kialakulására a diagnózisuk idejére. A magas progeszteronreceptor -expressziós daganatok jó prognózissal rendelkeznek az alacsony progeszteron -receptor -expressziós daganatokhoz képest; A magas progeszteronreceptor -betegségben szenvedő nők 93% -a három évig élte túl, míg az alacsony progeszteron -receptor betegségben szenvedő nők 36% -a. A szívbetegség a leggyakoribb halálok azok között, akik túlélik az endometriális rákot, és más elhízással kapcsolatos egészségügyi problémák is gyakoriak. A diagnózist követően az életminőség pozitív kapcsolatban áll az egészséges életmóddal is (nincs elhízás, jó minőségű étrend, fizikai aktivitás).
Ismétlődési arányok
A korai stádiumú endometriális rák kiújulása 3-17%között mozog, az elsődleges és az adjuváns kezeléstől függően. A legtöbb kiújulás (75–80%) a medencén kívül fordul elő, és a legtöbb a kezelés két -három évében jelentkezik - 64% két éven belül és 87% három éven belül.
A magasabb stádiumú rákok nagyobb valószínűséggel ismétlődnek meg, akárcsak azok, amelyek behatoltak a myometriumba vagy a méhnyakba, vagy áttétet adtak a nyirokrendszerbe. A papilláris savós karcinóma , a tiszta sejtes karcinóma és az endometrioid karcinóma azok az altípusok, amelyeknél a legnagyobb a kiújulás kockázata. A magas fokú szövettani altípusok is fokozottan ki vannak téve a kiújulás kockázatának.
A kiújulás leggyakoribb helye a hüvelyben van ; az endometriális rák hüvelyi visszaesései a legjobb prognózissal rendelkeznek. Ha a sugárzással nem kezelt daganatból kiújul a betegség, az EBRT az első vonalbeli kezelés, és gyakran sikeres. Ha a sugárzással kezelt rák megismétlődik, a kismedencei extervenció az egyetlen lehetőség a gyógyító kezelésre. Palliatív kemoterápiát, citoreduktív műtétet és sugárzást is végeznek. Sugárkezelés (VBT és EBRT) helyi hüvelyi kiújulás esetén 50% -os ötéves túlélési arányt mutat. A kismedencei kiújulásokat műtéttel és sugárzással kezelik, a hasi recidívákat sugárzással és lehetőség szerint kemoterápiával kezelik. További gyakori kiújulási helyek a kismedencei nyirokcsomók, para-aorta nyirokcsomók, hashártya (a kiújulások 28%-a) és a tüdő, bár az agyban (<1%), a májban (7%), a mellékvesékben ( 1%), csontok (4–7%; jellemzően az axiális csontváz ), a hason kívüli nyirokcsomók (0,4–1%), a lép és az izom/lágyrészek (2–6%).
Járványtan
2014 -ig évente körülbelül 320 000 nőt diagnosztizálnak méhnyálkahártya -rákos megbetegedéssel világszerte, és 76 000 hal meg, ami a hatodik leggyakoribb rák a nők körében. Gyakrabban fordul elő a fejlett országokban, ahol az endometriális rák kockázata a nők életében 1,6%, míg a fejlődő országokban 0,6%. A fejlett országokban évente 100 000 nőből 12,9 -nél fordul elő .
Az Egyesült Államokban a méhnyálkahártya rák a leggyakrabban diagnosztizált nőgyógyászati rák, nőknél pedig a negyedik leggyakoribb rák, amely a nők összes rákos megbetegedésének 6% -át teszi ki. Ebben az országban 2014 -re becslések szerint évente 52 630 nőt diagnosztizáltak, és 8590 -en halnak meg a betegségben. Észak -Európában, Kelet -Európában és Észak -Amerikában a legmagasabb az endometriális rák aránya, míg Afrikában és Nyugat -Ázsiában a legalacsonyabb. 2012 -ben Ázsiában a világ endometriumrákjának 41% -át diagnosztizálták, míg Észak -Európa, Kelet -Európa és Észak -Amerika együtt a diagnózisok 48% -át tette ki. A rákos megbetegedések többségével ellentétben az új esetek száma nőtt az elmúlt években, beleértve az Egyesült Királyságban több mint 40% -os növekedést 1993 és 2013 között. Ennek a növekedésnek egy része a fejlett országokban tapasztalható elhízási arányok növekedésének köszönhető, a várakozások és az alacsonyabb születési arány. Az endometriális rák átlagos életkori kockázata körülbelül 2-3% a méhben szenvedők körében. Az Egyesült Királyságban évente körülbelül 7400 esetet diagnosztizálnak, az EU -ban pedig körülbelül 88 000 esetet.
Az endometriális rák leggyakrabban a perimenopauza idején (a közvetlenül a menopauza előtti, az azt követő időszakban és alatt), 50 és 65 éves kor között jelentkezik; összességében az endometriális rák 75% -a a menopauza után jelentkezik. A 40 évnél fiatalabb nők teszik ki az endometrium rákos esetek 5% -át, és az esetek 10-15% -a 50 év alatti nőknél fordul elő. Ebben a korcsoportban fennáll a petefészekrák kialakulásának kockázata. A diagnózis átlagos életkora világszerte 63 év; az Egyesült Államokban, az átlagos életkor a diagnózis 60 éves. A fehér amerikai nőknél nagyobb a kockázata az endometriális ráknak, mint a fekete amerikai nőknek, 2,88% és 1,69% élethosszig tartó kockázatuk van. A japán-amerikai nők és az amerikai latina nők aránya alacsonyabb, a bennszülött hawaii nőké pedig magasabb.
Kutatás
Számos kísérleti terápia létezik az endometrium rák kezelésére, beleértve az immunológiai, hormonális és kemoterápiás kezeléseket. Trastuzumabot (Herceptin), a Her2 fehérje elleni antitestet használtak olyan rákos megbetegedésekben, amelyekről ismert, hogy pozitívak a Her2/neu onkogénre, de a kutatás még folyamatban van. Immunológiai terápiákat is vizsgálnak, különösen a méh papilláris szerózus karcinómájában.
A rákokat genetikai technikákkal (beleértve a DNS -szekvenálást és az immunhisztokémiát ) lehet elemezni annak megállapítására, hogy a mutált génekre specifikus terápiák alkalmazhatók -e a kezelésre. A PARP -gátlókat az endometrium rák PTEN -mutációkkal való kezelésére használják, különösen olyan mutációk esetén, amelyek csökkentik a PTEN expresszióját. Az endometriális rák ellen aktív PARP -gátló az olaparib . A 2010 -es évektől folynak a kutatások ezen a területen.
Folyamatos kutatások folynak a metformin , cukorbetegség elleni gyógyszer alkalmazásáról endometrium -rákos elhízott nőknél a műtét előtt. A korai kutatások kimutatták, hogy hatékonyan lassítja a rákos sejtek proliferációját. Előzetes kutatások kimutatták, hogy a preoperatív metformin beadása csökkentheti a tumor markerek expresszióját. A metformin hosszú távú alkalmazása nem bizonyítottan megelőző hatással van a rák kialakulására, de javíthatja az általános túlélést.
A temszirolimuszt , az mTOR gátlót potenciális kezelésként vizsgálják. A kutatások azt mutatják, hogy az mTOR inhibitorok különösen hatékonyak lehetnek a PTEN mutációkkal rendelkező rákos megbetegedéseknél. A ridaforolimuszt (deforolimuszt) is kutatják olyan betegek kezelésére, akik korábban részesültek kemoterápiában. Az előzetes kutatások ígéretesek voltak, és 2013 -ra befejeződött a ridaforolimusz II. Stádiumú vizsgálata. Kutatásokat végeztek a visszatérő endometriumrák kombinált ridaforolimusz/progesztin -kezelésével kapcsolatban is. A bevacizumabot és a tirozin -kináz inhibitorokat , amelyek gátolják az angiogenezist , kutatják, mint lehetséges kezelési módszereket az endometriális rákoknak, amelyek magas vaszkuláris endoteliális növekedési faktorral rendelkeznek . Az ixabepilont vizsgálják, mint lehetséges kemoterápiát előrehaladott vagy visszatérő endometriális rák kezelésére. A ritka, magas fokú, differenciálatlan endometrium-szarkóma kezelését vizsgálják, mivel ennek a betegségnek még nincs kialakított ellátási standardja. A kemoterápiák közé tartozik a doxorubicin és az ifoszfamid .
Kutatások is folynak több olyan génről és biomarkerről , amelyek kapcsolódhatnak az endometrium rákhoz. A kombinált orális fogamzásgátlók és az IUD védőhatását vizsgálják. Előzetes kutatások kimutatták, hogy az egy évre elhelyezett levonorgesztrel spirál, havi 6 havi gonadotropin-felszabadító hormon injekcióval kombinálva megállíthatja vagy megfordíthatja az endometrium rák előrehaladását fiatal nőknél; kifejezetten komplex atipikus hiperplázia, azonban az eredmények nem voltak meggyőzőek. Egy kísérleti gyógyszert, amely egyesíti a hormont a doxorubicinnel, szintén vizsgálják a hormonreceptorokkal rendelkező rákos megbetegedések nagyobb hatékonysága érdekében. Az emlőrák kezelésében hatékony hormonterápiát, beleértve az aromatázgátlók alkalmazását , szintén vizsgálják az endometriális rák kezelésére. Az egyik ilyen gyógyszer az anasztrozol , amelyet jelenleg a kemoterápia utáni hormon-pozitív kiújulásokban kutatnak. Folyamatban van az endometrium stróma szarkóma hormonális kezeléseinek kutatása is. Ez magában foglalja olyan gyógyszerek vizsgálatát, mint a mifepriszton , egy progesztin antagonista, valamint az aminoglutetimid és a letrozol, két aromatáz inhibitor.
Folytatódik a kutatás az endometriális rák kimutatására és stádiumozására szolgáló legjobb képalkotó módszerre. A sebészetben a kutatások kimutatták, hogy a teljes kismedencei limfadenektómia és a méheltávolítás az első stádiumú endometriális rákban nem javítja a túlélést, és növeli a negatív mellékhatások, köztük a nyiroködéma kockázatát. Más kutatások azt vizsgálják, hogy lehet -e azonosítani az őrszem nyirokcsomóit biopsziához, ha a daganatot infravörös fényben ragyogó festékkel fecskendezik be . Az intenzitás modulált sugárterápiát jelenleg vizsgálják, és néhány központban már alkalmazzák endometriális rák kezelésére, a hagyományos sugárterápia mellékhatásainak csökkentésére. Megismétlődésének kockázatát még nem számszerűsítették. Folyamatban vannak a hyperbarikus oxigénterápiával kapcsolatos kutatások is a mellékhatások csökkentése érdekében. 2014 végén várták az adjuváns sugárkezelést kemoterápiával kombináló PORTEC 3 vizsgálat eredményeit.
Nincs elegendő bizonyíték annak megállapítására, hogy az endometriális rákos betegek részesülnek -e további magatartási és életmódbeli beavatkozásokból, amelyek célja a túlsúly csökkentése.
Történelem és kultúra
A méhnyálkahártya -daganat gyakorisága ellenére nem ismert széles körben a lakosság körében. A tünetek tudatossága alacsony, ami későbbi diagnózishoz és rosszabb túléléshez vezethet.
Hivatkozások
Külső linkek
| Osztályozás | |
|---|---|
| Külső erőforrások |