Thymus - Thymus
| Thymus | |
|---|---|
 Thymus
| |
|
A csecsemőmirigy működésének magyarázata
| |
| Részletek | |
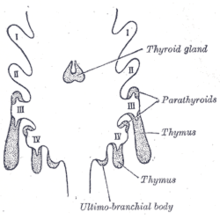
| Prekurzor | Harmadik garat tasak |
| Rendszer | Nyirokrendszer , az immunrendszer része |
| Nyirok | tracheobronchialis , parasternalis |
| Funkció | Támogatja a funkcionális T -sejtek fejlődését |
| Azonosítók | |
| latin | Thymus |
| Háló | D013950 |
| TA98 | A13.1.02.001 |
| TA2 | 5152 |
| FMA | 9607 |
| Anatómiai terminológia | |
A csecsemőmirigy az immunrendszer speciális primer nyirokszerve . Belül a csecsemőmirigy, csecsemőmirigy sejt limfociták vagy T-sejtek érett. A T -sejtek kulcsfontosságúak az adaptív immunrendszer számára , ahol a szervezet kifejezetten alkalmazkodik az idegen betolakodókhoz. A csecsemőmirigy a mellkas felső elülső részében, az elülső felső mediastinumban , a szegycsont mögött és a szív előtt helyezkedik el . Két lebenyből áll, mindegyik egy központi medullából és egy külső kéregből áll, amelyet egy kapszula vesz körül.
A csecsemőmirigy alkotja az éretlen T-sejtek nevezett timociták , valamint a bélés sejteket nevezik hámsejtek , amelyek segítik a timociták fejleszteni. A sikeresen kifejlődő T -sejtek megfelelően reagálnak a test MHC immunreceptorával ( pozitív szelekciónak nevezik ), és nem a test fehérjéivel szemben ( negatív szelekció ). A csecsemőmirigy a legnagyobb és legaktívabb az újszülött és a serdülőkorban. A korai tizenéves korban a csecsemőmirigy mérete és aktivitása csökkenni kezd, és a csecsemőmirigy szövetét fokozatosan zsírszövet váltja fel . Ennek ellenére bizonyos T -sejtek fejlődése a felnőtt élet során is folytatódik.
A csecsemőmirigy rendellenességei a T -sejtek és az autoimmun betegségek, például az 1. típusú autoimmun polyendokrin szindróma és a myasthenia gravis csökkenéséhez vezethetnek . Ezek gyakran társul rákos szövet a csecsemőmirigy, úgynevezett thymoma , vagy szöveteket származó éretlen limfocitákat, mint például T-sejtek, az úgynevezett limfóma . A csecsemőmirigy eltávolítását tymectomiának nevezik . Bár a csecsemőmirigyet az ókori görögök óta a test részeként azonosították, csak a hatvanas évektől vált világosabbá a csecsemőmirigy funkciója az immunrendszerben.
Szerkezet
A csecsemőmirigy olyan szerv, amely a mellkas felső részén, a szegycsont alatt helyezkedik el , felfelé nyúlik a nyak felé. Gyermekeknél a csecsemőmirigy rózsaszínes-szürke, puha és felszíni lebenyes. Születésekor körülbelül 4–6 cm hosszú, 2,5–5 cm széles és körülbelül 1 cm vastag. Mérete nő a pubertásig, ahol mérete körülbelül 40-50 g lehet, ezt követően pedig az involúció néven ismert folyamatban csökken .
A csecsemőmirigy két lebenyből áll, amelyek a felső középvonalban találkoznak, és a pajzsmirigy aljától a nyakon húzódnak, egészen a negyedik borda porcáig. A lebenyeket egy kapszula borítja. A csecsemőmirigy alatt fekszik a szegycsont, nyugszik a szívburkot , és elválasztjuk a aortaív és nagy hajók egy réteg fascia . A bal brachiocephalica véna akár a csecsemőmirigybe is beágyazódhat. A nyak, hogy fekszik az elején és oldalán a légcső mögött sternohyoid és sternothyroid izmokat .
Mikroanatómia
A csecsemőmirigy két lebenyből áll, amelyek középen egyesülnek, és egy kapszula veszi körül, amely az erekkel a belső térbe nyúlik. A lebeny sejtekben gazdag külső kéregből és egy kevésbé sűrű belső velőből áll . A lebenyek vannak osztva kisebb lebenykékben 0.5-2mm átmérőjű, amelyek között extrudálni sugárzó inszerciókat a kapszulából mentén szeptum .
A kéreg főleg timocitákból és hámsejtekből áll. A timocitákat, az éretlen T-sejteket a finoman elágazó hámos retikuláris sejtek hálózata támogatja , amely folyamatos a medulla hasonló hálózattal. Ez a hálózat adventitiát képez az erekben, amelyek a kéregben a medulával való találkozás közelében lévő septákon keresztül lépnek be a kéregbe. Más sejtek is jelen vannak a csecsemőmirigyben, beleértve a makrofágokat , a dendritikus sejteket és kis mennyiségű B -sejtet , neutrofilt és eozinofilt .
A velőben a hámsejtek hálózata durvább, mint a kéregben, és a nyiroksejtek száma viszonylag kevesebb. Koncentrikus, fészkeszerű testek, amelyeket Hassall -testeknek (más néven thymus -testeknek) neveznek , a velős hámsejtek aggregációi képezik. Ezek koncentrikus, réteges hámsejtek, amelyek száma az élet során növekszik. Ezek a hámcsövek maradványai, amelyek az embrió harmadik garatzsákjából nőnek ki, hogy a csecsemőmirigyet képezzék.
Mikrográf a csecsemőmirigy lebenyét mutatja. A kéreg (mélyebb lila terület) körülvesz egy kevésbé sűrű és világosabb medullát.
Vér- és idegellátás
A csecsemőmirigyet ellátó artériák a belső mellkasi és alsó pajzsmirigy -artériák ágai, néha a felső pajzsmirigy -ágból származó ágak láthatók. Az ágak elérik a csecsemőmirigyet, és a kapszula szeptumával együtt a kéreg és a velő közötti területre utaznak, ahol belépnek a csecsemőmirigybe; vagy alternatívaként közvetlenül adja be a kapszulát.
A csecsemőmirigy vénái a bal brachiocephalica vénában , a belső mellkasi vénában és a pajzsmirigy alsó vénájában végződnek . Néha az erek közvetlenül a felső vena cava -ban végződnek.
A nyirokerek csak a csecsemőmirigytől távol, az artériákat és a vénákat kísérik. Ezek a brachiocephalic, tracheobronchialis és parasternalis nyirokcsomókba kerülnek .
A csecsemőmirigyet tápláló idegek a vagus idegből és a nyaki szimpatikus láncból származnak . A phrenicus idegek ágai elérik a csecsemőmirigy kapszuláját, de nem lépnek be a csecsemőmirigybe.
Variáció
A két lebeny mérete kissé eltér, a bal lebeny általában magasabb, mint a jobb. A csecsemőmirigy szövete a mirigyen vagy annak környékén, esetenként a pajzsmirigyben található. A csecsemőmirigy gyermekeknél változóan nyúlik felfelé, néha a pajzsmirigyig.
Fejlődés
A timociták és a csecsemőmirigy hámja eltérő fejlődési eredetű. Először a csecsemőmirigy hámja fejlődik ki, és a harmadik garatzsák két kinövéseként jelenik meg, az egyik mindkét oldalon . Néha magában foglalja a negyedik garat tasakot is. Ezek kinyúlnak és hátra a környező mezodermából és idegtaréj -eredetű mesenchyma előtt a ventrális aorta . Itt a timociták és a hám találkozik és kötődik a kötőszövethez. Az egyes divertikulumok garatnyílása hamarosan eltűnik, de a lombik nyaka egy ideig sejtzsinórként megmarad. A lombikot bélelő sejtek további szaporodásával sejtek rügyei keletkeznek, amelyeket a behatoló mezoderma körülvesz és elkülönít.
A hám finom lebenyeket képez, és szivacsszerű struktúrává fejlődik. Ebben a szakaszban vérképző csontvelő-prekurzorok vándorolnak a csecsemőmirigybe. A normális fejlődés az epithelium és a hematopoietikus timociták közötti kölcsönhatástól függ . A jód szükséges a csecsemőmirigy fejlődéséhez és tevékenységéhez is.
Komplikáltság
A csecsemőmirigy a szülés után tovább növekszik, és a pubertás korig eléri a relatív maximális méretet. A magzat és az újszülött életében a legaktívabb . A pubertáskor 20-50 grammra nő. Ezután csökken a mérete és aktivitása a thymus involúciónak nevezett folyamatban . Az első életév után a termelt T -sejtek mennyisége csökkenni kezd. A zsír és a kötőszövet kitölti a thymus térfogatának egy részét. Az involúció során a csecsemőmirigy mérete és aktivitása csökken. A zsírsejtek születéskor jelen vannak, de méretük és számuk jelentősen megnő a pubertás után, először a lobulák közötti falakból, majd a kéregbe és a velőbe hatolnak be a mirigybe. Ez a folyamat idős korban is folytatódik, ahol akár mikroszkóppal, akár emberi szemmel a tímusz nehezen észlelhető, bár jellemzően 5–15 gramm súlyú.
Az atrófiát a nemi hormonok keringő szintjének növekedése okozza , és egy felnőtt kémiai vagy fizikai kasztrációja a csecsemőmirigy méretének és aktivitásának növekedését eredményezi. Súlyos betegség vagy humán immunhiányos vírusfertőzés is okozhat involúciót.
Funkció
T -sejtek érése
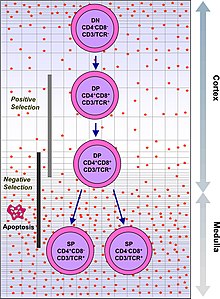
A csecsemőmirigy elősegíti a T-sejtek érését , amely az immunrendszer fontos része, amely sejtközvetített immunitást biztosít . A T-sejtek vérképző prekurzorként kezdődnek a csontvelőből, és a csecsemőmirigybe vándorolnak, ahol timocitáknak nevezik őket . A csecsemőmirigyben érési folyamaton mennek keresztül, amelynek során biztosítják, hogy a sejtek reagáljanak az antigénekkel szemben ("pozitív szelekció"), de nem reagálnak a testszöveten található antigének ellen ("negatív szelekció"). Az érés után a T -sejtek kivándorolnak a csecsemőmirigyből, hogy létfontosságú funkciókat biztosítsanak az immunrendszerben.
Minden T -sejtnek van egy külön T -sejt -receptora , amely megfelel egy adott anyagnak, az antigénnek . A legtöbb T -sejt -receptor kötődik a test sejtjein található fő hisztokompatibilitási komplexhez . Az MHC antigént mutat be a T -sejt receptornak, amely akkor válik aktívvá, ha megfelel a specifikus T -sejt -receptornak. Annak érdekében, hogy megfelelően működjön, az érett T -sejtnek képesnek kell lennie kötődni az MHC -molekulához ("pozitív szelekció"), és nem reagálnia a test szöveteiből származó antigénekkel szemben ("negatív szelekció"). A pozitív szelekció a kéregben, a negatív szelekció a csecsemőmirigy medullájában következik be. Ezt követően a túlélő T-sejtek elhagyják a csecsemőmirigyet, amelyet szfingozin-1-foszfát szabályoz . A további érés a perifériás keringésben történik. Néhány ilyen van, mert a hormonok és a citokinek által kiválasztott sejtek a csecsemőmirigy, beleértve thymulin , thymopoietin és thymosinra .
Pozitív választék
A T -sejteknek külön T -sejt -receptoraik vannak. Ezeket a különálló receptorokat az RAG1 és RAG2 gének által stimulált V (D) J rekombinációs gén -átrendeződés folyamatával hozzák létre . Ez a folyamat hibára hajlamos, és egyes timociták nem képesek működőképes T-sejt-receptorokat előállítani, míg más timociták T-sejt-receptorokat hoznak létre, amelyek autoreaktívak. Ha funkcionális T -sejt -receptor képződik, a timocita egyidejűleg elkezdi expresszálni a CD4 és CD8 sejtfelszíni fehérjéket .
A T -sejt túlélése és jellege attól függ, hogy milyen kölcsönhatásban van a környező thymicus hámsejtekkel. Itt a T -sejt receptor kölcsönhatásba lép a hámsejtek felszínén lévő MHC molekulákkal. Az olyan sejtek, amelyekben a receptor nem reagál vagy gyengén reagál, apoptózis következtében elpusztulnak . Az a sejt, amely reagál, túléli és szaporodik. Egy érett T -sejt csak a CD4 -et vagy a CD8 -at fejezi ki, de nem mindkettőt. Ez a kötődés erősségétől függ a TCR és az MHC 1. vagy 2. osztálya között. egy T -sejt -receptor, amely többnyire a II. osztályú MHC -hez kötődik, hajlamos CD4 -pozitív T -sejt termelésére.
Negatív kiválasztás
A szervezet saját fehérjéit megtámadó T -sejtek a csecsemőmirigyben eliminálódnak, az úgynevezett "negatív szelekció". A velőhártya hámsejtjei és a csecsemőmirigy dendritikus sejtjei a test más részeiből származó főbb fehérjéket fejeznek ki. Az ezt stimuláló gén az AIRE . A saját antigénekre erősen reagáló timociták nem élnek túl, és apoptózis következtében elpusztulnak. Egyes CD4 pozitív T -sejtek, amelyeket saját antigéneknek tettek ki, T -szabályozó sejtekként maradnak fenn .
Klinikai jelentőség
Immunhiány
Mivel a csecsemőmirigy fejlődik ki a T -sejtekben, a csecsemőmirigy fejlődésével kapcsolatos veleszületett problémák immunhiányhoz vezethetnek , akár a csecsemőmirigy fejlődésének problémája, akár a timocita -fejlődésre jellemző probléma miatt. Az immunhiány mélyreható lehet. A csecsemőmirigy korai életkorban történő elvesztése genetikai mutáció révén (mint például a DiGeorge -szindróma , a CHARGE -szindróma vagy egy nagyon ritka "meztelen csecsemőmirigy, amely a haj és a csecsemőmirigy hiányát okozza) súlyos immunhiányt és ezt követően nagy érzékenységet okoz a vírusok, protozoonok által okozott fertőzéseknek , és gombák . Csupasz egereket a nagyon ritka „meztelen” hiányosság következtében FoxN1 mutációs törzs kutatási egerek mint egy modell a T-sejt-hiány.
A csecsemőmirigy-immunhiány leggyakoribb veleszületett oka a 22. kromoszóma , a DiGeorge-szindróma törlése . Ennek eredményeként a harmadik és a negyedik garat tasak fejlődése meghiúsul, ami a csecsemőmirigy fejlődésének meghiúsulását eredményezi, és egyéb kapcsolódó problémákat, például veleszületett szívbetegséget és szájüregi rendellenességeket (például szájpadhasadékot és ajakhasadékot ), a mellékpajzsmirigyek fejlődésének sikertelensége , valamint a légcső és a nyelőcső közötti fistula jelenléte . Nagyon kicsi a keringő T -sejtek száma. Az állapotot fluoreszcens in situ hibridizációval diagnosztizálják, és thymus transzplantációval kezelik .
A súlyos kombinált immunhiány (SCID) a ritka veleszületett genetikai betegségek csoportja, amelyek kombinált T-, B- és NK -sejtek hiányát eredményezhetik. Ezeket a szindrómákat olyan mutációk okozzák, amelyek befolyásolják a vérképző progenitor sejtek érését , amelyek mind a B, mind a T -sejtek prekurzorai. Számos genetikai hiba okozhat SCID-t, beleértve az IL-2 receptor gén funkcióvesztését, és mutációt, amely az adenin-deamináz enzim hiányát eredményezi .
Autoimmun betegség
Autoimmun poli -endokrin szindróma
Az 1. típusú autoimmun polyendokrin szindróma egy ritka genetikai autoimmun szindróma, amely a csecsemőmirigy -szövetek genetikai hibájából ered. Pontosabban, a betegség az autoimmun szabályozó (AIRE) gén hibáiból ered , amely stimulálja az önantigének expresszióját a csecsemőmirigy hámsejtjeiben. Ennek az állapotnak a hibái miatt az önantigének nem expresszálódnak, így T -sejtek keletkeznek, amelyek nem kondicionálják a test szöveteinek elviselését, és idegenként kezelhetik őket, stimulálva az immunválaszt és autoimmunitást eredményezve. Emberek APECED fejleszteni egy autoimmun betegség, amely hatással van több endokrin szövetekben, az általában érintett szervek pedig hypothyreosis a pajzsmirigy , Addison-kór , a mellékvesék és candida fertőzés a test felületek, beleértve a belső bélés a száj és a körmök miatt a TH17 -sejtek diszfunkciójához , és a tünetek gyakran gyermekkorban kezdődnek. Sok más autoimmun betegség is előfordulhat. A kezelés az érintett szervekre irányul.
Thymoma-asszociált multiorgan autoimmunitás
Thymoma-asszociált multiorgan autoimmunitás fordulhat elő thymoma-ban szenvedő embereknél. Ebben az állapotban a csecsemőmirigyben kifejlődött T -sejtek a test szövetei ellen irányulnak. Ennek oka az, hogy a rosszindulatú csecsemőmirigy nem képes megfelelően nevelni a fejlődő timocitákat az önreaktív T-sejtek eltávolítására. Az állapot gyakorlatilag megkülönböztethetetlen a graft versus host betegségtől .
Myasthenia gravis
A myasthenia gravis egy autoimmun betegség, amely leggyakrabban az acetilkolin -receptorokat blokkoló antitesteknek köszönhető, amelyek részt vesznek az idegek és az izmok közötti jelátvitelben . Gyakran thymus -hiperpláziával vagy thymoma -val társul, valószínűleg az abnormálisan fejlődő T -sejtek miatt termelt antitestekkel. A myasthenia gravis leggyakrabban fiatal és középkorú korban alakul ki, ami az izommozgások könnyű fáradtságát okozza. A vizsgálatok közé tartozik az antitestek kimutatása (például acetilkolin-receptorok vagy izom-specifikus kináz ellen ), valamint a CT-vizsgálat a thymoma vagy a thymektomia kimutatására. Ami a csecsemőmirigyet illeti, a csecsemőmirigy eltávolítása, az úgynevezett thymectomia , kezelésnek tekinthető, különösen akkor, ha thymoma található. Más kezelések közé tartozik az acetilkolin hatásának időtartamának növelése idegszinapszisoknál a bomlás sebességének csökkentésével. Ezt acetil -kolinészteráz inhibitorok , például piridosztigmin gátolják .
Rák
Thymomas
A tímusz hámsejtekből származó daganatokat thymomáknak nevezik . Leggyakrabban 40 évnél idősebb felnőtteknél fordulnak elő. A daganatokat általában akkor észlelik, ha tüneteket okoznak, például nyaktömeget vagy hatással vannak a közeli struktúrákra, például a felső vena cava -ra ; a myasthenia gravisban szenvedő betegek szűrése miatt észlelték, ami erős kapcsolatban áll a thymomákkal és a hiperpláziával; és véletlenszerű megállapításként észlelték a képalkotás során, mint például a mellkasröntgen . A hiperplázia és a csecsemőmirigyből származó daganatok más autoimmun betegségekkel - például hypogammaglobulinemiával , Graves -betegséggel , tiszta vörösvérsejt -aplasiával , vészes vérszegénységgel és dermatomyositisszel - társulnak , valószínűleg a proliferáló T -sejtek negatív szelekciójának hibái miatt.
A thymomas jóindulatú lehet; jóindulatú, de a terjeszkedésnek köszönhetően, a tímusz kapszuláján túl („invazív pajzsmirigy”), vagy rosszindulatú ( karcinóma ). Ez a besorolás a sejtek megjelenésén alapul. A WHO besorolása is létezik, de nem használják a szokásos klinikai gyakorlat részeként. A csecsemőmirigyre korlátozódó jóindulatú daganatok a leggyakoribbak; amelyet lokálisan invazív daganatok, majd karcinómák követnek. A jelentésekben eltérések vannak, egyes források szerint a rosszindulatú daganatok gyakoribbak. Az invazív daganatok, bár technikailag nem rosszindulatúak, továbbra is terjedhetnek ( áttét ) a test más területein. Annak ellenére, hogy a thymomas hámsejtekben fordul elő, thymocytákat is tartalmazhatnak. A thymomas kezelése gyakran műtétet igényel a teljes thymus eltávolítására. Ez a kapcsolódó autoimmun állapotok átmeneti remisszióját is eredményezheti.
Limfómák
A csecsemőmirigy T -sejtjeiből származó daganatok az akut limfoblasztos leukémia (ALL) részhalmazát alkotják . Ezek tünetekben, vizsgálati megközelítésben és kezelésben hasonlóak az ALL más formáihoz. Az ALL egyéb formáihoz hasonlóan kialakuló tünetek a vérlemezkék hiányára vonatkoznak , ami zúzódást vagy vérzést okoz; immunszuppresszió, amely fertőzéseket okoz; vagy a sejtek által a testrészekbe történő beszivárgás, ami megnagyobbodott májat , lépet , nyirokcsomókat vagy más helyeket eredményez. A vérvizsgálat nagy mennyiségű fehérvérsejtet vagy limfoblasztokat , valamint más sejtvonalak hiányát - például alacsony vérlemezkeszámot vagy vérszegénységet - fedezheti fel . Az immunofenotipizálás feltárja azokat a sejteket, amelyek CD3 , a T -sejteken található fehérje, és segít tovább megkülönböztetni a T -sejtek érettségét. A genetikai elemzés, beleértve a kariotipizálást is, feltárhat olyan specifikus rendellenességeket, amelyek befolyásolhatják a prognózist vagy a kezelést, például a Philadelphia transzlokációt . A kezelés magában foglalhat több kemoterápiás tanfolyamot , őssejt -transzplantációt és a kapcsolódó problémák kezelését, például a fertőzések antibiotikumokkal történő kezelését és a vérátömlesztést . Nagyon magas a fehérvérsejtszám is megkövetelheti cytoreduction a aferezisben .
A csecsemőmirigyben található B -sejtek kis populációjából származó daganatok primer mediastinalis (thymus) nagy B -sejtes limfómákhoz vezetnek . Ezek a Non-Hodgkins limfóma ritka altípusai , bár a gének aktivitása és esetenként mikroszkopikus alakja miatt szokatlanul a Hodgkins limfómák jellemzőivel is rendelkeznek . amelyek leggyakrabban fiatal és középkorúaknál fordulnak elő, nőstényeknél. Leggyakrabban, amikor tünetek jelentkeznek, a csecsemőmirigy közelében lévő struktúrák, például a felső vena cava vagy a felső légutak összenyomódása okozza ; amikor a nyirokcsomók érintettek, gyakran a mediastinum és a nyaki csoportokban találhatók. Az ilyen daganatokat gyakran biopsziával észlelik, amely immunhisztokémiai vizsgálatnak van alávetve . Ez megmutatja a differenciálódási klaszterek jelenlétét , a sejtfelszíni fehérjék - nevezetesen a CD30 , CD19 , CD20 és CD22 , valamint a CD15 hiányát . Más markerek is használhatók a diagnózis megerősítésére. A kezelés általában magában foglalja a tipikus CHOP vagy EPOCH vagy más kezelési rendeket; rendszerint általában ciklofoszfamidot , antraciklint , prednizont és más kemoterápiás szereket ; és potenciálisan őssejt -transzplantáció is .
Tímusz ciszták
A csecsemőmirigy cisztákat tartalmazhat, általában 4 cm -nél kisebb átmérővel. A thymus cisztákat általában véletlenül észlelik, és általában nem okoznak tüneteket. Tímusz ciszták fordulhatnak elő a nyak mentén vagy a mellkasban ( mediastinum ). A ciszták általában csak folyadékot tartalmaznak, és sok réteg lapos sejt vagy oszlop alakú sejt borítja őket . Ennek ellenére a ciszta jelenléte hasonló problémákat okozhat, mint a thymomáké, a közeli struktúrák összenyomásával, és egyesek érintkezhetnek a belső falakkal ( szeptumok ), és nehéz megkülönböztetni őket a daganattól. Amikor cisztákat találnak, a vizsgálat magában foglalhatja a daganatok feldolgozását, amely magában foglalhatja a ciszta gyanúja szerinti terület CT vagy MRI vizsgálatát .
Sebészeti eltávolítás
A thymectomia a csecsemőmirigy sebészeti eltávolítása. Az eltávolítás szokásos oka az, hogy hozzáférjenek a szívhez, hogy műtétet végezzenek a veleszületett szívhibák kijavítására az újszülött korban. A thymektomia egyéb indikációi közé tartozik a thymomas eltávolítása és a myasthenia gravis kezelése. Újszülötteknél a csecsemőmirigy relatív mérete akadályozza a szív és a környező erek sebészeti bejutását. A csecsemőmirigy eltávolítása csecsemőkorban gyakran végzetes immunhiányt eredményez, mivel a funkcionális T -sejtek nem fejlődtek ki. Idősebb gyermekeknél és felnőtteknél, akiknek működő nyirokrendszere van, és érett T -sejtek is találhatók más nyirokszervekben, a hatás csökken, és az új antigének elleni immunválasz hiányának korlátozására korlátozódik.
Társadalom és kultúra
Ha emberi táplálékként használják, az állatok csecsemőmirigyét az édeskenyér egyik fajtájaként ismerik .
Történelem
A csecsemőmirigyet az ókori görögök ismerték , és elnevezése a görög θυμός ( thumos ) szóból származik , ami "haragot" vagy "szívet, lelket, vágyat, életet" jelent, valószínűleg a mellkasban, az érzelmek közelében szubjektíven érződnek; vagy pedig a név a kakukkfű gyógynövényből származik (szintén görögül θύμος vagy θυμάρι ), amely a "szemölcsös exreszcencia" neve lett, valószínűleg a kakukkfűhöz való hasonlóság miatt.
Galen volt az első, aki megjegyezte, hogy a szerv mérete az ember életében változott.
A XIX. Században a thymicolymphaticus állapotát állapították meg, amelyet a nyirokszövet növekedése és a tímusz megnagyobbodása határozott meg. Azt hitték, hogy a hirtelen csecsemőhalál -szindróma oka, de mára elavult kifejezés.
A csecsemőmirigy fontosságát az immunrendszerben 1961 -ben fedezte fel Jacques Miller , egynapos egerek műtéti eltávolításával, és megfigyelve az ezt követő hiányt egy limfocita -populációban, amelyet később a T -sejteknek neveztek el származási szervük után. Immunológiai szerepének felfedezéséig a csecsemőmirigyet „evolúciós balesetként”, funkcionális jelentőség nélkül elutasították. A csecsemőmirigy szerepe abban, hogy az érett T -sejtek tolerálják a test szöveteit, 1962 -ben derült ki, azzal a megállapítással, hogy az egerekben átültetett csecsemőmirigy T -sejtjei toleranciát mutattak a donor egér szöveteivel szemben. A B -sejteket és a T -sejteket 1968 -ban különböző típusú limfocitákként azonosították, és megértették azt a tényt, hogy a T -sejteknek a csecsemőmirigyben kell érlelniük. A T -sejtek altípusait (CD8 és CD4) 1975 -re azonosították. A T -sejtek ezen alosztályainak érési módja - az MHC -receptorokhoz funkcionálisan kötődő sejtek pozitív kiválasztása - a kilencvenes évekre ismert volt. Az AIRE gén fontos szerepét és a negatív szelekció szerepét az autoreaktív T -sejtek érésének megakadályozásában 1994 -ben megértették.
Az utóbbi időben az immunológia fejlődése lehetővé tette a csecsemőmirigy T-sejtek érésében betöltött funkciójának teljesebb megértését.
Más állatok
A csecsemőmirigy minden állkapcsos gerincesben megtalálható , ahol az életkorral azonos zsugorodáson megy keresztül, és ugyanolyan immunológiai funkciót lát el, mint más gerinceseknél. A közelmúltban, 2011-ben egy különálló csecsemőmirigy-szerű nyirok-hám szerkezetet fedeztek fel , amelyet timoidnak neveznek , a lárva lámpás kopoltyúiban . A Hagfish -nak prototymusja van, amely a garat velarizmaihoz kapcsolódik, és amely különböző immunválaszokért felelős .
A csecsemőmirigy a legtöbb más gerincesben is megtalálható, hasonló szerkezetű és funkciójú, mint az emberi csecsemőmirigy. A nyak második csecsemőmirigyéről néha beszámoltak az egerekben. Mint az embereknél, a tengerimalac csecsemőmirigye természetesen sorvad, amikor az állat eléri a felnőttkort, de a sportos szőrtelen tengerimalac (amely spontán laboratóriumi mutációból származik) nem rendelkezik a csecsemőmirigy -szövetet, és a szervüreget cisztikus terek helyettesítik .
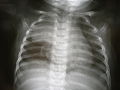
További képek
A mellkas röntgenfelvételén a csecsemőmirigy sugárzástömegű (ezen a képen világosabb) tömegként jelenik meg a gyermek jobb (képen bal) tüdő felső lebenyében.
Hivatkozások
![]() Ez a cikk a Gray's Anatomy (1918) 20. kiadásának 1273. oldaláról származó, nyilvánosan hozzáférhető szöveget tartalmazza.
Ez a cikk a Gray's Anatomy (1918) 20. kiadásának 1273. oldaláról származó, nyilvánosan hozzáférhető szöveget tartalmazza.
Könyvek
- Ralston SH, Penman ID, Strachan MW, Hobson RP, szerk. (2018). Davidson elvei és gyakorlata az orvostudományban (23. kiadás). Elsevier. ISBN 978-0-7020-7028-0.
- Kasper D, Fauci A, Hauser S, Longo D, Jameson J, Loscalzo J (2015). Harrison belgyógyászati alapelvei (19. kiadás). McGraw-Hill Professional. ISBN 9780071802154.
Külső linkek
- T -sejtek fejlődése a csecsemőmirigyben. Videó: Janice Yau, leírva a stromális jelzést és a toleranciát. A Torontói Egyetem Immunológiai és Biomedikai Kommunikációs Tanszéke. Masters Research Project, Biomedical Communications Master of Science. 2011.