Nukleáris antitest - Anti-nuclear antibody
Az antinukleáris antitestek ( ANA-k , más néven antinukleáris faktor vagy ANF ) olyan autoantitestek, amelyek kötődnek a sejtmag tartalmához . Normális egyénekben az immunrendszer idegen fehérjék ( antigének ) ellen termel antitesteket , emberi humán fehérjék ( autoantigének ) ellen azonban nem . Bizonyos esetekben antitestek termelődnek humán antigének ellen.
Az ANA-knak számos altípusa létezik, például anti-Ro antitestek , anti-La antitestek , anti-Sm antitestek , anti-nRNP antitestek , anti-Scl-70 antitestek , anti-dsDNS antitestek , anti-hiszton antitestek , antitestek a magpórus-komplexek számára , anti-centromer antitestek és anti-sp100 antitestek . Ezen antitest-altípusok mindegyike a mag különböző fehérjéihez vagy fehérjekomplexeihez kötődik. Számos rendellenességben megtalálhatók, beleértve az autoimmunitást , a rákot és a fertőzést , az antitestek előfordulása az állapottól függően eltérő. Ez lehetővé teszi az ANA-k alkalmazását néhány autoimmun rendellenesség, köztük a szisztémás lupus erythematosus , a Sjögren-szindróma , a scleroderma , a vegyes kötőszöveti betegségek , a polimiozitisz , a dermatomiozitisz , az autoimmun hepatitis és a gyógyszer által kiváltott lupus diagnosztizálásában .
Az ANA teszt kimutatja az egyén vérszérumában jelen lévő autoantitesteket . Az ANA-k kimutatására és mennyiségi meghatározására használt közös tesztek a közvetett immunfluoreszcencia és az enzimhez kapcsolt immunszorbens vizsgálat (ELISA). Immunfluoreszcens- szintje autoantitestek jelenteni titer . Ez a szérum legnagyobb hígítása, amelynél az autoantitestek még mindig kimutathatók. Az 1: 160 vagy annál nagyobb hígítású pozitív autoantitest titrokat általában klinikailag szignifikánsnak tekintik. Az 1: 160-nál kisebb pozitív titer az egészséges populáció 20% -ánál van, különösen az időseknél. Bár az 1: 160 vagy annál magasabb pozitív titer erősen összefügg az autoimmun rendellenességekkel, az egészséges egyének 5% -ában is megtalálható. Az autoantitest-szűrés hasznos az autoimmun rendellenességek diagnosztizálásában, és a szintek monitorozása segít megjósolni a betegség progresszióját. A pozitív ANA-teszt ritkán hasznos, ha a diagnózist alátámasztó egyéb klinikai vagy laboratóriumi adatok nincsenek.
Immunitás és autoimmunitás
Az emberi testnek számos védekezési mechanizmusa van a kórokozókkal szemben , az egyik a humorális immunitás . Ez a védekező mechanizmus antitesteket (nagy glikoproteineket ) termel immunreakcióra adott válaszként. Ehhez a folyamathoz számos immunrendszeri sejtre van szükség, beleértve a limfocitákat ( T-sejtek és B-sejtek ) és az antigént bemutató sejteket . Ezek a sejtek koordinálják az immunválaszt az idegen fehérjék ( antigének ) kimutatásakor , és antitesteket termelnek, amelyek kötődnek ezekhez az antigénekhez. A normál fiziológiában az emberi fehérjéket ( autoantigéneket ) felismerő limfociták vagy programozott sejthalálon ( apoptózis ) mennek keresztül, vagy működésképtelenné válnak. Ez az ön tolerancia azt jelenti, hogy a limfocitáknak nem szabad immunválaszt gerjeszteniük az emberi sejt antigének ellen. Néha azonban ez a folyamat meghibásodik és antitestek termelődnek az emberi antigének ellen, ami autoimmun betegséghez vezethet.
ANA altípusok
Az ANA-k számos rendellenességben, valamint néhány egészséges egyénben találhatók. Ilyen rendellenességek közé tartoznak: szisztémás lupus erythematosus (SLE), a reumás arthritis , Sjögren-szindróma , szkleroderma , polimiozitisz , dermatomiozitisz , primer biliaris cirrhosis , gyógyszer által indukált lupusz , autoimmun hepatitisz , sclerosis multiplex , discoid lupus , pajzsmirigy betegség , antifoszfolipid szindróma , fiatalkori idiopátiás arthritis , pszoriázisos ízületi gyulladás , juvenilis dermatomiozitisz , idiopátiás thrombocytopaeniás purpura , fertőzés és rák . Ezek az antitestek specifitásuk szerint feloszthatók, és mindegyik alcsoportnak más a hajlama a specifikus rendellenességekre.
Kihúzható nukleáris antigének
A kivonható nukleáris antigének (ENA) az autoantigének egy csoportja , amelyeket eredetileg antitest célpontként azonosítottak autoimmun rendellenességekben szenvedőknél. ENA-nak hívják, mert sóoldattal kivonhatók a sejtmagból. Az ENA-k ribonukleoproteinekből és nem hiszton fehérjékből állnak, amelyeket vagy a szérum prototípusát szolgáltató donor nevével (Sm, Ro, La, Jo), vagy annak a betegségnek a nevével nevezzük el, amelyben az antitesteket találták (SS- A, SS-B, Scl-70).
Anti-Ro / SS-A és anti-La / SS-B

Az anti-Ro és anti-La antitestek, más néven SS-A és SS-B, általában megtalálhatók a primer Sjögren-szindrómában , egy autoimmun rendellenességben, amely befolyásolja az exokrin mirigyeket . Mindkét antitest jelenléte a Sjögren-szindróma 30–60% -ában, egyedül anti-Ro antitestek találhatók a Sjögren-szindróma 50–70% -ában és az SLE 30% -ában bőrelvonással, és az anti-La antitestek elszigetelten ritkán . Az SLE-ben anti-La antitestek is találhatók; azonban általában Sjögren-szindróma is jelen van. Az anti-Ro antitestek ritkábban fordulnak elő egyéb rendellenességekben is, beleértve az autoimmun májbetegségeket, a lisztérzékenységet , az autoimmun reumás betegségeket, a szív újszülöttkori lupus erythematosust és a polymyositist . Terhesség alatt az anti-Ro antitestek átjuthatnak a placentán, és szívblokkot és újszülött lupuszt okozhatnak a csecsemőknél. A Sjögren-szindrómában az anti-Ro és anti-La antitestek korrelálnak a korai megjelenéssel, a betegség megnövekedett időtartamával, a parotid mirigy megnagyobbodásával, a mirigyen kívüli betegséggel és a mirigyek limfociták általi beszűrésével. Az anti-Ro antitestek specifikusak az Ro-RNP komplex komponenseire, amelyek 45 kDa, 52 kDa, 54 kDa és 60 kDa fehérjéket és RNS-t tartalmaznak . A 60 kDa DNS / RNS kötő fehérje és az 52 kDa T-sejt szabályozó fehérje az anti-Ro antitestek legjellemzőbb antigénje. Ezek a fehérjék együttesen egy ribonukleoprotein (RNP) komplex részét képezik, amelyek asszociálódnak a hY1-hY5 hyRNS-ekkel. A La antigén az RNS-polimeráz III 48 kDa méretű transzkripciós terminációs tényezője , amely asszociálódik az Ro-RNP komplexhez.
Az antitesttermelés mechanizmusa a Sjögren-szindrómában nem teljesen ismert, de az apoptózis (programozott sejthalál) és a molekuláris mimika szerepet játszhat. A Ro és La antigének az apoptózison áteső sejtek felszínén expresszálódnak, és az immunrendszer sejtjeivel kölcsönhatásban gyulladást okozhatnak a nyálmirigyben. Az antitestek molekuláris utánzással is előállíthatók, ahol keresztreaktív antitestek kötődnek mind a vírushoz, mind az emberi fehérjékhez. Ez előfordulhat az egyik antigénnel, Ro vagy La, és ezután epitóp-terjesztésként ismert eljárás révén antitesteket termelhet más fehérjék ellen . A retrovírusos gag fehérje hasonlóságot mutat a La fehérjével, és a Sjögren-szindróma molekuláris utánzásának lehetséges példájaként szerepel.
Anti-Sm
Az anti-Smith (Anti-Sm) antitestek nagyon specifikus markerek az SLE számára. Az SLE nélküli egyének körülbelül 99% -ában hiányoznak az anti-Sm antitestek, de az SLE-ben szenvedők csak 20% -ában vannak antitestek. Az SLE-ben központi idegrendszeri érintettséggel, vesebetegséggel , tüdőfibrózissal és pericarditisszel társulnak, de nem járnak betegség aktivitással. Az anti-Sm antitestek antigénjei a kis nukleáris ribonukleoproteinek (snRNP-k) magegységei, A-tól G-ig nevezik őket, és az U1, U2, U4, U5 és U6 snRNP-hez kötődnek. Leggyakrabban az antitestek specifikusak a B, B 'és D egységekre. Molekuláris és epidemiológiai vizsgálatok arra utalnak, hogy az anti-Sm antitesteket molekuláris utánzás indukálhatja, mivel a fehérje némi hasonlóságot mutat az Epstein-Barr vírus fehérjéivel.
Anti-nRNP / anti-U1-RNP
Az anti-nukleáris ribonukleoprotein (anti-nRNP) antitestek , más néven anti-U1-RNP antitestek az SLE 30–40% -ában találhatók. Gyakran előfordulnak anti-Sm antitesteknél, de különböző klinikai asszociációkkal társulhatnak. Az SLE mellett ezek az antitestek nagymértékben társulnak a vegyes kötőszöveti betegségekkel . Az anti-nRNP antitestek felismerik az snRNP-k A és C magegységeit, és emiatt elsősorban az U1-snRNP-hez kötődnek. Az RNP-re adott immunválasz oka lehet, hogy a sejtkomponensek apoptotikus vérző részekben jelennek meg a sejtmembránon. Molekuláris utánzást is javasoltak ezeknek a fehérjéknek az antitestek előállítására szolgáló lehetséges mechanizmusként, az U1-RNP polipeptidek és az Epstein-Barr vírus polipeptidek közötti hasonlóság miatt.
Anti-Scl-70 / anti-topoizomeráz I
Az anti-Scl-70 antitestek kapcsolódnak a szklerodermához . Az antitestek szkleroderma iránti érzékenysége megközelítőleg 34%, de magasabb a diffúz bőrelvonás esetén (40%), és alacsonyabb a korlátozott bőrelvonás esetén (10%). Az antitestek specificitása 98% és 99,6% más reumatikus betegségekben, illetve normál egyénekben. A szkleroderma mellett ezek az antitestek az SLE-ben szenvedő személyek körülbelül 5% -ában találhatók. A antigén célpont, az anti-Scl-70 antitestek topoizomeráz I .
Anti-Jo-1
Noha az anti-Jo-1 antitestek gyakran szerepelnek az ANA-kban, valójában a citoplazmatikus fehérje, a Histidyl-tRNS szintetáz - a hisztidinnel töltött tRNS szintéziséhez nélkülözhetetlen aminoacil-tRNS szintetáz - antitestek . Nagyon kapcsolódnak a polimiozitiszhez és a dermatomiozitiszhez , más kötőszöveti betegségeknél ritkán fordulnak elő. A polimiozitisz körülbelül 20–40% -a pozitív a Jo-1 antitestekre, és a legtöbbnek interstitialis tüdőbetegsége, HLA-DR3 és HLA-DRw52 humán leukocita antigén (HLA) markerei lesznek ; együttesen Jo-1 szindróma néven ismert.
Anti-dsDNS
Az anti-kettős szálú DNS (anti-dsDNS) antitestek erősen társulnak az SLE-hez. Nagyon specifikus markerek a betegségre, néhány tanulmány közel 100% -ot idéz. Az érzékenységre vonatkozó adatok 25 és 85% között mozognak. Az anti-dsDNS antitest szintek, amelyek titrként ismertek, korrelálnak a betegség aktivitásával az SLE-ben; a magas szint aktívabb lupusra utal. Az anti-dsDNS antitestek jelenléte a lupus nephritishez is kapcsolódik, és bizonyítékok vannak ezek okára. Egyes anti-dsDNS antitestek keresztreaktívak a vese glomeruláris bazális membránján (GBM) található más antigénekkel , mint például a heparán-szulfát , a kollagén IV, a fibronektin és a laminin . Ezeknek az antigéneknek a kötése a vesében gyulladást és komplement rögzülést okozhat , ami vesekárosodást okozhat. Kimutatták, hogy a magas DNS-kötő és alacsony C3 szint jelenléte rendkívül magas prediktív értékkel rendelkezik (94%) az SLE diagnosztizálásához. Az is lehetséges, hogy az anti-dsDNS antitesteket a sejtek internalizálják, amikor megkötik a membránantigéneket, majd megjelenítik a sejtfelszínen. Ez elősegítheti a vese T-sejtjeinek gyulladásos reakcióit. Fontos megjegyezni, hogy nem minden anti-dsDNS antitest társul lupus nephritisrel, és más tényezők is okozhatják ezt a tünetet távollétükben. Az anti-dsDNS antitestek antigénje kettős szálú DNS .
Hisztonellenes antitestek
Az anti-hiszton antitestek a gyógyszer által indukált lupusban szenvedők 75–95% -ában és az idiopátiás SLE 75% -ában találhatók a szérumban . Az SLE-ben található anti-dsDNS antitestekkel ellentétben ezek az antitestek nem rögzítik a komplementet. Bár leggyakrabban a gyógyszer által kiváltott lupusban fordulnak elő, SLE, scleroderma , rheumatoid arthritis és differenciálatlan kötőszöveti megbetegedések bizonyos eseteiben is megtalálhatók . Sok gyógyszerről ismert, hogy gyógyszer által indukált lupuszt okoznak, és a nukleoszómában különféle antigén célpontokat produkálnak, amelyek gyakran keresztreaktívak számos hiszton fehérjével és DNS-sel. A prokainamid a gyógyszer által kiváltott lupus egy olyan formáját okozza, amely antitesteket termel a hiszton H2A és H2B komplex ellen.
Anti-gp210 és anti-p62
Az anti-glikoprotein-210 (anti-gp210) és az anti-nukleoporin 62 (anti-p62) antitestek egyaránt antitestek a magmembrán komponenseivel szemben, és megtalálhatók a primer biliaris cirrhosisban (PBC). Minden antitest a PBC körülbelül 25–30% -ában van jelen. Mindkét antitest antigénje a magmembrán alkotóeleme . A gp210 egy 200 kDa fehérje, amely részt vesz a sejtmag pórusának a magmembránhoz való rögzítésében . A p62 antigén egy 60 kDa méretű magpórus-komplex.
Anti-centromer antitestek
Az anti-centromer antitestek korlátozott kután szisztémás szklerózissal, más néven CREST szindrómával , primer biliaris cirrhosissal és proximális szklerodermával járnak. Hat ismert antigén van, amelyek mind a centromérhoz kapcsolódnak ; CENP-A – CENP-F. A CENP-A egy 17 kDa-os hiszton H3- szerű fehérje. A CENP-B egy 80 kDa méretű DNS-kötő fehérje, amely részt vesz a heterokromatin hajtogatásában . CENP-C egy 140kDa fehérje részt vesz a kinetochor szerelvény. A CENP-D egy 50 kDa fehérje, amelynek funkciója ismeretlen, de homológ lehet egy másik, a kromatin kondenzációjában szerepet játszó fehérjével , az RCC1-gyel . A CENP-E a kinezin motoros fehérje családból származó 312 kDa fehérje . A CENP-F a magmátrix 367 kDa-os fehérje, amely a késői G2 fázisban lévő kinetochore-val társul a mitózis során. A CENP-A, B és C antitestek leggyakrabban megtalálhatók (a szisztémás szklerózis 16–42% -a), és Raynaud-jelenséggel, telangiectasiákkal , tüdő érintettséggel és a szisztémás szklerózis korai megjelenésével társulnak .
Anti-sp100
Az anti-sp100 antitestek a primer biliaris cirrhosis (PBC) körülbelül 20–30% -ában találhatók . Kevés PBC nélküli egyénben találhatók meg, ezért a betegség nagyon specifikus markerei. Az sp100 antigén a nukleáris testekben található meg; nagy fehérje komplexek a magban, amelyek szerepet játszhatnak a sejtek növekedésében és differenciálódásában.
Anti-PM-Scl
Az anti-PM-Scl antitestek a polimiozitisz / szisztémás szklerózis (PM / SSc) átfedési szindróma legfeljebb 50% -ában találhatók . A vérszérumban jelen lévő antitestekkel rendelkező személyek körülbelül 80% -ánál jelentkezik a rendellenesség. Az antitestek jelenléte a PM / SSc átfedési szindróma korlátozott kutánus érintettségéhez kapcsolódik. A antigén célpontok az antitestek komponensei RNS -feldolgozási exoszóma komplex a nukleoláris . Tíz fehérje van ebben a komplexben, és ezek közül nyolc ellenanyag különböző frekvencián található; PM / Scl-100 (70–80%), PM / Scl-75 (46–80%), hRrp4 (50%), hRrp42 (21%), hRrp46 (18%), hCr14 (14%), hRrp41 ( 10%) és hRrp40 (7%).
Anti-DFS70 antitestek
Az anti-DFS70 antitestek sűrű, finom foltos mintázatot generálnak a közvetett immunfluoreszcenciában, és normális körülmények között és különféle körülmények között találhatók meg, de nem kapcsolódnak szisztémás autoimmun patológiához. Ezért felhasználhatók az ilyen állapotok kizárására ANA-pozitív egyéneknél. A betegek jelentős részén szisztémás lupus erythematosust vagy differenciálatlan kötőszöveti betegséget diagnosztizálnak, nagyrészt pozitív ANA alapján. Abban az esetben, ha meghatározott autoantitest nem mutatható ki (pl. Anti-ENA antitestek), a diagnózis igazolásához anti-DFS70 antitestek tesztelése ajánlott. Az anti-DFS70 antitest tesztek CE jelöléssel ellátott tesztekként állnak rendelkezésre. Eddig nem áll rendelkezésre az FDA által jóváhagyott vizsgálat.
ANA teszt

Az ANA-k jelenléte a vérben szűrővizsgálattal igazolható. Bár számos teszt létezik az ANA kimutatására, a szűréshez használt leggyakoribb tesztek a közvetett immunfluoreszcencia és az enzimmel kapcsolt immunszorbens teszt (ELISA). Az ANA-k kimutatását követően különféle altípusokat határoznak meg.
Közvetett immunfluoreszcencia
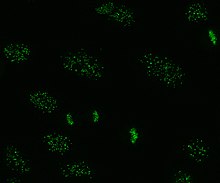
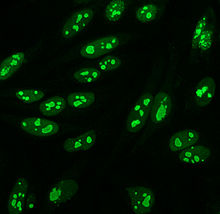
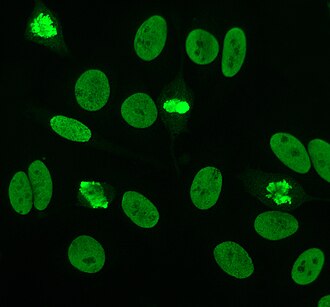
A közvetett immunfluoreszcencia az ANA-k egyik leggyakrabban használt tesztje. Jellemzően HEp-2 sejteket alkalmaznak szubsztrátként az antitestek kimutatására az emberi szérumban. A mikroszkóp tárgylemezeket HEp-2 sejtekkel vonjuk be, és a szérumot a sejtekkel inkubáljuk. Ha az említett és megcélzott antitestek jelen vannak, akkor a sejtek antigénjeihez kötődnek ; ANA-k esetében az antitestek a maghoz kötődnek. Ezeket fluoreszcens jelzésű (általában FITC vagy rodopsin B) anti-humán antitest hozzáadásával lehet láthatóvá tenni , amely az antitestekhez kötődik. A molekula akkor fog fluoreszkálni, ha egy meghatározott hullámhosszú fény világít rá, amely a mikroszkóp alatt látható. Az emberi szérumban jelenlévő antitesttől és az antigén sejtben való elhelyezkedésétől függően a fluoreszcencia különféle mintázatai láthatók a HEp-2 sejteken. Az antitestek szintjét a vérszérum hígításával elemezzük. Az ANA-teszt akkor tekinthető pozitívnak, ha fluoreszcencia látható 1: 40/1: 80 titer mellett. A magasabb titer klinikailag szignifikánsabb, mivel alacsony pozitív (≤1: 160) az egészséges egyének, különösen az idősek, legfeljebb 20% -ánál fordul elő. Az egészséges populációnak csak körülbelül 5% -ánál 1: 160 vagy annál magasabb az ANA-titer.
HEp-2
Egészen 1975 körül, a HEp-2 sejtek bejuttatásáig állati szövetet használtak az immunfluoreszcencia standard szubsztrátjaként. A HEp-2 sejtek jelenleg az ANA immunfluoreszcens detektálásának egyik leggyakoribb szubsztrátja.
Eredetileg egy gégekarcinóma-törzs volt a kezdője, a sejtvonalat HeLa- sejtek szennyezték és kiszorították , és mára tényleges HeLa- sejtként azonosították.
Ezek jobbak, mint a korábban használt állati szövetek, mert a nagy méretű és a magas aránya mitózis (sejtosztódás) a sejtvonalban . Ez lehetővé teszi a mitózis-specifikus antigének, például a centromer antitestek elleni antitestek kimutatását. Lehetővé teszik az anti-Ro antitestek azonosítását is, mivel az acetont használják a sejtek rögzítésére (más fixáló szerek képesek lemosni az antigént).
A HEp-2 sejteken számos magfestési minta látható: homogén, foltos, nukleoláris, maghártyás, centromerikus, magpontos és pleomorf. A homogén mintázat akkor látható, amikor a kondenzált kromoszómák és az interfázisú kromatin festődnek. Ez a minta az anti-dsDNS antitestekkel , a nukleoszomális komponensekkel szembeni antitestekkel és az anti-hiszton antitestekkel társul . Két pettyes minta létezik: finom és durva. A finom pettyes minta finom magfestést mutat festetlen metafázisú kromatinnal, amely anti-Ro és anti-La antitestekkel társul. A durva festési mintázat durva szemcsés magfestéssel rendelkezik, amelyet anti-U1-RNP és anti-Sm antitestek okoznak. A nukleoláris festési mintázat számos antitesthez kapcsolódik, beleértve az anti-Scl-70, anti-PM-Scl, anti-fibrillarint és anti-Th / To-t. A sejtmembrán festése fluoreszcens gyűrűként jelenik meg a sejtmag körül, és anti-gp210 és anti-p62 antitestek termelik. A centromer mintázat mutatja Több nukleáris pontok az interfázisban és a mitotikus sejtek, amely megfelel a kromoszómák számát a sejtben. A nukleáris pontmintázatok 13-25 magpontot mutatnak az interfázisú sejtekben, és anti- sp100 antitestek termelik őket . A pleomorf mintázatot a szaporodó sejtmag antigén elleni antitestek okozzák . Kimutatták, hogy a közvetett immunfluoreszcencia kissé jobb az ELISA-hoz képest az ANA kimutatásában HEp-2 sejtekből.
Crithidia luciliae
Crithidia luciliae vannak haemoflaggelate egysejtű egysejtűek . Szubsztrátként használják az immunfluoreszcenciában az anti-dsDNS antitestek kimutatására. A kinetoplaszt néven ismert organellával rendelkeznek,amely egy nagy mitokondrium , összekapcsolódó kör alakú dsDNS-molekulák hálózatával. Anti-dsDNS antitesteket és fluoreszcensen jelölt anti-humán antitesteket tartalmazó szérummal végzett inkubálás után a kinetoplaszt fluoreszkálni fog. A többi nukleáris antigén hiánya ebben az organellában azt jelenti, hogy a C.luciliae alkalmazása szubsztrátként lehetővé teszi az anti-dsDNS antitestek specifikus kimutatását.
ELISA
Enzimhez kapcsolt immunszorbens vizsgálat (ELISA) antigénnel bevont mikrotiter lemezeket használ az ANA kimutatására. A mikrotiterlemez minden üregét egyetlen antigénnel vagy több antigénnel vonjuk be a specifikus antitestek kimutatására vagy az ANA-k szűrésére. Az antigének vagy sejtkivonatokból származnak, vagy rekombinánsak. A vérszérumot a lemez üregeiben inkubáljuk és kimossuk. Ha antigénhez kötődő antitestek vannak jelen, azok mosás után is megmaradnak. Egy enzimhez, például torma-peroxidázhoz konjugált másodlagos anti-humán antitestet adunk hozzá. Az enzimreakció az oldat színváltozását eredményezi, amely arányos az antigénhez kötött antitest mennyiségével. Jelentős különbségek vannak az ANA kimutatásában immunfluoreszcenciával és különböző ELISA kitekkel, és ezek között csak marginális egyetértés van. A klinikusnak ismernie kell a különbségeket a különféle vizsgálatok eredményeinek értékelése érdekében.
Érzékenység
Az alábbi táblázat a különböző típusú ANA-k érzékenységét sorolja fel a különböző betegségekre.
| ANA típus | Cél antigén | Érzékenység (%) | ||||||
|---|---|---|---|---|---|---|---|---|
| SLE | Kábítószer-indukált LE | Diffúz szisztémás szklerózis | Korlátozott szisztémás szkleroderma | Sjögren-szindróma | Gyulladásos myopathia | MCTD | ||
| Minden ANA (közvetett IF-vel ) |
Különféle | 95 | 100 | 80 | 80 | 70 | 40–60 | 95 |
| Anti-dsDNS | DNS | 60 | - | - | - | 30 | - | - |
| Anti-Sm | Az snRNP-k magfehérjéi | 40 | - | - | - | - | - | - |
| Hisztonellenes | Hisztonok | 60 | 90 | - | - | - | - | - |
| Anti Scl-70 | I. típusú topoizomeráz | - | - | 20 | 10. | - | - | - |
| Centroméria-ellenes | Centromer fehérjék | - | - | 30 | 80 | - | - | - |
| SS-A (Ro) | RNP-k | 40 | - | - | - | 50 | 10. | - |
| SS-B (La) | RNP-k | 10–15 | - | - | - | 60–90 | - | |
| - = kevesebb, mint 5% érzékenység | ||||||||
Néhány ANA többféle betegségben jelenik meg, ami a teszt alacsonyabb specificitását eredményezi. Például kimutatták, hogy az IgM- reumatoid faktor (IgM-RF) keresztreakciót mutat az ANA-val, hamisan pozitív immunfluoreszcenciát eredményezve . Pozitív ANA, valamint anti-DNS antitestekről számoltak be autoimmun pajzsmirigy betegségben . Az ANA pozitív eredményt adhat autoimmun pajzsmirigybetegségben vagy reumás ízületi gyulladásban szenvedők 45% -ánál, valamint HIV-vel vagy hepatitis C-ben szenvedők 15% -ánál . Az Amerikai Lupus Alapítvány szerint "az általános népesség körülbelül 5% -ának pozitív ANA-ja lesz. Azonban a pozitív ANA-val rendelkező emberek legalább 95% -ának nincs lupusza. Pozitív ANA-teszt néha futhat a családokban, akkor is, ha a családtagoknak nincs bizonyítékuk a lupusra. " Másrészről azt mondják, bár a lupusban ténylegesen szenvedő betegek 95% -a ANA-pozitív, "Csak kis százalékban van negatív ANA, és sokukban vannak más antitestek (például anti-foszfolipid antitestek , anti-anti-antitestek) . Ro, anti-SSA) vagy ANA-juk pozitívról negatívra vált szteroidok , citotoxikus gyógyszerek vagy urémia (veseelégtelenség) hatására. "
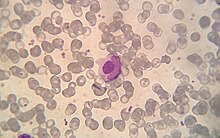
Történelem
Az LE sejtet a csontvelőben fedezték fel 1948-ban Hargraves et al. 1957-ben Holborow és mtsai. először mutatta be az ANA-t közvetett immunfluoreszcencia alkalmazásával. Ez volt az első jel arra, hogy a sejtmagot befolyásoló folyamatok felelősek az SLE-ért. 1959-ben kiderült, hogy az SLE-ben szenvedő egyének széruma olyan antitesteket tartalmaz, amelyek kicsapódnak a magok sóoldat-kivonataival, amelyek kivonható nukleáris antigének (ENA) néven ismertek . Ez az ENA antigének és a hozzájuk tartozó antitestek jellemzéséhez vezetett. Így anti-Sm és anti-RNP antitesteket fedeztek fel 1966-ban, illetve 1971-ben. Az 1970-es években felfedezték az anti-Ro / anti-SS-A és anti-La / anti-SS-B antitesteket. Az Scl-70 antitestről 1979-ben ismert volt, hogy a szkleroderma ellen specifikus antitest, azonban az antigént (topoizomeráz-I) csak 1986-ban jellemezték. A Jo-1 antigént és antitestet 1980-ban jellemezték.
Lásd még
Hivatkozások
Külső linkek
- Autoimmunitásblog - HEp-2 ANA összefoglaló
- Antinukleáris + antitestek az Egyesült Államok Országos Orvostudományi Könyvtárában Medical Subject Headings (MeSH)
- Greidinger, Eric L .; Hoffman, DO; Robert W. (2003. január 31.). "CE frissítés [kémia | immunológia]: Antinukleáris antitest tesztelés: módszerek, indikációk és értelmezés" . Laboratóriumi orvoslás . 34 (2): 113–117. doi : 10.1309 / VUB90VTPMEWV3W0F .