TAAR1 - TAAR1
| TAAR1 | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Azonosítók | |||||||||||||||||||||||||
| Álnevek | A TAAR1 , TA1, TAR1, TRAR1, nyomaminasszociált receptort 1, Trace amin receptor | ||||||||||||||||||||||||
| Külső azonosítók | OMIM : 609333 MGI : 2148258 HomoloGene : 24938 GeneCards : TAAR1 | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Ortológusok | |||||||||||||||||||||||||
| Faj | Emberi | Egér | |||||||||||||||||||||||
| Entrez | |||||||||||||||||||||||||
| Ensembl | |||||||||||||||||||||||||
| UniProt | |||||||||||||||||||||||||
| RefSeq (mRNS) | |||||||||||||||||||||||||
| RefSeq (fehérje) | |||||||||||||||||||||||||
| Helyszín (UCSC) | Kr. 6: 132,64 - 132,66 Mb | nincs | |||||||||||||||||||||||
| PubMed keresés | |||||||||||||||||||||||||
| Wikidata | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
A nyomkövető amin-asszociált receptor 1 ( TAAR1 ) egy nyomelemhez kapcsolódó receptor (TAAR) fehérje , amelyet emberben a TAAR1 gén kódol . TAAR1 egy intracelluláris amin -aktivált G s -kapcsolt és G q -kapcsolt G-fehérjéhez kapcsolt receptor (GPCR), amely elsősorban a kifejezett számos környéki szervekben és sejtekben (pl, a gyomor , a vékonybél , duodenum , és a fehér vérsejtek ) , asztrociták , és az intracelluláris miliőben a központi idegrendszerben (CNS) található monoamin neuronok preszinaptikus plazmamembránjában (azaz axon terminálisában ). A TAAR1 -et 2001 -ben fedezte fel két független vizsgálócsoport, Borowski et al. és Bunzow et al. A TAAR1 egyike a hat funkcionális humán nyomelemmel társított receptornak , amelyek így nevezték el, hogy képesek megkötni a szövetekben nyomokban koncentrációban előforduló endogén aminokat. TAAR1 játszik jelentős szerepet szabályozásában ingerületátvitel a dopamin , norepinefrin és szerotonin neuronok a központi idegrendszer; különböző mechanizmusokon keresztül befolyásolja az immunrendszert és a neuroimmun rendszer működését is.
A TAAR1 egy nagy affinitású receptor az amfetamin , metamfetamin , dopamin és nyomelemek számára, amelyek közvetítik egyes sejthatásaikat a központi idegrendszer monoamin neuronjaiban .
A humán TAAR1 (hTAAR1) receptor elsődleges endogén ligandumai a hatásfok rangsorában a következők:
tiramin > β-fenetilamin > dopamin = oktopamin .
Felfedezés
A TAAR1 -et Borowski et al. és Bunzow et al. 2001-ben Ahhoz, hogy megtalálják a genetikai variánsok felelős TAAR1 szintézis, használtak keverékei oligonukleotidok szekvenciákkal kapcsolatos G-proteinnel kapcsolt receptorok (GPCR-ek) a szerotonin és a dopamin felfedezni új DNS-szekvenciák a patkány genomiális DNS és a cDNS-t , amelyet aztán amplifikált és klónoztak. A kapott szekvencia egyetlen adatbázisban sem található, és TAAR1 kódolású. Később Raul Gainetdinov és munkatársai tanulmányozták a TAAR1 és más, e családból származó receptorok funkcionális szerepét .
Szerkezet
A TAAR1 szerkezeti hasonlóságot mutat az A osztályú rodopszin GPCR alcsaláddal . 7 transzmembrán doménnel rendelkezik, rövid N és C terminális kiterjesztéssel. A TAAR1 62–96% -ban azonos a TAARs2-15-tel, ami arra utal, hogy a TAAR alcsalád nemrégiben alakult ki ; ugyanakkor a TAAR1 ortológok közötti alacsony hasonlóság azt sugallja, hogy gyorsan fejlődnek. TAAR1 osztja prediktív peptid motívum minden más Taars. Ez a motívum átfedésben van a transzmembrán VII doménnel, és azonossága NSXXNPXX [Y, H] XXX [Y, F] XWF. A TAAR1 és homológjai ligandum zsebvektorokkal rendelkeznek , amelyek 35 aminosavból álló készletet használnak fel , amelyekről ismert, hogy közvetlenül részt vesznek a receptor-ligandum kölcsönhatásban.
Gén
Minden humán TAAR gén egyetlen kromoszómán helyezkedik el, amely a kb. 109 kb -s humán 6q23.1 kromoszómát, 192 kb méretű 10A4 egér kromoszómát és 216 kb patkány 1p12 kromoszómát tartalmaz. Mindegyik TAAR származik egyetlen exon , kivéve a TAAR2 , amely a kódolt két exon. Úgy gondolják, hogy a humán TAAR1 gén intron nélküli gén.
Szöveteloszlás
A mai napig a TAAR1 -et öt különböző emlős genomban azonosították és klónoztak : ember, egér, patkány, majom és csimpánz . Patkányokban a TAAR1 mRNS -je alacsony vagy közepes szinten található a perifériás szövetekben, például a gyomorban , a vesében , a belekben és a tüdőben , és alacsony az agyban . A Rhesus majom Taar1 és a humán TAAR1 nagy szekvencia -hasonlóságot mutat, és a TAAR1 mRNS erősen expresszálódik mindkét faj ugyanazon fontos monoaminerg régióiban . Ezek a régiók közé tartozik a dorsalis és a ventrális caudate mag , a putamen , a substantia nigra , a nucleus accumbens , a ventrális tegmentális terület , a locus coeruleus , az amygdala és a raphe mag . A hTAAR1 -et humán asztrocitákban is azonosították.
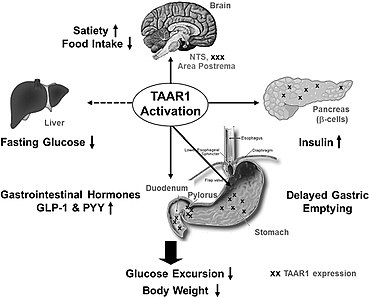
Az emberi központi idegrendszeren kívül a hTAAR1 intracelluláris receptorként is előfordul, és elsősorban a gyomorban , a belekben , a nyombélben , a hasnyálmirigy β-sejtjeiben és a fehérvérsejtekben expresszálódik . A nyombélben a TAAR1 aktiválása növeli a glukagonszerű peptid-1 (GLP-1) és a peptid YY (PYY) felszabadulását; a gyomorban megfigyelték, hogy a hTAAR1 aktiválása fokozza a szomatosztatin (növekedési hormon gátló hormon) szekrécióját a delta sejtekből .
A hTAAR1 az egyetlen humán nyomelemhez kapcsolódó receptor altípus, amely nem fejeződik ki a humán szaglóhámban .
Az idegsejteken belüli elhelyezkedés
A TAAR1 egy intracelluláris receptor, amely emberekben és más állatokban a monoamin neuronok preszinaptikus terminálisában expresszálódik. Modellsejtrendszerekben a hTAAR1 rendkívül gyenge membrán expressziót mutat. A hTAAR1 membrán expressziójának kiváltására szolgáló módszert alkalmazták annak farmakológiájának tanulmányozására biolumineszcens rezonancia energiaátviteli cAMP vizsgálattal.
Mivel a TAAR1 intracelluláris receptor a monoamin neuronokban, az exogén TAAR1 ligandumoknak egy membrán transzport fehérjén keresztül kell belépniük a preszinaptikus neuronba, vagy képesnek kell lenniük a preszinaptikus membránon keresztül diffundálni, hogy elérjék a receptort, és újrafelvétel gátlást és neurotranszmitter kiáramlást hozzanak létre . Következésképpen egy adott TAAR1 ligandum hatékonysága ezeknek a hatásoknak a kiváltásában különböző monoamin idegsejtekben függ a TAAR1 -hez való kötődési affinitásától és attól, hogy képes -e áthaladni a preszinaptikus membránon minden egyes neurontípusnál. A TAAR1 ligandum szubsztrát -affinitása közötti változatosság a különböző monoamin transzportereknél nagymértékben megkülönbözteti a neurotranszmitter felszabadulását és az újrafelvétel gátlását előidéző képességét a különböző típusú monoamin neuronokban. Például egy TAAR1 ligandum, amely könnyen átjuthat a norepinefrin transzporteren, de nem a szerotonintranszporteren, a noradrenalin idegsejtekben-a többihez hasonlóan- jelentősen nagyobb TAAR1-indukált hatást fog kifejteni, mint a szerotonin neuronok.
Receptor oligomerek
A TAAR1 GPCR oligomereket képez monoamin autoreceptorokkal neuronokban in vivo . Ezek és más jelentett TAAR1 hetero-oligomerek a következők:
Ligandok
| Az aminnal kapcsolatos receptorok nyomon követése 1 | |
|---|---|
| Transzdukciós mechanizmusok | G s , G q , GIRKs , β-arresztin 2 |
| Elsődleges endogén agonisták | tiramin , β-fenil-etil-amin , oktopamin , dopamin |
| Agonisták | Endogén: nyomokban lévő aminok Exogén: RO5166017 , amfetamin , metamfetamin , egyéb |
| Semleges antagonisták | Egyik sem jellemezte |
| Inverz agonisták | EPPTB |
| Pozitív alloszterikus modulátorok | N/A |
| Negatív alloszterikus modulátorok | N/A |
| Külső erőforrások | |
| IUPHAR/BPS | 364 |
| DrugBank | Q96RJ0 |
| HMDB | HMDBP10805 |
Agonisták
Nyomozz aminokat
A nyomkövető aminok endogén aminok, amelyek agonistaként hatnak a TAAR1 -nél, és 0,1-10 nM extracelluláris koncentrációban vannak jelen az agyban, ami az emlősök idegrendszerében lévő összes biogén amin kevesebb mint 1% -át teszi ki . Néhány emberi nyom-aminok közé tartozik a triptamin , fenetilamin (PEA), N -methylphenethylamine , p -tyramine , m -tyramine , N -methyltyramine , p -octopamine , m -octopamine , és szinefrint . Ezek szerkezeti hasonlóságot mutatnak a három közös monoaminnal: a szerotoninnal , a dopaminnal és a noradrenalinnal . Mindegyik ligandumnak más a hatása, mint a megnövekedett ciklikus AMP (cAMP) koncentráció a kötési esemény után.
Az elsődleges endogén ligandumok hatékonysági sorrendje a hTAAR1-en a következő:
tiramin > β-fenetilamin > dopamin = oktopamin .
Tironaminok
Thyronamines molekuláris származékai pajzsmirigy hormon , és nagyon fontos a endokrin rendszer működését. A 3-jódtironamin (T 1 AM) a legerősebb TAAR1 agonista, amelyet eddig felfedeztek, bár nem rendelkezik monoamin transzporter affinitással, és ezért kevés hatással van a központi idegrendszer monoamin neuronjaira . A TAAR1 T 1 AM által történő aktiválása nagy mennyiségű cAMP termelését eredményezi. Ez a hatás párosul a testhőmérséklet csökkenésével és a szív teljesítményével .
Szintetikus
- Az amfetamin és helyettesített származékai, a metamfetamin és az MDMA erős hTAAR1 agonisták . A TAAR1-hez társítva a PEA és a p-tiraminhoz hasonlóan a cAMP-termelés növekedését idézik elő. Ezek a vegyületek szerkezetileg hasonlóak a PEA-hoz és a p-tiraminhoz.
- Benzofuránok : 5-APB , 5-APDB , 6-APB , 6-APDB , 4-APB , 7-APB , 5-EAPB , és 5-MAPDB , valamint a benzodifuran 2C-B-FLY , olyan hTAAR1 agonisták, hogy van egy MDMA -szerű farmakodinámiás profil.
- A metilfenetilaminok a hTAAR1 agonistái ; ezek közé tartoznak a α-metilf (amfetamin), β-metilf , N -methylphenethylamine (nyomnyi amin), 2-metilf , 3-metilf , és 4-metilf .
- Patkányokban, lizergsav-dietilamid (LSD) agonistája rTAAR1 , de emberben nincs semmilyen affinitása az hTAAR1 .
- Bizonyos 2- aminooxazolin -vegyületek ( RO5166017 , RO5256390 , RO5203648 és RO5263397 ) orálisan biológiailag hozzáférhetőek , erősen erős és szelektív TAAR1 agonisták laboratóriumi állatokban.
- Az RO5166017 vagy (S) -4-[(etil-
- Az RO5203648 és az RO5263397 erősen szelektív TAAR1 parciális agonisták. Az RO5203648 egyértelmű antidepresszáns és antipszichotikus aktivitást mutatott, emellett gyengítette a gyógyszerek önbeadását, és ébrenlétet elősegítő és kogníciójavító tulajdonságokat mutatott az egér és az egyedek modelljeiben.
Részleges agonisták
- Ralmitaront , vizsgálati antipszichotikum.
Inverz agonisták
- Az EPPTB vagy N- (3-etoxi-fenil) -4- (pirrolidin-1-il) -3-trifluormetil-benzamid szelektív hTAAR1 inverz agonista .
Semleges antagonisták
2018 elején a hTAAR1 semleges semleges antagonistáit nem jellemezték.
Funkció
|
Fenetil-amin és amfetamin egy TAAR1-lokalizált dopamin neuronban
|
Monoaminerg rendszerek
A TAAR1 felfedezése előtt úgy gondolták, hogy a nyomelemek nagyon korlátozott funkciókat látnak el. Úgy gondolták, hogy indukálják a noradrenalin felszabadulását a szimpatikus idegvégződésekből, és versengnek a katekolamin- vagy szerotonin -kötőhelyekért a rokon receptorokon, transzportereken és tárolóhelyeken. Ma úgy vélik, hogy sokkal dinamikusabb szerepet játszanak, mivel szabályozzák az agy monoaminerg rendszereit.
Az egyik downstream hatások aktív TAAR1 növelése cAMP a preszinaptikus sejtben keresztül Ga s G-protein aktiválását adenilil-cikláz . Ennek önmagában sok sejtes következménye lehet. A cAMP fő funkciója lehet a nyomokban lévő aminok expressziójának szabályozása a sejt citoplazmájában . Ezek az aminok ezután aktiválják az intracelluláris TAAR1 -et. A monoamin autoreceptorok (pl. D 2 rövid , preszinaptikus α 2 és preszinaptikus 5-HT 1A ) ellentétes hatást fejtenek ki, mint a TAAR1, és ezek a receptorok együttesen szabályozó rendszert biztosítanak a monoaminok számára. Nevezetesen, az amfetamin és a nyomelemek nagy kötési affinitással rendelkeznek a TAAR1 -hez, de nem a monoamin autoreceptorokhoz. A TAAR1 agonisták hatása az agy monoamin transzportereire helyspecifikusnak tűnik. A képalkotó vizsgálatok azt mutatják, hogy az amfetamin és a nyomelemek monoamin visszavételének gátlása a TAAR1 együttes lokalizációjának jelenlététől függ a kapcsolódó monoamin neuronokban. 2010 -től a TAAR1 és a dopamin transzporter (DAT) együttes lokalizációját vizualizálták rhesus majmoknál, de a TAAR1 és a norepinefrin transzporter (NET) és a szerotonin transzporter (SERT) együttes lokalizációját csak a hírvivő RNS bizonyította (mRNS) expresszió.
Az egyidejűleg lokalizált TAAR1 neuronokban a TAAR1 agonisták növelik a kapcsolódó monoaminok koncentrációját a szinaptikus hasadékban , ezáltal növelve a posztszinaptikus receptor kötődést. A G-proteinnel kapcsolt, befelé korrigáló káliumcsatornák (GIRK) közvetlen aktiválásával a TAAR1 csökkentheti a dopamin-idegsejtek tüzelési sebességét , és megakadályozhatja a hiper-dopaminerg állapotot. Az amfetamin és a nyomelemek bejuthatnak a preszinaptikus neuronba akár DAT -on keresztül, akár közvetlenül a neuronális membránon keresztül diffundálva. A DAT -felvétel következtében az amfetamin és a nyomelemek versenyképes visszavételt gátolnak a transzporterben. A preszinaptikus neuronba való belépéskor ezek a vegyületek aktiválják a TAAR1 -et, amely a protein -kináz A (PKA) és a protein -kináz C (PKC) jelátvitel révén DAT -foszforilációt okoz . Bármelyik proteinkináz által végzett foszforiláció DAT internalizációt ( nem kompetitív visszavétel gátlás) eredményezhet, de a PKC által közvetített foszforiláció önmagában fordított transzporter funkciót (dopamin efflux ) indukál .
Immunrendszer
A TAAR1 limfocitákon való expressziója a limfocita immunjellemzők aktiválásával jár. Az immunrendszerben a TAAR1 aktív PKA és PKC foszforilációs kaszkádokon keresztül továbbítja a jeleket . Egy 2012 -es tanulmányban Panas et al. megfigyelte, hogy a metamfetaminnak vannak ilyen hatásai, ami arra utal, hogy az agyi monoamin-szabályozás mellett az amfetaminhoz kapcsolódó vegyületek is hatással lehetnek az immunrendszerre. Egy nemrég megjelent tanulmány kimutatta, hogy a TAAR1 mellett a TAAR2 is szükséges a nyomelemek teljes aktivitásához a PMN sejtekben .
A fitohaemagglutinin felülszabályozza a hTAAR1 mRNS -t a keringő leukocitákban ; ezekben a sejtekben a TAAR1 aktiváció a leukocita kemotaxist közvetíti a TAAR1 agonisták felé. A TAAR1 agonisták (pontosabban nyomelemek) szintén kimutatták, hogy interleukin 4 szekréciót indukálnak a T-sejtekben és immunglobulin E (IgE) szekréciót a B-sejtekben .
Az asztrocitákban lokalizált TAAR1 szabályozza az EAAT2 szintjét és működését ezekben a sejtekben; ez összefüggésbe hozható a neuroimmun rendszer metamfetamin által kiváltott patológiáival .
Klinikai jelentőség
Az agy alacsony fenetilamin (PEA) koncentrációja súlyos depressziós rendellenességgel , a magas koncentráció pedig skizofréniával jár . Úgy tűnik, hogy az alacsony PEA-szint és a TAAR1 alulaktiválása is összefügg az ADHD-val . Feltételezések szerint az elégtelen PEA -szint a TAAR1 inaktiválódását és a transzporterek túlbuzgó monoamin -felvételét eredményezi, ami depressziót eredményezhet. Egyes antidepresszánsok a monoamin -oxidáz (MAO) gátlásával működnek , ami növeli a nyomelemek koncentrációját, ami feltételezések szerint fokozza a TAAR1 aktivációt a preszinaptikus sejtekben. A csökkent PEA- anyagcsere összefüggésbe hozható a skizofréniával, logikus megállapítás, hogy a PEA-felesleg a TAAR1 túlaktiválását és a monoamin transzporter funkció megelőzését eredményezné. A humán 6. kromoszóma q23.1 régiójának mutációi - ugyanaz a kromoszóma, amely a TAAR1 kódját tartalmazza - összekapcsolódtak a skizofréniával.
A 2015 és 2016 februári orvosi vélemények megállapították, hogy a TAAR1-szelektív ligandumok jelentős terápiás potenciállal rendelkeznek a pszichostimuláns függőségek (pl. Kokain, amfetamin, metamfetamin stb.) Kezelésére. Annak ellenére, hogy a CNS -en és a PNS -en kívüli széles körű elterjedés TAAR1 nem befolyásolja a hematológiai funkciókat és a pajzsmirigyhormonok szabályozását az öregedés különböző szakaszaiban. Ezek az adatok azt mutatják, hogy a jövőbeni TAAR1-alapú terápiáknak kevés hematológiai hatást kell kifejteniük, és így valószínűleg jó biztonsági profiljuk lesz.
Kutatás
A 2011 szeptemberében közzétett nagy jelölt génszövetség-tanulmány jelentős különbségeket talált a TAAR1 allél gyakoriságában a fibromyalgia betegek kohora és a krónikus fájdalommentes kontrollcsoport között, ami arra utal, hogy ez a gén fontos szerepet játszhat az állapot patofiziológiájában; ez valószínűleg a terápiás beavatkozás célpontja.
Patkányokon végzett preklinikai vizsgálatokban a TAAR1 aktiválása a hasnyálmirigy sejtjeiben elősegíti az inzulin , YY peptid és GLP-1 szekréciót; ezért a TAAR1 potenciálisan biológiai célpont az elhízás és a cukorbetegség kezelésére .
Megjegyzések
Hivatkozások
Ez a cikk az Egyesült Államok Nemzeti Orvostudományi Könyvtárának szövegét tartalmazza , amely nyilvános .
Külső linkek
-
 A TAAR1 -hez kapcsolódó média a Wikimedia Commons -ban
A TAAR1 -hez kapcsolódó média a Wikimedia Commons -ban