CYP3A4 - CYP3A4
A citokróm P450 3A4 (rövidítve CYP3A4 ) ( EC 1.14.13.97 ) fontos enzim a szervezetben, főleg a májban és a bélben található. Ez oxidálja kis külföldi szerves molekulák ( xenobiotikumok ), mint például a toxinok vagy gyógyszerek, úgy, hogy el lehet távolítani a szervezetből.
Míg sok gyógyszert inaktivál a CYP3A4, vannak olyan gyógyszerek is, amelyeket az enzim aktivál . Egyes anyagok, mint például néhány gyógyszer és a grapefruitlében lévő furanokumarinok , zavarják a CYP3A4 hatását. Ezek az anyagok tehát felerősítik vagy gyengítik azoknak a gyógyszereknek a hatását, amelyeket a CYP3A4 módosít.
A CYP3A4 a citokróm P450 oxidáló enzimcsalád tagja. Ennek a családnak számos más tagja is részt vesz a gyógyszerek metabolizmusában, de a CYP3A4 a leggyakoribb és a legsokoldalúbb. E család minden tagjához hasonlóan ez is hemoprotein , azaz fehérje, amely vasatomot tartalmazó hem -csoportot tartalmaz. Emberben a CYP3A4 fehérjét a CYP3A4 gén kódolja . Ez a gén része a 7q22.1 kromoszómán található citokróm P 450 géneknek .
Funkció
CYP3A4 tagja a citokróm P450 szupercsalád a enzimek . A citokróm P450 fehérjék monooxigenázok, amelyek katalizálják a gyógyszerek metabolizmusában és a koleszterin, szteroidok és egyéb lipidkomponensek szintézisében szerepet játszó számos reakciót .
A CYP3A4 fehérje az endoplazmatikus retikulumban lokalizálódik , és expresszióját glükokortikoidok és egyes farmakológiai szerek indukálják . A citokróm P450 enzimek az előírt gyógyszerek hozzávetőleg 60% -át metabolizálják, a metabolizmus körülbelül feléért a CYP3A4 felelős; a szubsztrátok közé tartozik az acetaminofen, a kodein, a ciklosporin (ciklosporin), a diazepám és az eritromicin. Az enzim egyes szteroidokat és rákkeltő anyagokat is metabolizál. A legtöbb gyógyszer dezaktiválódik a CYP3A4 által, közvetlenül vagy a szervezetből történő egyszerű kiválasztás révén. Ezenkívül sok anyagot a CYP3A4 bioaktivál , hogy aktív vegyületeket hozzon létre, és sok protoxin mérgezővé válik toxikus formákká (példák - lásd az alábbi táblázatot) .
CYP3A4 is rendelkezik epoxigenáz aktivitással, hogy metabolizál arachidonsav hogy epoxyeicosatrienoic savak (EETS), azaz (±) -8,9-, (±) -11,12-, és (±) -14,15-epoxyeicosatrienoic savak. Az EET -k számos tevékenységet folytatnak, beleértve bizonyos típusú rákok népszerűsítését (lásd epoxi -eicosatetraénsav ). A CYP3A4 elősegíti a különböző típusú emberi rákos sejtvonalak növekedését a tenyészetben azáltal, hogy (±) -14,15-epoxi-eicosatrieno-savakat termel, amelyek stimulálják ezeket a sejteket. A citokróm P450 zsírsav-monooxgenáz aktivitással is rendelkezik, amely az arachidonsavat 20-hidroxi- eicosatetraénsavvá (20-HETE) metabolizálja . A 20-HETE tevékenységek széles skáláját kínálja, amelyek magukban foglalják a növekedés serkentését emlő- és más típusú rákokban is (lásd 12-hidroxi-eicosatetraénsav ).
Evolúció
A CYP3A4 gén a paralogeihoz képest sokkal bonyolultabb felfelé irányuló szabályozó régiót mutat . Ez a megnövekedett komplexitás érzékenyebbé teszi a CYP3A4 gént az endogén és exogén PXR és CAR ligandumokkal szemben, ahelyett, hogy tágabb specifikációra támaszkodna. A csimpánz és a humán CYP3A4 sok ligandum anyagcseréjében erősen konzerválódott , bár az emberekben pozitívan kiválasztott négy aminosav a 7-BFC 5-szörös benzilációjához vezetett a hepatotoxikus másodlagos epesav- litokolsav jelenlétében . Ez a változás hozzájárul az emberi kolesztázis elleni fokozott védekezéshez .
Szöveteloszlás
A magzatok általában nem a CYP3A4 -et fejezik ki a májszövetükben, hanem inkább a CYP3A7 -et ( EC 1.14.14.1 ), amely hasonló szubsztrátumokra hat. A CYP3A4 nincs jelen a magzati májban, de a felnőtt szint körülbelül 40% -ára emelkedik az élet negyedik hónapjában és 72% -ra a 12. hónapban.
Bár a CYP3A4 túlnyomórészt a májban található, a test más szerveiben és szöveteiben is jelen van, ahol fontos szerepet játszhat az anyagcserében. A bélben található CYP3A4 fontos szerepet játszik bizonyos gyógyszerek metabolizmusában. Ez gyakran lehetővé teszi a prodrugok aktiválását és felszívódását -mint a hisztamin H 1 -receptor antagonista terfenadin esetében .
A közelmúltban a CYP3A4 -et is azonosították az agyban, de szerepe a központi idegrendszerben még mindig nem ismert.
Mechanizmusok
A citokróm P450 enzimek számos módosítást végeznek különféle ligandumokon, kihasználva annak nagy aktív helyét és azt a képességét, hogy egyszerre több szubsztrátot is megköthet, hogy bonyolult kémiai változásokat végezzen az endogén és exogén vegyületek metabolizmusában. Ide tartozik a hidroxilezés , az olefinek epoxidálása , aromás oxidáció , heteroatom-oxidációk, N- és O-dealkilációs reakciók, aldehid oxidációk, dehidrogénezési reakciók és aromatázaktivitás.
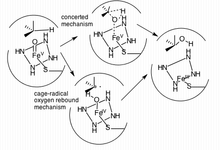
Az sp 3 CH kötés hidroxilezése az egyik módja annak, hogy a CYP3A4 (és a citokróm P450 oxigenázok) befolyásolja a ligandumát. Valójában a hidroxilezést néha dehidrogénezés követi, ami bonyolultabb metabolitokhoz vezet. Példa egy olyan molekulára, amely a CYP3A4 miatt egynél több reakción megy keresztül, a tamoxifen , amelyet 4-hidroxi-tamoxifenné hidroxileznek, majd 4-hidroxi-tamoxifen-kinon-metiddé dehidratálnak. Két mechanizmust javasoltak a P450 enzimek hidroxilezésének elsődleges útjaként.
Az első javasolt út egy ketrec által vezérelt radikális módszer ("oxigén visszapattanás"), a második pedig egy összehangolt mechanizmust foglal magában, amely nem használ gyökös köztiterméket, hanem nagyon gyorsan működik egy " radikális óra " segítségével.
Gátlás gyümölcslenyelés útján
1998 -ban különböző kutatók kimutatták, hogy a grapefruitlé és általában a grapefruit a CYP3A4 erős inhibitora, amely befolyásolhatja a különböző gyógyszerek metabolizmusát, növelve azok biohasznosulását . Bizonyos esetekben ez végzetes kölcsönhatáshoz vezethet olyan gyógyszerekkel, mint az asztemizol vagy a terfenadin . A grapefruitlé hatását a gyógyszerek felszívódására vonatkozóan eredetileg 1989-ben fedezték fel. Az első közzétett jelentés a grapefruit gyógyszerkölcsönhatásokról 1991-ben jelent meg a Lancet-ben , " A citruslevek kölcsönhatása a felodipinnel és a nifedipinnel" címmel, és ez volt az első bejelentett élelmiszer-gyógyszer. kölcsönhatás klinikailag. A grapefruit hatása 3-7 napig tart, és a legnagyobb hatás akkor jelentkezik, ha a levet egy órával a gyógyszer beadása előtt veszik be.
A grapefruit mellett más gyümölcsök is hasonló hatásúak. A Noni ( M. citrifolia ) például táplálékkiegészítő, amelyet általában gyümölcslé formájában fogyasztanak, és gátolja a CYP3A4 -et is; a gránátalma lé is ezt a hatást fejti ki .
Változékonyság
Míg több mint 28 egyetlen nukleotid polimorfizmust (SNP) azonosítottak a CYP3A4 génben, azt találták, hogy ez nem jelent jelentős egyénközi variabilitást in vivo . Feltételezhető, hogy ennek oka a szubsztrátoknak való expozíció során a CYP3A4 indukciója lehet.
Azok a CYP3A4 allélok, amelyekről a jelentések szerint minimális funkciójuk van a vad típusúakhoz képest, a CYP3A4*6 (A17776 inszerció) és CYP3A4*17 (F189S). Mindkét SNP csökkentette a katalitikus aktivitást bizonyos ligandokkal, beleértve a tesztoszteront és a nifedipint a vad típusú metabolizmushoz képest. Ezzel szemben a CYP3A4*1G allél erősebb enzimatikus aktivitással rendelkezik, mint a CYP3A4*1A (vad típusú allél).
A CYP3A4 funkció változékonyságát nem invazív módon lehet meghatározni az eritromicin légzésvizsgálattal (ERMBT). A ERMBT becslések in vivo a CYP3A4 aktivitást mérjük a radioaktív izotóppal jelzett szén-dioxid a kilélegzett után intravénás dózis ( 14 C- N -metil) - eritromicin .
Indukció
A CYP3A4 -et számos ligandum indukálja . Ezek a ligandumok kötődnek a pregnán X receptorhoz (PXR). Az aktivált PXR komplex heterodimert képez a retinoid X receptorral (RXR), amely a CYP3A4 gén XREM régiójához kötődik . Az XREM a CYP3A4 gén szabályozó régiója , és a kötődés kooperatív kölcsönhatást okoz a gén proximális promoter régióival, ami a CYP3A4 fokozott transzkripcióját és expresszióját eredményezi. Aktiválása PXR / RXR heterodimert kezdeményezi transzkripcióját a CYP3A4 promoter régió és a gén. A ligandumkötés fokozódik, ha CYP3A4 ligandumok jelen vannak, például aflatoxin B1, M1 és G1 jelenlétében . Valójában az enzim nagy és alakítható aktív helye miatt lehetséges, hogy az enzim egyszerre több ligandumot köt meg, ami potenciálisan káros mellékhatásokhoz vezethet.
Kimutatták, hogy a CYP3A4 indukciója emberben nemtől függően változik. A bizonyítékok azt mutatják, hogy a nőknél a CYP3A4 fokozza a gyógyszer clearance -ét, még akkor is, ha figyelembe vesszük a testsúlybeli különbségeket. Wolbold és munkatársai tanulmánya. (2003) azt találták, hogy a nők véletlenszerű mintájából sebészileg eltávolított májmintákból mért átlagos CYP3A4 -szintek 129%-kal meghaladták a férfiak májában lévő CYP3A4 -szintet. A CYP3A4 mRNS- átiratokat hasonló arányban találták, ami a transzláció előtti mechanizmusra utal a nőknél a CYP3A4 fokozott szabályozására. Ennek az emelkedett enzimszintnek a pontos oka még mindig csak találgatás alatt áll, azonban a vizsgálatok más mechanizmusokat is tisztáztak (mint például a CYP3A5 vagy a CYP3A7 kompenzációja a csökkent CYP3A4 -szintekért), amelyek mind a férfiak, mind a nők esetében befolyásolják a gyógyszer clearance -ét.
A CYP3A4 szubsztrát aktivációja különböző állatfajok között változik. Bizonyos ligandumok aktiválják a humán PXR -t, amely elősegíti a CYP3A4 transzkripciót, míg más fajokban nem mutat aktivációt. Például az egér PXR-t nem aktiválja a rifampicin, és a humán PXR-t nem aktiválja a pregnenalon 16α-karbonitril. A CYP3A4 funkcionális útvonalainak in vivo tanulmányozásának megkönnyítése érdekében egér törzseket fejlesztettek ki transzgének felhasználásával a null/humán CYP3A4 és PXR előállítására keresztek. Bár a humanizált hCYP3A4 egerek sikeresen expresszálták az enzimet a bélrendszerükben, a májban alacsony hCYP3A4 szintet találtak. Ezt a hatást a növekedési hormon jelátviteli útja a CYP3A4 szabályozásnak tulajdonította . Az in vivo modell biztosítása mellett humanizált CYP3A4 egereket (hCYP3A4) használtak a nemi különbségek további hangsúlyozására a CYP3A4 aktivitásban.
A CYP3A4 aktivitási szinteket étrenddel és környezeti tényezőkkel is összefüggésbe hozták, például a xenobiotikus anyagok expozíciójának időtartamával. Mivel az enzim széles körben jelen van a bélnyálkahártyában, az enzim érzékeny az éhezés tüneteire, és a káros hatások védelmében felül van szabályozva. Valójában a kövér fejű mínuszokban kimutatták, hogy az etetés nélküli nőstény halak megnövelték a PXR és a CYP3A4 expresszióját, és több napos éhezés után az expozíciót követően kifejezettebben reagáltak a xenobiotikus tényezőkre. Az állatmodellek tanulmányozásával és a CYP3A4 aktiváció veleszületett különbségeinek szem előtt tartásával a kutatók jobban meg tudják jósolni a gyógyszerek metabolizmusát és mellékhatásait az emberi CYP3A4 útvonalakban.
Forgalom
A humán CYP3A4 forgalmi arányára vonatkozó becslések nagymértékben eltérnek. A máj CYP3A4 esetében az in vivo módszerek az enzim felezési idejének becsléseit elsősorban a 70 és 140 óra közötti tartományban, míg az in vitro módszerek 26 és 79 óra közötti becsléseket adják. Forgalma gut CYP3A4 valószínűleg függvényében az arány enterocyte megújítása ; a közvetett megközelítés, amely a grapefruitlé-expozíciót követő aktivitás helyreállításán alapul, 12 és 33 óra közötti méréseket eredményez.
Technológia
A membránhoz kötött CYP3A4 természetes konglomerátum-hajlamának köszönhetően történelmileg nehéz volt tanulmányozni a gyógyszerkötést oldatban és felületen egyaránt. Az együttkristályosodás nehéz, mivel a szubsztrátok hajlamosak alacsony Kd- értékre (5-150 μM) és alacsony oldhatóságra vizes oldatokban. A megkötött enzim izolálásának sikeres stratégiája a monomer CYP3A4 funkcionális stabilizálása ezüst nanorészecskéken, amelyeket nanoszféra litográfiából állítanak elő, és lokalizált felületi plazmonrezonancia -spektroszkópiával (LSPR) elemeznek. Ezek az elemzések felhasználhatók a gyógyszer-kötődés nagy érzékenységi vizsgálataként, és szerves részévé válhatnak a további nagy áteresztőképességű vizsgálatoknak, amelyeket a kezdeti gyógyszerkutatási tesztek során alkalmaznak. Az LSPR mellett a CYP3A4-Nanodisc komplexeket más alkalmazásokban is hasznosnak találták, beleértve a szilárdtest-NMR-t , a redox-potenciometriát és az egyensúlyi állapotú enzimkinetikát .
Ligandok
Az alábbiakban egy táblázat található a kiválasztott szubsztrátokról , a CYP3A4 induktorokról és inhibitorokról . Ahol az ügynökök osztályai szerepelnek, előfordulhatnak kivételek az osztályon belül.
A CYP3A4 inhibitorokat hatásosságuk szerint lehet osztályozni , például:
- Erős inhibitor, amely a plazma AUC értékeinek legalább ötszörösét , vagy a clearance több mint 80% -os csökkenését okozza .
- Mérsékelt inhibitor , amely legalább kétszeres növekedést okoz a plazma AUC-értékében, vagy 50-80% -os csökkenést okoz a clearance-ben.
- A gyenge inhibitor az, amely legalább 1,25-szeres, de kevesebb, mint 2-szeres növekedést okoz a plazma AUC-értékében, vagy 20-50% -kal csökkenti a clearance-t.
| Aljzatok | Gátlók | Indukálók |
|---|---|---|
|
Erős
Mérsékelt
Gyenge
Meghatározatlan hatékonyság
|
Erős potencia Meghatározatlan hatékonyság
|
Interaktív pályatérkép
Kattintson az alábbi génekre, fehérjékre és metabolitokra a megfelelő cikkekre mutató hivatkozáshoz.
Lásd még
Hivatkozások
Külső linkek
- PharmGKB: Annotált PGx géninformáció a CYP3A4 -hez
- A CYP3A4 szubsztrát előrejelzése
- A humán CYP3A4 genom elhelyezkedése és a CYP3A4 gén részleteinek oldala az UCSC Genome Browser alkalmazásban .
- Áttekintést az összes szerkezeti információ áll rendelkezésre a PDB a UniProt : P08684 (citokróm P450 3A4) a pDBE-KB .
Ez a cikk az Egyesült Államok Nemzeti Orvostudományi Könyvtárának szövegét tartalmazza , amely nyilvános .