A szklerózis multiplex kezelése - Management of multiple sclerosis
A szklerózis multiplex (MS) krónikus gyulladásos demielinizáló betegség , amely a központi idegrendszert (CNS) érinti . Számos terápia létezik, bár nincs ismert gyógymód.
A betegség leggyakoribb kezdeti lefolyása a visszaeső-remitáló altípus, amelyet előre nem látható rohamok ( visszaesések ) jellemeznek, majd a relatív remisszió periódusai, a betegség aktivitásának új jelei nélkül. Néhány év elteltével sokan, akiknek ez az altípusa van, neurológiai hanyatlást tapasztalnak akut visszaesések nélkül. Ebben az esetben másodlagos progresszív szklerózis multiplexnek nevezik. A betegség egyéb, kevésbé gyakori lefolyása az elsődleges progresszív (kezdettől fogva hanyatlás támadások nélkül) és a progresszív-visszaeső (folyamatos neurológiai hanyatlás és egymásra helyezett támadások). Különböző terápiákat alkalmaznak az akut rohamokban szenvedő betegeknél, a relapszusos-remitáló altípusban szenvedő betegeknél, a progresszív altípusú betegeknél, az MS diagnózis nélküli betegeknél, akik demielinizáló eseményt szenvednek, és az SM különböző következményeinek kezelésére.
A terápia elsődleges célja a funkció visszatérése a támadás után, az új támadások megelőzése és a fogyatékosság megelőzése. Mint minden orvosi kezelésnél, az SM kezelésére használt gyógyszereknek is lehetnek káros hatásai , és sok lehetséges terápiát még vizsgálnak. Ugyanakkor sokan alternatív gyógymódokat követnek, annak ellenére, hogy kevés az alátámasztó, összehasonlítható, megismételt tudományos tanulmány. Az őssejt -terápiát tanulmányozzák.
Ez a cikk a standard MS terápiáira összpontosít; az SM határ menti formái speciális kezelésekkel rendelkeznek, amelyek kizártak.
Akut támadások
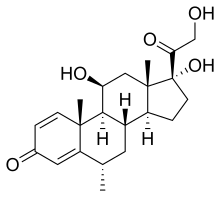
Nagy dózisú intravénás kortikoszteroidok , például metilprednizolon alkalmazása az akut relapszusok rutinterápiája. Ezt három-öt napos periódusban adják be, és jól bevált hatékonysággal segíti elő a roham utáni fogyatékosságból való gyorsabb gyógyulást . Mindazonáltal nincs elegendő bizonyíték arra, hogy bármilyen jelentős hatást jelezne a kortikoszteroid-kezelések hosszú távú fogyatékosságára. A szájon át adott szteroidok hasonló hatékonysággal és biztonsággal rendelkeznek az SM tüneteinek kezelésében, mint az intravénás kezelés. A súlyos rohamok következményei, amelyek nem reagálnak a kortikoszteroidokra, plazmaferézissel kezelhetők .
Betegséget módosító kezelések
2020-tól számos betegségmódosító kezelést hagytak jóvá különböző országok szabályozó ügynökségei, köztük az USA Élelmiszer- és Gyógyszerügyi Hatósága (FDA), az Európai Gyógyszerügynökség (EMA) és a japán Gyógyszerészeti és Orvosi Eszközök Ügynöksége (PMDA) Egészségügyi, Munkaügyi és Jóléti Minisztérium .
Az FDA által jóváhagyott gyógyszerek a következők: béta-1a és béta-1b interferonok , monoklonális antitestek: natalizumab , alemtuzumab , okrelizumab és immunmodulátorok: glatiramer-acetát , mitoxantron , fingolimod , teriflunomid , dimetil-fumarát és diroximel-fumarát . A Siponimodot 2019 márciusában hagyták jóvá. A kladribint 2019 márciusában hagyták jóvá. Az Ozanimodot 2020 márciusában hagyták jóvá.
A daklizumabot , amelyet egyszer jóváhagytak, később visszavonták.
Gyógyszerek
1993-ban a béta-1b-interferon volt az első olyan gyógyszer, amelyet valaha is MS-ben engedélyeztek, ezt hamarosan a béta-1a-interferon és a glatiramer-acetát követte.
A béta-1a-interferont hetente ( intramuszkuláris injekció ) vagy hetente háromszor ( szubkután injekció ) injektálják, a kereskedelmi forgalomban kapható készítményektől függően, míg a béta-1b-interferont szubkután injekciózzák minden második napon. 2014-ben mutatták be a béta-1a interferon pegilált formáját Plegridy márkanévvel, amely szubkután injekció formájában kapható. Ez a peginterferon béta 1-a polietilénglikolt köt az interferon molekulákhoz, lehetővé téve a szervezetben a tartósabb biológiai hatásokat, miközben kéthetente egyszer csökkenti az alkalmazás gyakoriságát. A béta-interferon kiegyensúlyozza a gyulladásgátló és gyulladásgátló szerek expresszióját az agyban, és csökkenti a vér-agy gáton áthaladó gyulladásos sejtek számát . Összességében a béta -interferonnal végzett kezelés a neuronok gyulladásának csökkenéséhez vezet. Ezenkívül úgy gondolják, hogy növeli az ideg növekedési faktor termelését és következésképpen javítja az idegsejtek túlélését.
A glatiramer -acetát négy aminosavból álló véletlenszerű polimerek keveréke, amely antigénben hasonlít a mielin -alapfehérjéhez, amely az idegek mielinhüvelyének egyik összetevője, amellyel verseng a T -sejteknek való megjelenésért. Naponta szubkután adják be.
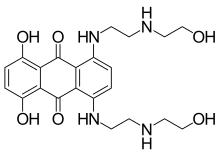
A mitoxantron egy olyan immunszuppresszáns, amelyet rákos kemoterápiában is alkalmaznak, és amelyet 2000 -ben engedélyeztek az MS számára; mivel a natalizumab egy monoklonális antitest , amelyet eredetileg 2004 -ben hagytak jóvá. Mindkettőt intravénás infúzióban adják be havi időközönként natalizumab esetén, és háromhavonta mitoxantron esetén.
2010-ben a fingolimod , a szfingozin-1-foszfát receptor modulátor lett az első orális gyógyszer, amelyet az FDA hagyott jóvá, majd 2012-ben a teriflunomid követte , amely a pirimidin szintézisét gátolja, és megzavarja a T-sejtek kölcsönhatását az antigént bemutató sejtekkel . A fingolimodot és a teriflunomidot naponta egyszer kell bevenni. 2013 -ban az FDA jóváhagyott egy további orális gyógyszert, a dimetil -fumarátot vagy a BG12- (amely a már létező gyógyszer, a fumársav továbbfejlesztett változata ).
Egy másik orális gyógyszert, a kladribint 2010 -ben hagyták jóvá Oroszországban és Ausztráliában. Kérelmét az FDA és az EMEA 2011 -ben biztonsági okok miatt elutasította. Ez arra késztette a gyógyszert, hogy hagyja abba a forgalmazást és vonja vissza az összes marketing alkalmazást.
2017 márciusában az okrelizumabot jóváhagyták az Egyesült Államokban a primer progresszív sclerosis multiplex felnőttek kezelésére. Felnőtteknél is alkalmazzák a szklerózis multiplex kiújuló formáinak kezelésére, beleértve a klinikailag izolált szindrómát, a relapszusos-remisszív betegséget és az aktív másodlagos progresszív betegséget. Az okrelizumabot 2018 januárjában engedélyezték az Európai Unióban való használatra.
2019 -ben a sziponimodot és a kladribint jóváhagyták az Egyesült Államokban a másodlagos progresszív szklerózis multiplex kezelésére. A Siponimodot az Európai Unióban 2020 januárjában engedélyezték másodlagos progresszív sclerosis multiplexben szenvedő felnőttek kezelésére. A Cladribine -t 2017 augusztusában engedélyezték az Európai Unióban a sclerosis multiplex kiújuló formáiban szenvedő felnőttek kezelésére.
2019 októberében a diroximel -fumarátot (Vumerity) orvosi használatra engedélyezték az Egyesült Államokban.
2020 márciusában az ozanimodot (Zeposia) jóváhagyták az Egyesült Államokban a relapszusos sclerosis multiplex kezelésére, beleértve a klinikailag izolált szindrómát, a relapszusos-remisszív betegséget és az aktív másodlagos progresszív betegséget felnőtteknél.
2020 áprilisában az Egyesült Államokban jóváhagyták a monometil-fumarátot (Bafiertam) a szklerózis multiplex kiújuló formáinak kezelésére, beleértve a klinikailag izolált szindrómát, a relapszusos-remisszív betegséget és az aktív másodlagos progresszív betegséget felnőtteknél.
A Ponesimodot 2021 márciusában engedélyezték orvosi használatra az Egyesült Államokban.
Mellékhatások
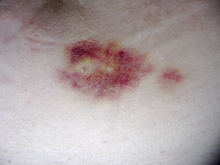
Mind az interferonok, mind a glatiramer -acetát csak injekciós formában állnak rendelkezésre, és mindkettő bőrreakciókat okozhat az injekció beadásának helyén, különösen szubkután adagolás esetén. A bőrreakciók klinikai megjelenése nagymértékben eltér, és tartalmazhat zúzódást, bőrpírt , fájdalmat, viszketést , irritációt, duzzanatot és a legszélsőségesebb esetekben a bőr nekrózisát . Általában a kezelés első hónapjában jelentkeznek, bár gyakoriságuk és fontosságuk hat hónapos használat után csökken. Az enyhe bőrreakciók általában nem akadályozzák a kezelést, míg a nekrózisok a betegek körülbelül 5% -ánál jelentkeznek, és a kezelés abbahagyásához vezetnek. Idővel az injekció beadásának helyén látható horpadás is kialakulhat a zsírszövet helyi pusztulása miatt, amelyet lipoatrófiának neveznek .
Az interferonok , a citokinek egy alosztálya, a szervezetben betegségek, például influenza során termelődnek , hogy segítsenek a fertőzés elleni küzdelemben. Ők felelősek az influenza -fertőzések számos tünetéért, beleértve a lázat , az izomfájdalmat , a fáradtságot és a fejfájást . Sok beteg influenzaszerű tünetekről számol be órákkal a béta-interferon bevétele után, amelyek általában 24 órán belül javulnak, ilyen tünetek a citokinek ideiglenes növekedésével kapcsolatosak. Ez a reakció hajlamos eltűnni 3 hónapos kezelés után, és tünetei kezelhetők vény nélkül kapható nem szteroid gyulladáscsökkentő szerekkel , például ibuprofennel , amelyek csökkentik a lázat és a fájdalmat. A béta-interferon másik gyakori átmeneti másodlagos hatása a betegség már meglévő tüneteinek funkcionális romlása. Az ilyen állapotromlás hasonló a SM -ben szenvedő betegeknél hő, láz vagy stressz ( Uhthoff -jelenség ) következtében fellépő romláshoz , általában a kezelés után 24 órán belül jelentkezik, gyakoribb a kezelés első hónapjaiban, és több napig is eltarthat. A súlyosbodásra különösen érzékeny tünet a spaszticitás . A béta-interferon csökkentheti a fehérvérsejtek ( leukopenia ), a limfociták ( limfopénia ) és a neutrofilek ( neutropenia ) számát is , valamint befolyásolhatja a májműködést . A legtöbb esetben ezek a hatások nem veszélyesek és visszafordíthatók a kezelés abbahagyása vagy csökkentése után. Mindazonáltal az ajánlás az, hogy minden beteget laboratóriumi vérvizsgálatokkal , beleértve a májfunkciós vizsgálatokat is ellenőrizni kell az interferonok biztonságos alkalmazásának biztosítása érdekében.
A glatiramer -acetátot általában jól tolerálják. A glatiramer-acetát leggyakoribb másodlagos hatása bőrprobléma után az injekció utáni reakció, amely kipirulás, mellkasi szorítás, szívdobogás , légszomj és szorongás formájában nyilvánul meg , és általában harminc percnél rövidebb ideig tart, és nem igényel további kezelést.
A mitoxantron terápia immunszuppresszív hatásokkal és májkárosodással járhat ; legveszélyesebb mellékhatása azonban a dózisfüggő szívtoxicitás . Ezért elengedhetetlen az adminisztrációs és ellenőrzési irányelvek gondos betartása ; ez magában foglalja az echokardiogram és a teljes vérkép megszerzését a kezelés előtt annak eldöntésére, hogy a terápia alkalmas -e a betegre, vagy a kockázatok túl nagyok. Javasoljuk, hogy a terápia során a szívkárosodás, fertőzés vagy májműködési zavar első jeleinél hagyja abba a mitoxantron szedését . Szívproblémák (főleg szisztolés diszfunkció ) a betegek több mint 10% -ánál jelentkeznek, míg a leukémia prevalenciája 0,8%.
Nem sokkal a jóváhagyása után a natalizumabot kivonta a forgalomból a gyártója, miután összefüggésbe hozták a ritka, de veszélyes neurológiai állapot három esetével, az úgynevezett progresszív multifokális leukoencephalopathiával (PML). PML egy opportunista fertőzés neurológiai progresszív által okozott tüneteket replikáció a JC-vírus a gliasejtek az agy. Mindhárom kezdeti eset natalizumabot kapott béta-1a-interferonnal kombinálva . A biztonsági felülvizsgálat után a gyógyszer 2006 -ban került vissza a piacra, mint monoterápia az SM -hez egy speciális vényköteles program keretében. 2011 májusáig több mint 130 PML -esetet jelentettek, mindezt azoknál a betegeknél, akik több mint egy éve szedtek natalizumabot. Bár egyikük sem szedte a gyógyszert más betegségmódosító kezelésekkel kombinálva, az MS-kezelések korábbi alkalmazása 3 és 4-szeresére növeli a PML kockázatát. A PML becsült prevalenciája 1,5 eset ezer natalizumab -felhasználóra. A PML -ben szenvedő SM -betegek körülbelül 20% -a meghal, míg a fennmaradó betegek jelentős része fogyatékos.
A klinikai vizsgálatok során a fingolimod olyan mellékhatásokat okozott, mint a magas vérnyomás és a bradycardia , a makulaödéma , a májenzimek emelkedése vagy a limfociták szintjének csökkenése. A teriflunomid nagyon biztonságos gyógyszer. Ennek ellenére beszámoltak májelégtelenségről és PML -ről. A teriflunomidról is ismert, hogy veszélyes a magzat fejlődésére. A dimetil -fumarát leggyakoribb másodlagos hatásai a klinikai vizsgálatok során az öblítés és a gyomor -bélrendszeri problémák voltak. Ezek a problémák általában enyhék voltak, és gyakrabban fordultak elő a kezelés első hónapjában. Míg a dimetil -fumarát a fehérvérsejtek számának csökkenéséhez vezet, és a betegek szintjét monitorozni kell, a klinikai vizsgálatok során nem számoltak be opportunista fertőzésekről. Ezenkívül a fumársavat a pikkelysömör , egy másik autoimmun betegség kezelésére is használják , és több mint 14 éves használatról hosszú távú biztonsági adatok állnak rendelkezésre, anélkül, hogy további veszélyes mellékhatásokat jeleznének. A valós nemkívánatos események jelentésein (FAERS) alapuló aránytalansági elemzésben az FDA által jóváhagyott DMT-k egyike sem társult a rákos megbetegedések jelentette nagyobb kimenetelű kockázathoz.
Klinikailag izolált szindróma
Az RRMS legkorábbi klinikai megjelenése a klinikailag izolált szindróma (CIS), azaz egyetlen tünet egyetlen támadása. A FÁK alatt szubakut roham következik be, amely demielinizációra utal, de a beteg nem felel meg a szklerózis multiplex diagnózisának kritériumainak . A korai kezelés csökkentheti annak kockázatát, hogy az első rohamból klinikailag meghatározott sclerosis multiplexbe kerüljön. Nehéz azonban határozott következtetéseket levonni a legjobb kezelésről, különösen a korai kezelés hosszú távú haszna és biztonsága tekintetében, mivel nincsenek olyan tanulmányok, amelyek közvetlenül összehasonlítanák a betegségmódosító terápiákat vagy a betegek kimenetelének hosszú távú nyomon követését.
Relapszáló-remitáló MS
Gyógyszerek a mérsékelten hatékonynak csökkenő száma támadások RRMS és csökkenti a felhalmozódása agyi elváltozások, amelyek alkalmazásával mérjük a gadolínium - továbbfejlesztett mágneses rezonancia képalkotás (MRI). Az interferonok és a glatiramer-acetát nagyjából egyenértékűek, körülbelül 30% -kal csökkentik a relapszusokat, és biztonságos profiljuk miatt az első vonalbeli kezelések. Ennek ellenére nem minden beteg reagál ezekre a terápiákra. Ismeretes, hogy az SM betegek 30% -a nem reagál a béta-interferonra. A nem reagálással kapcsolatos egyik tényező a magas béta-interferon-semlegesítő antitestek jelenléte . Az interferonterápia, és különösen a béta-1b-interferon, a kezelt betegek 5-30% -ában, a kezelés második 6 hónapjában, általában semlegesítő antitestek termelődését idézi elő. Ezenkívül a kifejezetten aktív SM-ben szenvedő RRMS-betegek egy része, amelyet néha "gyorsan súlyosbodó SM-nek" neveznek, általában nem reagál az immunmodulátorokra, és vagy mitoxantronnal vagy natalizumabbal kezelik.
A natalizumab rendkívül hatékonynak tekinthető a visszaesés gyakoriságának csökkentése és a fogyatékosság progressziójának megállítása szempontjából, azonban a mellékhatások kockázata miatt második vonalbeli kezelésnek minősül. A natalizumab felére csökkenti a relapszusok kockázatát az interferonokhoz képest, összhatékonysága meghaladja a 70%-ot. A mitoxantron szintén rendkívül hasznos a támadások és a fogyatékosság csökkentésében, de általában nem tekintik hosszú távú terápiának súlyos szívtoxicitása miatt.
Hivatalos irányelvek még nincsenek a betegséget módosító szájüregi kezelések alkalmazására, azok legújabb fejlesztése miatt. Míg egyesek úgy vélik, hogy valószínűleg csökkenteni fogják az első vonalbeli kezelések használatát, az interferonok és a glatiramer-acetát hosszú távú biztonsága valószínűleg lelassítja ezt a tendenciát. Javasolt, hogy jelenleg orális kezelést ajánljanak főként azokban az esetekben, amikor a betegek tűfóbia vagy más okok, például az interferonok és a glatiramer -acetát hatástalansága miatt nem alkalmaznak meglévő kezelést . Alkalmazhatók natalizumabot szedő betegeknél is, akiknél JC -vírus antitestek alakultak ki, és ezért fokozott a PML kockázata. A dimetil -fumarát potenciálisan az egyik legérdekesebb orális gyógyszer a pikkelysömörben való használat hosszú távú adatai miatt, ami nagyon jó biztonsági profil felé mutat. A Cochrane 2015-ös szisztematikus áttekintése közepes minőségű bizonyítékot talált arra, hogy a dimetil-fumarát-kezelés kétéves kezelési ideje alatt visszaesett az RRMS-ben szenvedők száma, szemben a placebóval, valamint rossz minőségű bizonyíték a fogyatékosság romlásának csökkenésére, és általános igény magasabb minőségű vizsgálatokra, hosszabb nyomon követéssel.
A különböző kezelések relatív hatékonysága nem egyértelmű, mivel a legtöbbet csak placebóval vagy kis számú más terápiával hasonlították össze. Az interferonok és a glatiramer -acetát közvetlen összehasonlítása hasonló hatásokat vagy csak kismértékű különbségeket jelez a relapszus arányára, a betegség progressziójára és a mágneses rezonancia képalkotó intézkedésekre. Az alemtuzumab, a natalizumab és a fingolimod más gyógyszereknél hatékonyabbak lehetnek a relapszusok rövid távú csökkentésében az RRMS -ben szenvedő betegeknél. A natalizumab és a béta-1a-interferon ( Rebif ) csökkentheti a relapszust mind a placebóhoz, mind a béta-1a-interferonhoz ( Avonex ) képest, míg a béta-1b-interferon ( Betaseron ), a glatiramer-acetát és a mitoxantron szintén megakadályozhatja a visszaeséseket. A fogyatékosság progressziójának csökkentésére vonatkozó relatív hatékonyságra vonatkozó bizonyítékok nem világosak. Minden gyógyszerhez mellékhatások kapcsolódnak, amelyek befolyásolhatják az előnyökre gyakorolt kockázatukat.
Míg további vizsgálatokra van szükség a gyógyszerek hosszú távú hatásairól, különösen a legújabb kezelések esetében, az interferonok és a glatiramer-acetát hatásairól rendelkezésre álló adatok azt mutatják, hogy a korai kezdetű hosszú távú terápia biztonságos, és összefüggésben van a jobb eredményekkel.
Az orális fogamzásgátló tabletták ellentmondásos eredménnyel járnak különböző vizsgálatokban, amelyek a szklerózis multiplexben szenvedő nőknél a visszaesés arányának csökkentésére gyakorolt bármilyen hatást érintik. Bizonyos gyógyszerek az SM tünetei ellen, például a karbamazepin (görcsök és fájdalom kezelésére) és a modafinil (a fáradtság kezelésére) csökkenthetik az orális fogamzásgátló tabletták hatékonyságát.
Másodlagos progresszív SM és progresszív relapszáló MS
A mitoxantron pozitív hatásokat mutatott azoknál az embereknél, akik másodlagosan progresszív és progresszív relapszusos tanfolyamokat végeztek. Közepesen hatékonyan csökkenti a betegség progresszióját és a visszaesések gyakoriságát két év után. 2007 -ben ez volt az egyetlen gyógyszer, amelyet az Egyesült Államokban jóváhagytak mind a másodlagos progresszív, mind a progresszív relapszusos sclerosis multiplex kezelésére; azonban dózisfüggő szívtoxicitást okoz, ami korlátozza hosszú távú használatát. Európában sem engedélyezett. A natalizumab hatásosnak bizonyult, és jóváhagyták a relapszusokkal járó másodlagos progresszív SM kezelésére. Az interferon-béta-1b másodlagos progresszív és progresszív relapszáló SM-ben történő alkalmazásával kapcsolatos vizsgálatok nem támasztják alá, hogy lassítja a betegség progresszióját, bár hatékonyan csökkenti a visszaesések számát.
Elsődleges progresszív SM
Az elsődleges progresszív sclerosis multiplex (PPMS) kezelése problémás, mivel sok beteg nem reagál semmilyen rendelkezésre álló terápiára, és egyetlen kezelést sem engedélyeztek kifejezetten a betegség ezen formájának alkalmazására. Számos vizsgálatban vizsgálták a különböző gyógyszerek hatékonyságát PPMS -re pozitív eredmények nélkül. 2013 - tól 9 immunmodulátor és immunszuppresszáns szer hálózati metaanalízise azt sugallta, hogy nincs bizonyíték arra, hogy bármelyik hatékonyan megakadályozná a fogyatékosság progresszióját progresszív SM-ben szenvedő embereknél. A vizsgált gyógyszerek közé tartozik a béta -interferon, a mitoxantron, a glatiramer -acetát vagy a riluzol . PPMS -ben szenvedő személyeket is bevontak az azatioprin , metotrexát , intravénás immunglobulin , ciklofoszfamid és vérképző őssejt -transzplantáció kísérleteibe .
2017 márciusában az okrelizumabot jóváhagyták az Egyesült Államokban a primer progresszív szklerózis multiplex kezelésére felnőtteknél. A szklerózis multiplex kiújuló formáinak kezelésére is használják, beleértve a klinikailag izolált szindrómát, a relapszusos-remisszív betegséget és az aktív másodlagos progresszív betegséget felnőtteknél.
Az SM hatásainak kezelése
Rehabilitáció
Foglalkozásterápia
A munkaterápia fontos szerepet játszhat a szklerózis multiplex tüneteinek kezelésében. Ezek a tünetek nem korlátozódnak a remegésre, a járás romlására és az átvitel nehézségeire. Az OT -k segíthetnek a remegés kezelésében, ha apró passzív súlyokkal felszerelik a beteget, hogy csökkentsék a remegés intenzitását. Ami a járásromlást illeti, a foglalkozási terapeuták segíthetnek egy konkrét járásképzési program kidolgozásában, értékelhetik a legmegfelelőbb adaptív eszközöket és eszközöket, és mérlegelhetik a motoros mozgás szükségességét. A foglalkozásterapeuták jártasak az átvitelben, és segíthetnek a szklerózis multiplexben szenvedőknek az átviteli képességeikben, valamint képzést nyújtanak az átviteli technikákról és a segítő eszközök értékeléséről.
Fizikoterápia
Az SM tünetei, amelyek javíthatók, a fáradtság , görcsösség , depresszió , hólyagműködési zavar és neurológiai tünetek. Ezeket a tüneteket gyógytornával és gyógyszeres kezeléssel lehet javítani. A fizikoterapeuták megerősítő gyakorlatokat és nyújtási módokat mutathatnak be; végső soron megkönnyíti a napi feladatokat és csökkenti a fáradtságot, miközben az izomerő növekszik a rugalmasság növekedésével. Az edzésterápia biztonságosan betiltható anélkül, hogy megnövekedne a visszaesés kockázata, és ez a legjobban támogatott rehabilitációs beavatkozás a fáradtság csökkentésére és az izomerő, a mobilitás és az életminőség javítására a Cochrane rehabilitációs szisztematikus áttekintése szerint. Mind a gyógyszeres terápia, mind a neurorehabilitáció bizonyítottan enyhíti bizonyos tünetek terheit, bár egyik sem befolyásolja a betegség előrehaladását. Más tünetek esetén a kezelések hatékonysága még mindig nagyon korlátozott.
A vízi terápiáról is kimutatták, hogy enyhíti a szklerózis multiplex tüneteit. A vízi kerékpározás és az aerob testmozgás biztonságos és hatékony módja az izomerő, állóképesség és keringés fokozásának SM betegeknél. A vízi terápia csökkentette a beteg fájdalmát, elősegítette a depressziót/fáradtságot, és javította a szív -légzőképességet. Összességében ez a módszer jótékony hatással van a mindennapi tevékenységekre és az életminőségre.
Neurorehabilitáció
Bár viszonylag kevés tanulmány található a SM rehabilitációjáról, általános hatékonysága, amelyet egy szakembercsoport végez, egyértelműen bizonyított más betegségek, például stroke vagy fejsérülés esetén is . Mint minden neurológiai betegségben szenvedő beteg esetében, a multidiszciplináris megközelítés kulcsfontosságú a fogyatékosság korlátozásához és leküzdéséhez; különös nehézségeket okoz azonban a „törzscsapat” meghatározása, mivel az SM -ben szenvedő betegeknek szinte bármely egészségügyi szakma vagy szolgáltatás segítségére lehet szükségük valamikor. A neurológusok főként a szklerózis multiplex és az esetleges súlyosbodások diagnosztizálásában és folyamatos kezelésében vesznek részt. A szklerózis multiplexben szenvedő betegek átfogó rehabilitációs folyamatát általában fizikusok irányítják . A szövetséges kezelések, például a fizioterápia , a beszéd- és nyelvterápia vagy a foglalkozási terápia szintén segíthetnek bizonyos tünetek kezelésében és az életminőség megőrzésében . A neuropszichiátriai tünetek, például az érzelmi szorongás és a klinikai depresszió kezelésében olyan mentális egészségügyi szakembereket kell bevonni , mint a terapeuták , pszichológusok és pszichiáterek , míg a neuropszichológusok segíthetnek a kognitív hiányosságok értékelésében és kezelésében .
A multidiszciplináris megközelítések hatékonynak bizonyultak az aktivitási szint növelésében és a szklerózis multiplexben való részvételben. A betegek megértését és részvételét alátámasztó információszolgáltatást vizsgáló tanulmányok azt sugallják, hogy bár a beavatkozások (írásos tájékoztatás, döntési segédeszközök, coaching, oktatási programok) növelhetik a betegek tudását, a döntéshozatalra és az életminőségre gyakorolt hatás bizonyítéka vegyes és alacsony bizonyosságú. A randomizált, kontrollált vizsgálatok kevés volta miatt korlátozott bizonyíték van az egyes terápiás tudományágak általános hatékonyságára, bár jó bizonyíték van arra, hogy a konkrét megközelítések, például a testmozgás, a pszichológiai terápiák, különösen a kognitív viselkedési megközelítések és az energiatakarékossági oktatás hatékonyak. Pontosabban a pszichológiai beavatkozások hasznosnak tűnnek a depresszió kezelésében, míg az egyéb felhasználási módokra, például a kognitív károsodások kezelésére vagy a szakmai tanácsadásra vonatkozó hatékonyság bizonyítéka kevésbé erős. A kognitív tréning önmagában vagy más neuropszichológiai beavatkozásokkal kombinálva pozitív hatással lehet a memóriára és a figyelemre, bár határozott következtetések nem lehetségesek kis mintaszám, változó módszertan, beavatkozások és kimeneti mérések alapján. A palliatív megközelítések hatékonysága a szokásos ellátás mellett bizonytalan, a bizonyítékok hiánya miatt. Nehéz pontosan megmondani, hogy milyen típusú rehabilitáció lesz a legelőnyösebb, mert a terápiákat az egyén sajátos szükségleteinek megfelelően alakítják ki.
Ami a jólétet illeti, a járástanításra összpontosító fizikoterápia létfontosságú lehet az MS-betegek részvételének maximalizálásához a gyaloglás és a mindennapi tevékenységek (ADL) alatti fáradtság csökkentése révén . A legtöbb járástanítást földön (például edzőteremben vagy kint egyenetlen talajon), futópadokon vagy ritkábban robotsegítő eszközökkel végzik. A robot által támogatott testtömeggel támogatott futópad-edzés hatékony terápiás megoldás lehet súlyos járáskárosodásban szenvedő SM-es betegeknél. Ezzel szemben a szárazföldi járásképzés lehet a leghatékonyabb a járási sebesség javításában a kevésbé súlyos károsodásban szenvedő SM betegeknél. A ló által támogatott terápiák, például a terápiás lovaglás és a hippoterápia további kezelések, amelyek pozitívan befolyásolhatják a járást, az egyensúlyt és az életminőséget az SM-ben szenvedő embereknél. Egy másik hatékony módszer, amelyet a fizikai terápiában használnak az MS betegek járásának és egyensúlyának javítására, a vízi terápia . Az SM -ben szenvedő betegek sétálhatnak, funkcionális gyakorlatokat végezhetnek, egyensúlyi edzéseket és nyújtásokat végezhetnek a vízi terápiában, hogy javítsák a járás általános teljesítményét. A vízi terápia nemcsak az MS betegek járását javíthatja, hanem a dinamikus egyensúlyt és a testtartás stabilitását is.
Történelmileg az SM -ben szenvedő egyéneket tanácsolták, hogy a súlyosbodó tünetek miatt ne vegyenek részt fizikai aktivitásban. Szakértő irányítása mellett azonban a fizikai tevékenységekben való részvétel biztonságos lehet, és bizonyítottan előnyös az SM -ben szenvedő személyek számára. A kutatás támogatta a fizikai aktivitás rehabilitációs szerepét az izomerő, a mobilitás, a hangulat, a bél egészségének, az általános kondíció és az életminőség javításában. A beavatkozások, köztük a testmozgás hatékonysága, különösen az MS -ben szenvedő emberek elesésének megelőzésére, bizonytalan, miközben bizonyítékok vannak arra, hogy hatással vannak az egyensúly működésére és a mobilitásra. A személytől függően a tevékenységek magukban foglalhatják az ellenállóképzést, a sétát, az úszást, a jógát, a tai chi -t és másokat. A megfelelő és biztonságos edzésprogram meghatározása kihívást jelent, és gondosan személyre kell szabni, hogy minden személy figyelembe vegye az összes ellenjavallatot és óvintézkedést.
Megnövekedett maghőmérsékletet észleltek, amely a tünetek fokozottabb megjelenéséhez vezetett a testmozgás során, a napi cirkadián testhőmérséklet változásai miatt, valamint a hőhatás miatt, beleértve a meleg hőmérsékletet, meleg zuhanyokat, napozást stb. túlhevítse az SM -es személyt a gyakorlat során. Van néhány bizonyíték arra, hogy a hűtési intézkedések hatékonyan lehetővé teszik a nagyobb mértékű testmozgást: hidegzuhanyok, hidegvizes végtagmerülés, jégcsomagolás és hideg italok fogyasztása. Ezek a stratégiák akkor hatékonyak, ha az edzés után a maghőmérsékletet kívánják csökkenteni, és előhűtésként a fizikai aktivitás vagy a hőhatás előtt.
2021. március 26-án az Amerikai Egyesült Államok Élelmiszer- és Gyógyszerügyi Hivatala (FDA) engedélyezte egy új eszköz forgalomba hozatalát, amely a sclerosis multiplex (MS) enyhe vagy közepes tünetei miatt a járáshiány rövid távú kezelésére szolgál. A készüléket csak orvosi rendelvényre szabad használni felügyelt terápiás edzésprogram kiegészítéseként 22 éves és idősebb betegeknél. A hordozható neuromodulációs stimulátornak (PoNS) nevezett eszköz egy neuromuszkuláris nyelvstimulátor, amely egy nem beültethető készülékből áll, amely elektromos impulzusokat állít elő a trigeminális és az arcidegek nyelven keresztüli stimulálására, a motoros hiányok kezelésére. A PoNS eszköz egy hordozható, nem beültethető eszköz, amely enyhe neuromuscularis elektromos stimulációt biztosít a nyelv háti felületére.
Orvosi kezelések a tünetek kezelésére
A szklerózis multiplex számos tünetet okozhat, beleértve az érzékenység megváltozását ( hypoesthesia ), izomgyengeséget, rendellenes izomgörcsöket, mozgásszervi zavarokat, koordinációs és egyensúlyzavarokat, beszédproblémákat ( diszartria ) vagy nyelési nehézségeket ( dysphagia ), látási problémákat ( nystagmus) , látóideggyulladás vagy diplopia ), fáradtság és akut vagy krónikus fájdalom szindróma, hólyag- és bélproblémák , kognitív károsodás vagy érzelmi tünetek (főleg depresszió ). Ugyanakkor minden tünet esetében különböző kezelési lehetőségek állnak rendelkezésre.
- Hólyag : A húgyúti tünetek gyakoriak az SM -ben. A hólyagproblémák kezelése a diszfunkció eredetétől vagy típusától függően változik, de elsősorban a hólyagkontroll és az inkontinencia , valamint a húgyúti fertőzések kezelésére osztható . Ami a hólyagkontrollot illeti, néhány példa a felhasznált gyógyszerekre a nocturia elleni desmopresszin és az antikolinerg szerek, mint például az oxibutinin és a tolterodin a vizelet sürgősségére . A nem gyógyszeres kezelés magában foglalja a medencefenék izomképzését , stimulációját, pesszáriumokat , hólyag-átképzést, a mindennapi élet szokásainak megváltoztatását, például ruházatot, külső vizeletgyűjtő eszközök használatát férfiaknál és inkontinencia betéteket nőknél; és néha szakaszos vizeletkatéterezés . Ami a hosszú távú katéterezést illeti, a húgyúti fertőzésekhez kapcsolódik, és lehetőség szerint kerülni kell. Ezen ajánlások némelyike nem az MS -ben végzett konkrét vizsgálatokból származik, hanem általános ajánlások azok számára, akik neurogén hólyaggal rendelkeznek .
- Bél : a bélproblémák a betegek körülbelül 70% -át érintik, a betegek körülbelül 50% -a székrekedésben és 30% -ban székletinkontinenciában szenved . A bélműködés károsodásának okai az SM betegekben általában a bélmozgás csökkenése vagy a székletürítés neurológiai kontrolljának romlása . Az előbbi általában a betegség kezelésére használt gyógyszerek mozgásképtelenségéhez vagy másodlagos hatásaihoz kapcsolódik . A fájdalom vagy a székelési problémák segíthetnek az étrend megváltoztatásában, amely többek között megnövelt folyadékbevitelt, szájon át szedhető hashajtókat vagy kúpokat és beöntéseket tartalmaz, amikor a szokások megváltoztatása és a szóbeli intézkedések nem elegendőek a problémák kezelésére.
- Kognitív és érzelmi : a neuropszichiátriai tünetek gyakoriak a betegség során. A depresszió és a szorongás a betegek akár 80% -ánál is megjelenik. Gyakori az érzelmi labilitás is, amely kontrollálatlan síráshoz vezet. Ezek a tünetek kezelhetők antidepresszánsokkal és kognitív viselkedésterápiával ; azonban hiányoznak a hatékonyságra vonatkozó magas színvonalú vizsgálatok. Például az antidepresszánsok és a depresszió konkrét esetében a Cochrane -együttműködés 2011 -ig csak két vizsgálatot tartott érdemesnek megfontolni, és ezek csak a hatékonyság irányába mutattak. További neuropszichiátriai tünetek az eufória és a gátlás . A kognitív károsodás az SM gyakori szövődménye, még a betegségmódosító kezelések bevezetése után is az elmúlt 20 évben. Bár a betegség általában a kognitív problémák elsődleges oka, más tényezők, például gyógyszerek, visszaesések vagy depresszió fokozhatják ezeket, ezért fontos a hiányok és az őket súlyosbító tényezők helyes értékelése. Ami az elsődleges hiányokat illeti, az adatok arra utalnak, hogy az L-amfetamin és a metil - fenidát beadása hasznos lehet, míg a memantin és az antikolinészteráz- gyógyszerek, például a donepezil-amelyeket gyakran használnak Alzheimer-kórban- nem tekinthetők hatékonynak a kognitív funkciók javításában. A kognitív rehabilitációs terápia hatékonysága inkább vitatott. Azoknál az MS -ben szenvedő betegeknél, akiknek pszeudobulbáris affektusuk (PBA) van, amelyet sírás és/vagy nevetés ellenőrizhetetlen epizódjai vagy más érzelmi megjelenések jellemeznek, a dextrometorfán/kinidin kezelésnek tekinthető, mivel ez az egyetlen FDA által jóváhagyott gyógyszer a PBA kezelésére, bár más gyógyszereket, például szelektív szerotonin -visszavétel -gátlókat , triciklusos antidepresszánsokat alkalmaztak a klinikai gyakorlatban.
- Dysphagia diszartria : dysphagia olyan nehézség az evés és a nyelés, ami okozhat fulladást és aspirációs étel vagy folyadék a tüdőben , míg artikulációs egy neurológiai motoros beszédzavar jellemző a gyenge felett az alrendszerek és felelős izmokat beszéd ( „artikuláció” ). A beszéd- és nyelvterapeuta tanácsokat adhat bizonyos nyelési technikákról, az élelmiszer -konzisztencia és a táplálékbevitel kiigazításáról, a beszédképzés és -értelmezés javítására és fenntartására szolgáló technikákról, valamint az alternatív kommunikációs módszerekről . Előrehaladott dysphagia esetén az ételt nasogastricus csővel lehet ellátni , amely egy cső, amely az orron keresztül közvetlenül a gyomorba megy; vagy perkután endoszkópos gasztrosztómia (PEG), amely egy eljárás a cső gyomorba helyezésére, és ezért közvetlenül a táplálék beadására.
- Erekciós diszfunkció : Az erekciós zavar gyakori az SM -ben szenvedő férfiaknál. Van néhány bizonyíték arra, hogy a szildenafil -citrát hasznos kezelés lehet. A prosztaglandin E1 számos okból, köztük a szklerózis multiplex miatt, előnyösnek bizonyult a merevedési zavarban szenvedő betegek számára.
- Fáradtság : a fáradtság nagyon gyakori és fogyatékos az SM -ben, ugyanakkor szoros kapcsolatban áll a depressziós tünetekkel. Ha a depresszió csökken, a fáradtság is javul, ezért a betegeket más terápiás módszerek alkalmazása előtt értékelni kell a depresszió szempontjából. Hasonló módon más tényezők, mint például a zavart alvás, a krónikus fájdalom, a rossz táplálkozás vagy akár egyes gyógyszerek is hozzájárulhatnak a fáradtsághoz; ezért az egészségügyi szakembereket arra ösztönzik, hogy azonosítsák és módosítsák azokat. Néhány gyógyszert tanulmányoztak az SM-hez kapcsolódó fáradtság kezelésére, például az amantadin- pemolint (amely a figyelemhiányos hiperaktivitási zavar és a narkolepszia kezelésére is használt pszichostimuláns ), vagy a modafinilt , valamint az energiamegtakarítás pszichológiai beavatkozásait, de mindegyik kicsi. A fáradtság tehát nagyon nehezen kezelhető tünet, amelyre semmilyen gyógyszert nem javasolnak.
- Fájdalom : az akut fájdalom főként a látóideggyulladásnak köszönhető (a kortikoszteroidok a legjobb kezelés), valamint a trigeminális neuralgia , a Lhermitte -jel vagy a diszesztézia . A szubakut fájdalom általában másodlagos a betegséghez, és annak következménye lehet, hogy túl sokáig tartózkodik ugyanabban a helyzetben, vizeletvisszatartás és fertőzött bőrfekély. A kezelés az októl függ. A krónikus fájdalom nagyon gyakori és nehezebben kezelhető, mivel leggyakoribb oka a diszesztézia. A trigeminális neuralgia okozta akut fájdalmat általában sikeresen kezelik görcsoldó szerekkel, például karbamazepinnel vagy fenitoinnal . Mind a Lhermitte -jel, mind a fájdalmas diszesztézia általában reagál a karbamazepin- , klonazepám- vagy amitriptilin -kezelésre . A Sativex -et különböző országokban a fájdalom kezelésére használják az SM -ben, de kannabiszból való származása miatt jelenleg nem elérhető más országokban, például az USA -ban. Ezt a gyógyszert más SM tünetek, például görcsösség kezelésére is vizsgálják, és hosszú távú biztonságosságot és hatékonyságot mutatott. A krónikus fájdalom kezelésére szolgáló nem gyógyszeres beavatkozások hatékonyságára vonatkozó bizonyítékok korlátozottak, nagyon gyenge minőségűek és nem elegendőek ahhoz, hogy önmagában ilyen beavatkozásokat javasoljanak, azonban ezek alkalmazása farmakológiai hatóanyagokkal kombinálva ésszerű lehet.
- Spasticitás : a spasticitást a végtagok mozgásának fokozott merevsége és lassúsága , bizonyos testhelyzetek kialakulása, az önkéntes izomerő gyengeségével , valamint a végtagok akaratlan és néha fájdalmas görcsei jellemzik. A fizioterápia segíthet csökkenteni a görcsöket és elkerülni a kontraktúrák kialakulását olyan technikákkal, mint a passzív nyújtás . A Nabiximols biztonságos és hatékony a görcsök enyhítésére. Bizonyítékok vannak, bár korlátozottak, de a baklofen , a dantrolén , a diazepám és a tizanidin klinikai hatékonyságára . A legbonyolultabb esetekben intratekális baclofen injekciót lehet alkalmazni. Vannak palliatív intézkedések is, például öntvények , sínek vagy testreszabott ülések. A nem farmakológiai beavatkozások között alacsony szintű és korlátozott bizonyíték van arra, hogy a szklerózis multiplexben szenvedő emberek spaszticitása előnyös a fizikai aktivitási programok, a koponyán keresztüli mágneses stimuláció és az impulzusos elektromágneses terápia esetében . A szisztematikus áttekintés azt találta, hogy nincs bizonyíték a transzkután elektromos idegstimuláció, a sportmászás és a vibrációs terápia előnyeire.
- Látás : különböző gyógyszerek, valamint optikai kompenzációs rendszerek és prizmák használhatók a nystagmus vagy diplopia (kettős látás) tüneteinek javítására . Bizonyos esetekben sebészeti beavatkozás is alkalmazható.
- Gyaloglás : A dalfampridin ( ampyra ) széles spektrumú káliumcsatorna-blokkoló . Az FDA jóváhagyta a járási nehézségek kezelésére az SM -ben. Kimutatták, hogy növeli a gyaloglási sebességet, bár magas költsége (havi 1000 dollár felett) korlátozza használatát.
Más tünetek, mint például ataxia , remegés vagy érzékszervi veszteségek , nem rendelkeznek bizonyított kezeléssel. A légzőizom -képzés hatására vonatkozó bizonyítékok heterogének és gyenge minőségűek, míg a fontos eredményekre, például a köhögés hatékonyságára, a tüdőgyulladásra és az életminőségre gyakorolt hatást nem értékelték. Az epilepsziás rohamok potenciálisan súlyos komorbiditást jelentenek a szklerózis multiplexben szenvedő betegeknél, amely nem gyakori, de ennek ellenére gyakrabban fordul elő, mint az általános populációban, azonban jelenleg nincs bizonyíték az epilepszia elleni gyógyszerek hatékonyságára és biztonságosságára, különösen a szklerózis multiplexben szenvedőknél . esetleg a demielinizáló elváltozások másodlagos eredménye, nem gyakori, de potenciálisan súlyos panasz
Kutatás
Az SM kezelésével kapcsolatos kutatási irányok közé tartozik az SM patogenezisének és heterogenitásának vizsgálata; az RRMS hatékonyabb, kényelmesebb vagy tolerálható új kezeléseinek kutatása; terápiák létrehozása a progresszív altípusokhoz; neuroprotekciós stratégiák; és a hatékony tüneti kezelések keresése.
Az elmúlt évtizedekben elért eredmények számos orális gyógyszer közelmúltbeli jóváhagyásához vezettek. Ezek a gyógyszerek várhatóan egyre népszerűbbek és gyakoribbak lesznek a korábban meglévő terápiák rovására. További orális gyógyszereket még vizsgálnak, a legjelentősebb példa a laquinimod , amelyet 2012 augusztusában jelentettek be a harmadik fázis III vizsgálatának középpontjában, miután az előzőekben vegyes eredményeket értek el. Hasonlóképpen, más tanulmányok célja a már meglévő terápiák hatékonyságának és könnyű használatának javítása új készítmények használatával. Ilyen például az interferon-β-1a PEGilált változata, amelynek élettartama hosszabb, mint a normál interferoné, és ezért vizsgálják, ha ritkább dózisban adják-e be, hasonló hatékonysággal rendelkezik, mint a meglévő termék. Egy robusztus kétéves vizsgálat befejezésével bebizonyosodott, hogy a PEGilált béta-1a-interferon a placebóhoz képest nagyobb hatékonysággal csökkenti a relapszus gyakoriságát és a fogyatékosság progresszióját.
Az előzetes adatok azt sugallják, hogy a mikofenolát-mofetil , egy elutasító immunszuppresszáns gyógyszer , előnyös lehet a szklerózis multiplexben szenvedőknél. Egy szisztematikus felülvizsgálat azonban azt találta, hogy a rendelkezésre álló korlátozott bizonyítékok nem elegendőek a mikofenolát-mofetil, mint a béta-1a-interferon kiegészítő terápiájának hatásainak megállapításához RRMS-ben szenvedő betegeknél.
A monoklonális antitestek, amelyek a natalizumabdal azonos családba tartozó gyógyszerek, szintén nagy érdeklődést és kutatást váltottak ki. Az alemtuzumab , a daklizumab és a CD20 monoklonális antitestek, mint például a rituximab , az okrelizumab és az ofatumumab , valamennyire előnyösnek bizonyultak, és tanulmányozzák, mint az SM lehetséges kezeléseit. Ennek ellenére használatukat potenciálisan veszélyes káros hatások, legfőképpen opportunista fertőzések megjelenése kísérte. Ezekhez a vizsgálatokhoz kapcsolódik a közelmúltban kifejlesztett teszt a JC vírus antitestek ellen, amely segíthet megjósolni, hogy a betegeknél nagyobb a kockázata a progresszív multifokális leukoencephalopathia kialakulásának a natalizumab szedése során. Míg a monoklonális antitestek valószínűleg szerepet játszanak a betegség kezelésében a jövőben, úgy vélik, hogy a hozzájuk kapcsolódó kockázatok miatt kicsi lesz.
Egy másik kutatási stratégia két vagy több gyógyszer együttes hatékonyságának értékelése . A politerapia fő indoka az SM -ben az, hogy az érintett kezelések a betegség különböző mechanizmusait célozzák, és ezért használatuk nem feltétlenül kizárólagos. Sőt, szinergiák is lehetségesek, amelyekben a gyógyszer felerősíti egy másik hatását. Ennek ellenére fontos hátrányok is felbukkanhatnak, például antagonizáló hatásmechanizmusok vagy a káros másodlagos hatások fokozása. Bár számos klinikai vizsgálatot végeztek a kombinált terápiával kapcsolatban, egyik sem mutatott elegendő pozitív hatást ahhoz, hogy megfontolható legyen az SM életképes kezelése.
Hasonlóképpen nincs hatékony kezelés a betegség progresszív változataira. A legújabb és a fejlesztés alatt álló gyógyszereket valószínűleg a PPMS vagy az SPMS terápiájaként fogják értékelni, és a korábban meglévő gyógyszerekhez képest javított hatékonyságuk végül pozitív eredményhez vezethet ezekben a betegcsoportokban.
A feszültségfüggő nátriumion-csatornákat befolyásoló gyógyszereket potenciális neuroprotektív stratégiaként vizsgálják, mivel feltételezett szerepe van a nátriumnak a kóros folyamatban, amely axonális sérüléshez és felhalmozódó fogyatékossághoz vezet. Jelenleg nincs elegendő bizonyíték a nátriumcsatorna -blokkolók MS -ben szenvedő emberekre gyakorolt hatására.
Az orvosi képalkotás és az MRI területén egyre nagyobb fejlemények tapasztalhatók, lehetővé téve a betegek jobb áttekintését és megértését az SM -ben, valamint az egyes esetek hatékonyabb kezelési módját.
Őssejt -transzplantáció
Végül, ami a neuroprotektív és speciálisan regeneráló kezeléseket illeti, mint például az őssejt -terápia , miközben kutatásaikat jelenleg nagyon fontosnak tartják, ezek csak ígéretet jelentenek a jövőbeli terápiás megközelítésekhez.
Egy 2018-as tanulmány ígéretes eredményeket talált a relapszáló-remitáló SM-ben, de további kutatásokra van szükség.
CCSVI
2008 -ban Paolo Zamboni érsebész azt javasolta, hogy az SM magában foglaljon egy érrendszeri folyamatot, amelyet krónikus cerebrospinális vénás elégtelenségnek (CCSVI) neveznek , és amelyben az agy vénái összehúzódnak. Vizsgálatában mind a 65 MS -ben szenvedő betegnél megtalálta a CCSVI -t. Ez az elmélet fontos figyelmet kapott a médiában és az SM -ben szenvedők körében, különösen Kanadában. Zamboni kutatásai aggodalmat keltettek, mivel nem vakították el és nem kontrollálták, ráadásul a betegség patofiziológiájára vonatkozó feltételezéseit nem támaszthatják alá ismert adatok. A további tanulmányok vagy nem találtak kapcsolatot, vagy sokkal kevésbé erős kapcsolatot találtak. Ez kifogást emelt a CCSVI -ből származó MS hipotézise ellen. A "felszabadítási eljárást" kritizálták, mivel ez súlyos szövődményekhez és halálhoz vezethet, miközben előnyeit nem bizonyították. Jelenleg nem javasolt a javasolt kezelés alkalmazása, kivéve, ha hatékonyságát ellenőrzött vizsgálatok igazolják. A CCSVI -vel kapcsolatos kutatásokat gyorsan nyomon követik, de a kutatók nem tudták megerősíteni, hogy a CCSVI szerepet játszik -e az SM kialakulásában.
Alternatív kezelések
Az SM betegek több mint 50% -a használhat kiegészítő és alternatív gyógyászatot , bár a számok nagymértékben eltérnek az alkalmazott alternatív gyógyászat definíciójától függően. Az Egyesült Államokban a becslések szerint az SM betegpopulációinak 75% -a legalább egy kiegészítő és alternatív gyógyszert alkalmaz a kezelésre és a tüneti kontrollra. Az ilyen kezelések hatékonyságára vonatkozó bizonyítékok a legtöbb esetben gyengék vagy hiányoznak. A betegek által használt kezelések közé tartozik például az étrend -kiegészítés és az olyan kezelési rendek, mint a D -vitamin, a kalcium, a B12 -vitamin és az antioxidánsok. A D-vitamin-kiegészítés alkalmazása mögött az áll, hogy a vizsgálatok összefüggést mutatnak a D-vitamin-hiány és az SM növekvő progressziója, valamint a D-vitamin gyulladáscsökkentő hatása között. A rendelkezésre álló bizonyítékok azonban a D-vitamin pótlására utalnak, formától és formától függetlenül. Az alkalmazott dózis nem nyújt nyilvánvaló előnyt az SM -ben szenvedő betegek számára olyan intézkedéseknél, mint a kiújulás, a fogyatékosság súlyosbodása és az MRI -elváltozások, míg az egészséggel kapcsolatos életminőségre és fáradtságra gyakorolt hatás nem egyértelmű.
Az antioxidáns terápia esetében a vizsgálatok kimutatták, hogy a reaktív oxidatív fajok szklerózis multiplex -elváltozások kialakulásához vezetnek, amelyekben az antioxidánsok segíthetnek neuroprotektív és immunmoduláló hatások kiváltásában. Valószínűleg a legnyilvánvalóbb betegségmódosító tényező (rosszabb esetben) a dohányzás, ezért meg kell fontolni a dohányzás abbahagyását.
Egyéb alternatív kezelések közé tartoznak a relaxációs technikák, például a jóga , a gyógynövények (beleértve az orvosi kannabisz használatát ), a hiperbár oxigénellátás , a kampós féreggel való önfertőzés (általában helminthikus terápia néven ismert ), valamint a méhméreg-terápia , a reflexológia vagy az akupunktúra . Ami a felhasználók jellemzőit illeti, gyakrabban nők, hosszabb ideig szenvedtek SM -ben, és inkább fogyatékosok. Ezenkívül alacsonyabb szintű elégedettségük van a hagyományos egészségügyi ellátással.
Hivatkozások
További irodalom
- Doshi A, Chataway J (2017. december). "A szklerózis multiplex, gyógyítható betegség" . Klinikai orvostudomány . 17 (6): 530–536. doi : 10.7861/klinikai orvoslás.17-6-530 . PMC 6297710 . PMID 29196354 .
- Faissner S, Gold R (2019). "Progresszív sclerosis multiplex: legújabb terápiás fejlemények és jövőbeli irányok" . A neurológiai rendellenességek terápiás fejlődése . 12 : 1756286419878323. doi : 10.1177/1756286419878323 . PMC 6764045 . PMID 31598138 .
Klinikai irányelvek: A klinikai iránymutatások olyan dokumentumok, amelyek célja a döntések és kritériumok irányítása az egészségügy bizonyos területein, a jelenlegi bizonyítékok ( bizonyítékokon alapuló orvoslás ) hiteles vizsgálata alapján .
- Nemzeti Együttműködő Központ a Krónikus Betegségekért (Egyesült Királyság) (2004). Szklerózis multiplex. Országos klinikai iránymutatás az alap- és másodlagos ellátás diagnózisához és kezeléséhez . Nemzeti Egészségügyi és Klinikai Kiválósági Intézet: Útmutató. London: Royal College of Physicians. ISBN 978-1-86016-182-7. PMID 21290636 . NBK48919. Ez a kiadvány csak tájékoztató jellegű, és az információ elavult lehet.
- Szklerózis multiplex felnőtteknél: kezelés (PDF) . Nemzeti Egészségügyi és Gondozási Kiválósági Intézet (NICE). 2014. október ISBN 978-1-4731-0778-6. CG186. Lay összefoglaló .